Clear Sky Science · ru
Можно ли применять эволюционную терапию при немелкоклеточном раке легкого?
Переосмысление лечения рака как эволюционной борьбы
Уход за больными раком часто изображают как простую битву: дать максимально сильные лекарства и постараться истребить каждую последнюю раковую клетку. Однако при быстрых агрессивных опухолях, таких как прогрессирующий немелкоклеточный рак легкого (НМРЛ), этот подход «максимальной атаки» часто дает обратный эффект. Сначала опухоли уменьшаются, но почти всегда затем снова разрастаются, уже за счёт лекарственно‑резистентных клеток. В этом исследовании поставлен провокационный вопрос: что если вместо попытки уничтожить опухоль врачи будут лечить её как развивающуюся экосистему и применять схемы лечения, которые целенаправленно поддерживают часть чувствительных к препарату клеток, чтобы сдерживать резистентные?
Почему стандартная высокодозная терапия может ускорять развитие резистентности
В современной практике пациенты с метастатическим НМРЛ и определёнными генетическими изменениями часто принимают ежедневные таблетки — ингибиторы тирозинкиназы (ТИК), такие как эрлотиниб. Эти препараты могут резко сокращать опухоль в начале, но почти все пациенты в итоге сталкиваются с рецидивом, потому что выживают резистентные клетки. Когда врачи доводят дозу до максимально переносимой, они в основном убивают чувствительные клетки, хорошо реагирующие на препарат. Резистентные клетки, способные выживать даже при высоких дозах, внезапно оказываются без конкуренции за пространство и ресурсы. Итог — эволюционная «победа» самых стойких раковых клеток, и опухоль возвращается, теперь гораздо труднее поддаваясь лечению. 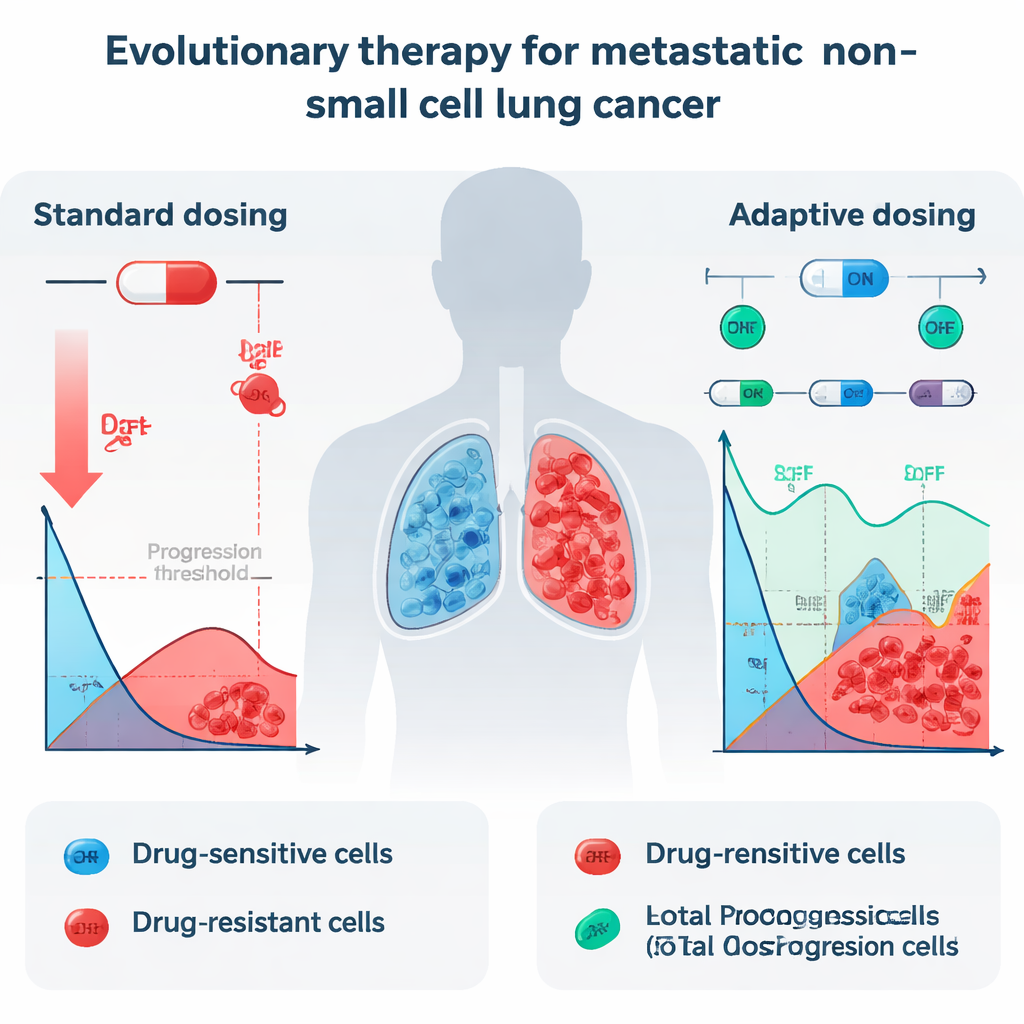
Использование математики для тестирования новой схемы дозирования на реальных пациентах
Исследователи изучили, может ли иная стратегия, называемая эволюционной терапией, сработать при IV стадии НМРЛ. Эволюционная терапия не стремится полностью искоренить опухоль. Вместо этого она пытается контролировать её, удерживая стабильный баланс чувствительных и резистентных клеток, позволяя чувствительным клеткам «перекрывать» резистентные. Команда взяла конкретный протокол приёма «вкл–выкл», который уже показал обещающие результаты при раке простаты, и задала вопрос: был бы этот подход теоретически эффективен и для рака легкого? Для ответа они проанализировали детальные измерения размеров опухолей у 13 пациентов с НМРЛ, лечившихся эрлотинибом в клиническом исследовании, преобразовали сканы в общий объём опухоли во времени и использовали эти данные в наборе математических моделей.
Поиск модели, которая действительно отражает развитие резистентности
Авторы протестировали 26 различных моделей роста опухоли, все разделявшие раковые клетки на две группы: чувствительные к препарату и резистентные. Эти модели различались описанием предельного роста, механизмами конкуренции между двумя типами клеток, фармакокинетикой препарата и способами гибели клеток под действием лечения. Многие более простые модели достаточно хорошо описывали данные пациентов, когда опухоли только уменьшались. Но когда опухоли следовали более реалистичной «U‑образной» траектории — сначала сокращались под лечением, а затем снова росли из‑за появления резистентности — большинство моделей давали сбой. Лучшим соответствием оказалась модель типа Гомперца, включающая две ключевые идеи: во‑первых, опухоли не могут расти бесконечно (они испытывают эффект уплотнения), и, во‑вторых, чувствительные и резистентные клетки конкурируют асимметрично, так что успех одного типа зависит от числа клеток другого типа.
Моделирование адаптивной терапии против стандартного лечения
Когда команда определила модели с наилучшей подгонкой, они использовали их для симуляции двух стратегий лечения для каждого пациента: обычной постоянной максимальной дозы и адаптивного протокола в духе работы Чжан и соавторов. В адаптивном подходе эрлотиниб даётся до тех пор, пока опухоль не уменьшится до половины исходного объёма, затем препарат приостанавливают, чтобы позволить чувствительным клеткам восстановиться; лечение возобновляют, когда опухоль возвращается к исходному объёму, и цикл повторяется. По всем хорошо работающим моделям, которые включали конкуренцию между типами клеток, эта адаптивная стратегия постоянно откладывала момент, когда опухоль превышала 110% от исходного размера — общий критерий прогрессирования. В лучшей по подгонке Гомперцевой модели с конкуренцией медианное время до прогрессирования увеличилось примерно с 24,8 месяцев при стандартной дозировке до 42,3 месяцев при адаптивном протоколе, что даёт прирост примерно в полтора года. 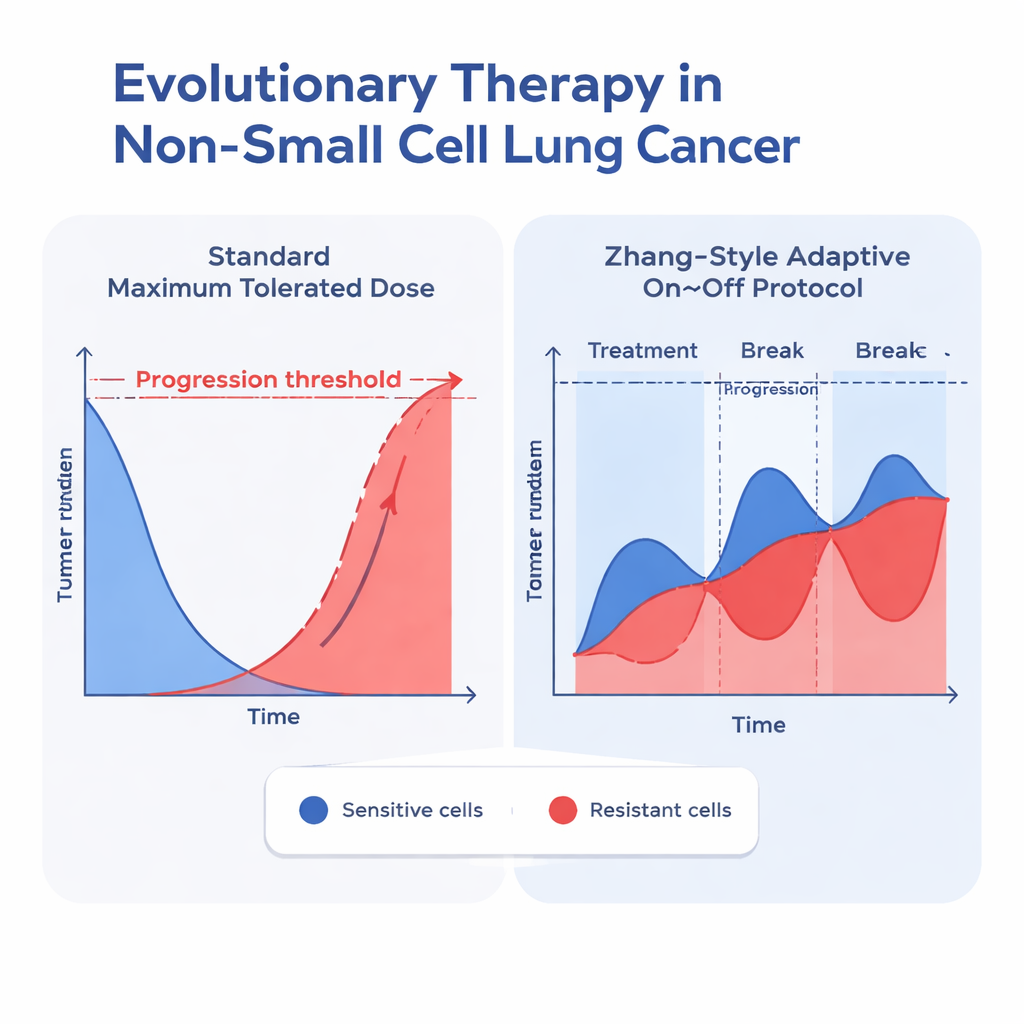
Что это может означать для будущих пациентов
Эта работа пока не меняет то, как врачи лечат пациентов с НМРЛ сегодня, но она даёт убедительное доказательство концепции. Опираясь на реальные данные пациентов и требуя, чтобы модели воспроизводили не только первоначальное сокращение опухоли, но и последующий рост, вызванный резистентностью, авторы показывают, что эволюционная терапия теоретически осуществима даже при быстром и опасном раке. Их результаты предполагают, что тщательно рассчитанные перерывы в лечении могут продлить контроль над заболеванием, используя чувствительные к лекарству клетки как союзников, а не как побочный ущерб. Чтобы превратить эту идею в клиническую практику, потребуется больше данных, лучшие биомаркеры — например, анализ крови для отслеживания опухолевой ДНК — и строгие клинические испытания. Тем не менее посыл для широкого читателя ясен: иногда самый умный способ бороться с раком — не наносить ему максимальный урон, а управлять его эволюцией, чтобы он оставался контролируемым, медленнее движущимся противником.
Цитирование: Jansén-Storbacka, L.R., Honasoge, K.S., Molnárová, E. et al. Can evolutionary therapy be applied in non-small cell lung cancer?. Sci Rep 16, 7442 (2026). https://doi.org/10.1038/s41598-026-36712-x
Ключевые слова: эволюционная терапия, немелкоклеточный рак легкого, резистентность к лекарствам, адаптивная дозировка, математическая онкология