Clear Sky Science · ru
Применение Lactococcus, экспрессирующего коллагеноподобный белок Scl1 группы A стрептококков, в качестве новой иммунотерапии против аденокарциномы протоков поджелудочной железы
Превращение дружественных бактерий в бойцов против рака
Рак поджелудочной железы — один из самых смертельных видов рака, отчасти потому, что он скрывается за мощными защитными барьерами, подавляющими иммунную систему организма. В этом исследовании изучается неожиданный союзник в борьбе с заболеванием: обычная «полезная» молочная бактерия, перепрограммированная так, чтобы направляться к опухолям поджелудочной железы и помогать иммунной системе эффективнее их атаковать. Заимствовав «липкий» поверхностный белок у опасного стрептококка, исследователи превратили безвредный микроорганизм в целенаправленный противораковый инструмент в моделях на мышах.
Сложный рак, который перехитривает иммунную систему
Аденокарцинома протоков поджелудочной железы чрезвычайно летальна: примерно только один из восьми пациентов жив через пять лет после диагноза. Одной из главных причин является микроокружение опухоли — плотная, подобная рубцу оболочка, наполненная поддерживающими клетками и молекулами, которые притупляют иммуный ответ и блокируют многие лекарства. Среди виновников — внеклеточные сети нейтрофилов, или NETs — сети из ДНК и белков, которые нейтрофилы выбрасывают в окружение. В случае рака поджелудочной железы эти липкие сети приносят больше вреда, чем пользы: они способствуют росту опухоли, удерживают киллерные Т‑клетки в стороне и связаны с худшими исходами. Блокирование NETs при одновременном пробуждении противоопухолевого иммунитета стало привлекательной стратегией.
Заимствование «липкого» белка без опасного микроба
Ранее было показано, что поверхностный белок группы A Streptococcus, называемый Scl1, способен как прикрепляться к волокнам, ассоциированным с опухолью, так и подавлять образование NETs, замедляя рост опухоли поджелудочной железы у мышей. Но группа A стрептококков — это также возбудитель ангины и тяжёлых инвазивных инфекций, поэтому его нельзя использовать в виде живой терапии. Чтобы сохранить полезный белок и избежать опасного микроба, команда генетически модифицировала Lactococcus lactis — пробиотик, широко применяемый в пищевой промышленности и считающийся безопасным, — чтобы выставлять Scl1 на своей поверхности. Этот новый штамм, обозначенный Lactococcus::620, был протестирован у мышей с опухолями поджелудочной железы, как в простых моделях с опухолями на боку, так и в более реалистичных моделях, где опухоли растут непосредственно в поджелудочной железе.
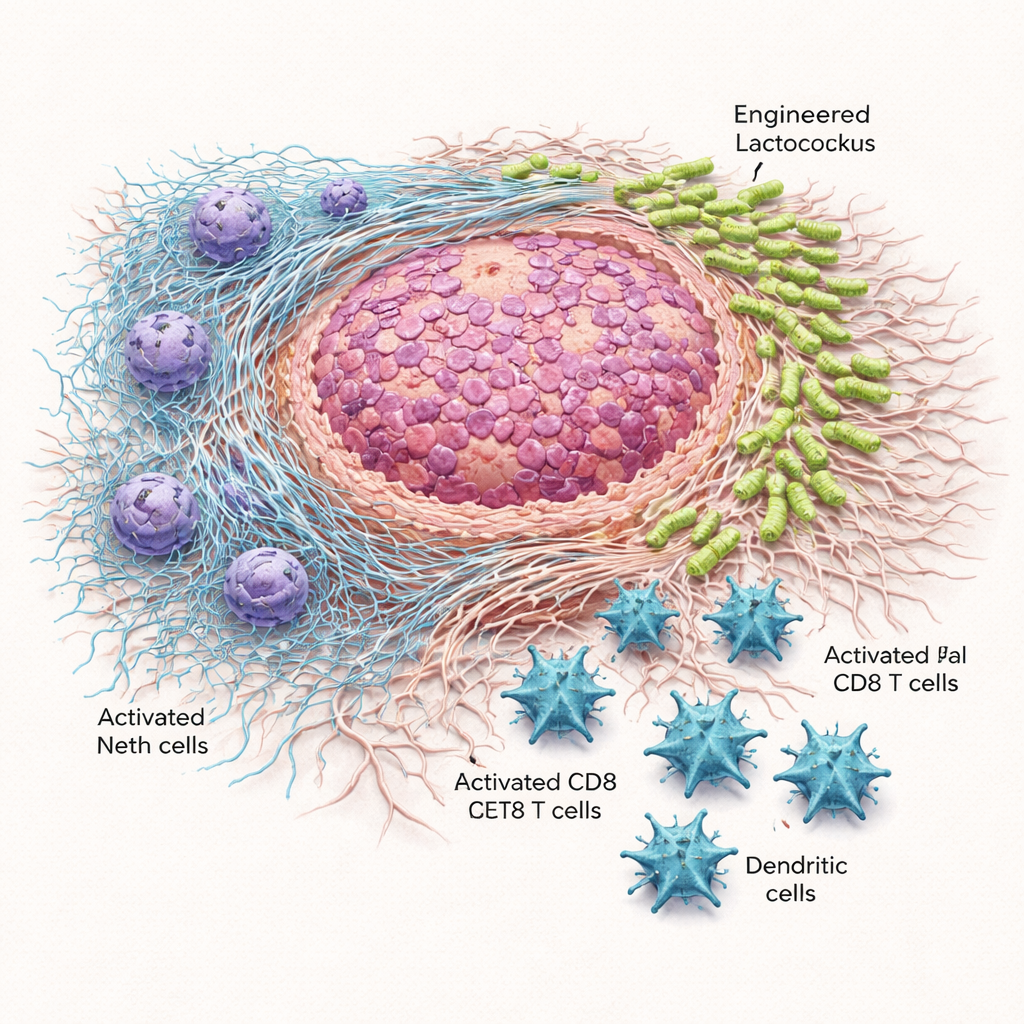
Направленные бактерии замедляют рост опухоли и продляют выживание
Когда однократную дозу модифицированных бактерий вводили прямо в опухоли на боку или доставляли в брюшную полость, опухоли росли медленнее и имели меньшую массу по сравнению с мышами, получавшими обычный Lactococcus или физиологический раствор. В более требовательной модели поджелудочной железы потребовалось многократное введение каждые три дня, но преимущества были заметны. Lactococcus::620 уменьшал размер опухолей, снижал их массу и продлевал выживание животных без причинения летальных исходов, связанных с лечением. Микроскопия и посевы ткани опухоли показали, что бактерии, несущие Scl1, последовательно накапливались в области опухоли, особенно в фиброзной матрице, образуемой фибробластами, ассоциированными с опухолью, при этом в основном обходили селезёнку. Напротив, немодифицированный Lactococcus распространялся шире по организму и иногда оказывал токсическое действие при системном введении.
Обезвреживание вредных сетей и пропускание иммунных клеток
Модифицированные бактерии также перестроили иммунный ландшафт вокруг опухолей. Опухоли у мышей, получавших Lactococcus::620, содержали больше CD8 «киллерных» Т‑клеток и дендритных клеток — ключевых участников распознавания и уничтожения раковых клеток — и эти Т‑клетки демонстрировали меньше маркеров истощения и больше молекул, связанных с активностью. Одновременно снизились показатели активности NETs. В лабораторных испытаниях нейтрофилы, подвергшиеся воздействию Lactococcus::620, выделяли меньше свободной ДНК и показывали более низкую активность миелопероксидазы — фермента, необходимого для формирования NETs. У обработанных мышей уровень циркулирующей ДНК, связанной с NETs, был снижен. Важно, что при проведении тех же экспериментов на мышах, генетически неспособных формировать NETs, модифицированные бактерии уже не замедляли рост опухолей. Потеря терапевтического эффекта сильно указывает на то, что блокирование NETs является ключевым механизмом действия терапии.
Что это может означать для будущей онкопомощи
В целом результаты очерчивают новую концепцию: использование безопасной пищевой бактерии как программируемого носителя для доставки враждебной среде рака поджелудочной железы белка, блокирующего NETs и направляющегося в опухоль. У мышей такой подход уменьшал опухолевую нагрузку, улучшал выживаемость и открывал путь для более эффективной работы иммунных клеток. Хотя предстоит много работы, прежде чем подобная стратегия сможет быть испытана на людях — в том числе тестирование в моделях метастатического заболевания и сочетание с современными иммунотерапиями — исследование показывает, что тщательно сконструированные «полезные» бактерии однажды могут помочь изменить баланс в борьбе с одним из самых устойчивых видов рака.
Цитирование: Godfrey, E.A., Choi, S.J., Sestito, M. et al. Application of group A streptococcal collagen-like protein 1-expressing Lactococcus as a novel immunotherapeutic against pancreatic ductal adenocarcinoma. Sci Rep 16, 5911 (2026). https://doi.org/10.1038/s41598-026-36657-1
Ключевые слова: рак поджелудочной железы, пробиотическая терапия, опухолевое микроокружение, модуляция иммунитета, внеклеточные сети нейтрофилов