Clear Sky Science · ru
Микросреда опухоли при раке пищевода и её связь с клиническими характеристиками и ответом на неоадъювантную терапию
Почему важно «окружение» опухоли
Рак пищевода — один из наиболее смертоносных видов рака в мире, и даже при современной химио- и радиотерапии многие пациенты не отвечают на лечение так хорошо, как хотелось бы. В этом исследовании поставлен на первый взгляд простой, но важный вопрос: что происходит в «окрестностях» опухоли — в её микросреде — и может ли её состав объяснить, почему одни пациенты реагируют на терапию, а другие нет? Тщательно изучая иммунные клетки и связанные маркеры до и после лечения, исследователи начинают картографировать взаимодействие организма и опухоли и то, как этот скрытый диалог может направлять более персонализированное лечение в будущем.
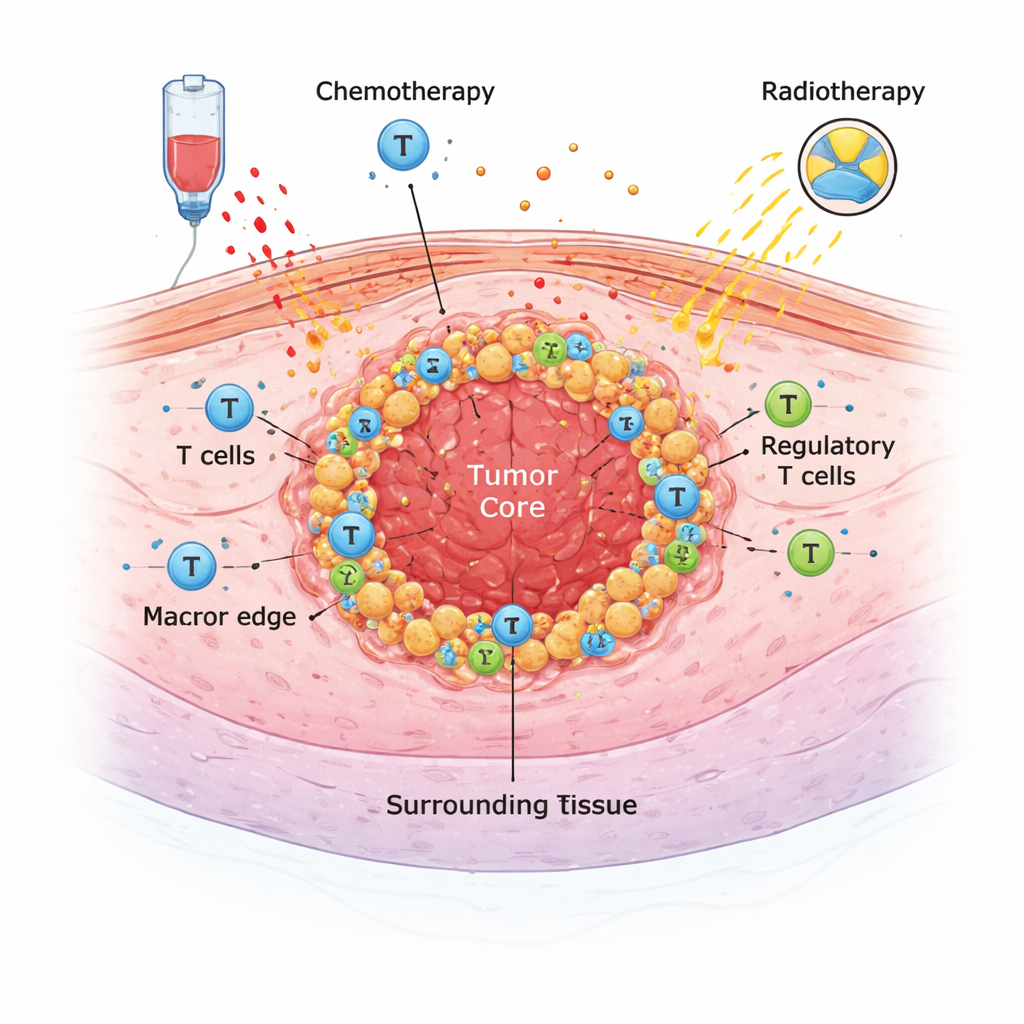
Скрытая экосистема вокруг опухоли
Твердые опухоли не растут в изоляции. Они существуют в сложной экосистеме иммунных клеток, поддерживающих клеток и сигнальных молекул, известной как микросреда опухоли. В этом исследовании врачи и патологи в Лозанне изучили образцы опухоли у 68 пациентов, перенесших операцию по поводу рака пищевода в период с 2009 по 2021 год. Большинство получали интенсивное лечение перед операцией — химиотерапию, химиолучевую терапию или их комбинацию — для уменьшения размера опухоли. С помощью специальных окрашиваний на срезах ткани команда подсчитывала несколько ключевых типов иммунных клеток (включая общие Т-клетки, цитотоксические Т-клетки и разные типы макрофагов) и измеряла маркеры, которые могут предсказать ответ на иммунотерапию, такие как PD-L1 и HER2.
Кто были пациенты и что измеряли
Пациенты в этой серии в основном были мужчинами в возрасте около шестидесяти лет, и у большинства был аденокарцином — тип рака пищевода, часто связанный с хроническим кислотным рефлюксом и пищеводом Барретта. Меньшая группа имела плоскоклеточный рак, другую форму, возникающую из плоского эпителия пищевода. Исследователи тщательно сопоставляли наблюдения под микроскопом с клиническими данными, такими как стадия заболевания, статус курения, потеря веса и вид предоперационного лечения. Они также отслеживали, насколько полно каждая опухоль отвечала на терапию, используя систему градации, которая различает полное исчезновение раковых клеток и отсутствующий либо слабый ответ.
Образ жизни, тип опухоли и ослабленное иммунное присутствие
Несколько повседневных и связанных с заболеванием факторов оказались связанными с более слабым иммунным присутствием вокруг опухоли. Пациенты — активные курильщики имели меньше макрофагов в целом и меньше так называемых M2-подобных макрофагов, которые часто ассоциируются с поддержкой опухоли и иммунным подавлением. У людей с более продвинутыми опухолями, большей предоперационной потерей веса или плоскоклеточным раком, как правило, отмечалось меньшее проникновение Т-клеток и макрофагов в опухоль. Напротив, опухоли с высоким уровнем PD-L1 — показатель, часто используемый при отборе пациентов для иммунотерапии — были «горячее», с большим количеством Т-клеток и макрофагов, но эта картина ранее связывалась с худшими исходами, вероятно потому, что опухоль активно использует PD-L1 для выключения иммунной атаки.
Как лечение перестраивает «окружение» опухоли
Неоадъювантное (предоперационное) лечение существенно перестраивало микросреду опухоли. И химиотерапия, и химиолучевая терапия увеличивали количество макрофагов, включая M2-подобные клетки, в то время как резко снижали количество регуляторных Т-клеток — группы клеток, которые обычно подавляют иммунные ответы. Общие числа Т-клеток и цитотоксических Т-клеток менялись менее последовательно. Интересно, что химиолучевая терапия имела тенденцию снижать уровни PD-L1 на опухолевых и окружающих клетках, уменьшая долю пациентов с высокими показателями PD-L1 после лечения. Это предполагает, что стандартное лечение может сделать опухоли менее подходящими для иммунотерапии с блокированием PD-1/PD-L1, если оценивать только по единственной послетерапевтической «снимке».
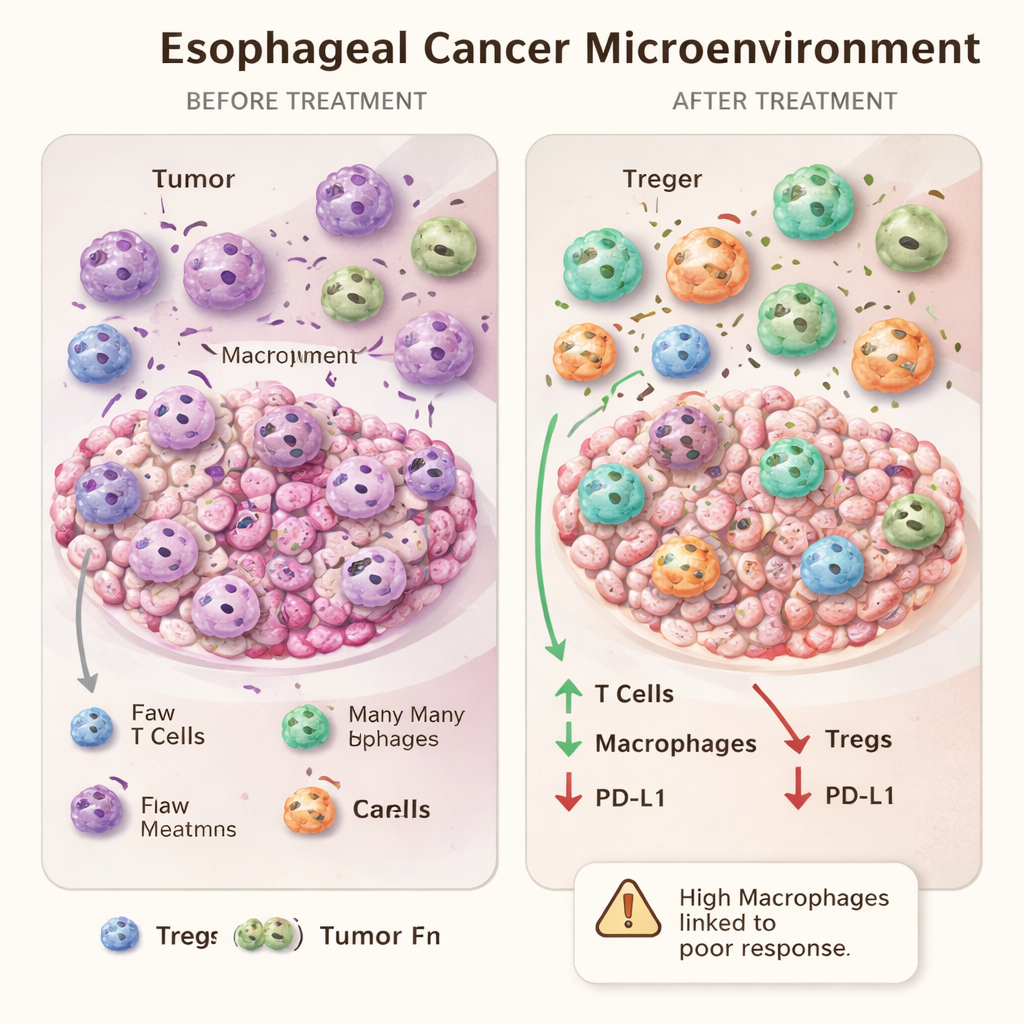
Когда больше иммунных клеток может означать устойчивость к лечению
Одно из наиболее интригующих наблюдений было получено при сравнении крайних ответов на лечение. У пациентов, у которых опухоли полностью исчезали при микроскопическом обследовании, на исходном этапе не было заметных отличий от плохих ответчиков по составу иммунных клеток вокруг рака. Однако после лечения у тех, кто плохо отвечал на терапию, в опухолевых очагах было больше макрофагов по сравнению с полными ответчиками. Вместо простого признака сильного иммунитета избыток макрофагов после терапии может отражать истощённый или смещённый ответ, который опухоль научилась использовать. Это усиливает идею о том, что некоторые макрофаги, особенно M2-подобные, могут фактически способствовать выживанию опухоли и развитию резистентности.
Что это значит для будущего лечения
Для пациентов и клиницистов ключевое послание в том, что биология вокруг опухоли пищевода — её микросреда — формируется курением, типом опухоли, тяжестью заболевания и самими методами лечения. Стандартная химио- и химиолучевая терапия не только уменьшают опухоль; они также привлекают и перестраивают иммунные клетки таким образом, что это может как помогать, так и мешать долгосрочному контролю заболевания. Исследование предполагает, что подсчёт определённых иммунных клеток, в особенности макрофагов, до и после терапии однажды может помочь выявлять тех, кто, вероятно, будет резистентен к лечению, и тех, кто может выиграть от дополнительных препаратов, нацеленных на эти клетки или на путь PD-1/PD-L1. Хотя требуются более крупные исследования, эта работа приблизила нас к персонализации лечения рака пищевода не только по генетике опухоли, но и по динамической экосистеме, которая её окружает.
Цитирование: Fasquelle, F., Teixeira Farinha, H., Sempoux, C. et al. The tumor microenvironment in esophageal cancer and its association with clinical features and neoadjuvant treatment response. Sci Rep 16, 5664 (2026). https://doi.org/10.1038/s41598-026-36537-8
Ключевые слова: рак пищевода, микросреда опухоли, иммунные клетки, химиолучевая терапия, иммунотерапия