Clear Sky Science · ru
Построение и первичная валидация ключевой генетической сети резистентности к прогестерону при раке эндометрия на основе геномного CRISPR-скрининга
Почему некоторые опухоли матки перестают реагировать на гормоны
Для многих людей с ранним раком эндометрия (слизистой оболочки матки), которые хотят сохранить способность иметь детей, гормональные таблетки, имитирующие естественный прогестерон, могут уменьшать опухоль, сохраняя матку. Тем не менее до трети таких опухолей либо изначально не реагируют, либо быстро приобретают устойчивость, вынуждая пациентов прибегать к операции или более жестким методам лечения. В этом исследовании использовали мощный инструмент редактирования генов, чтобы картировать, какие гены заставляют клетки рака эндометрия игнорировать прогестерон, что указывает путь к будущим тестам и препаратам, которые могли бы продлить эффективность этой терапии.
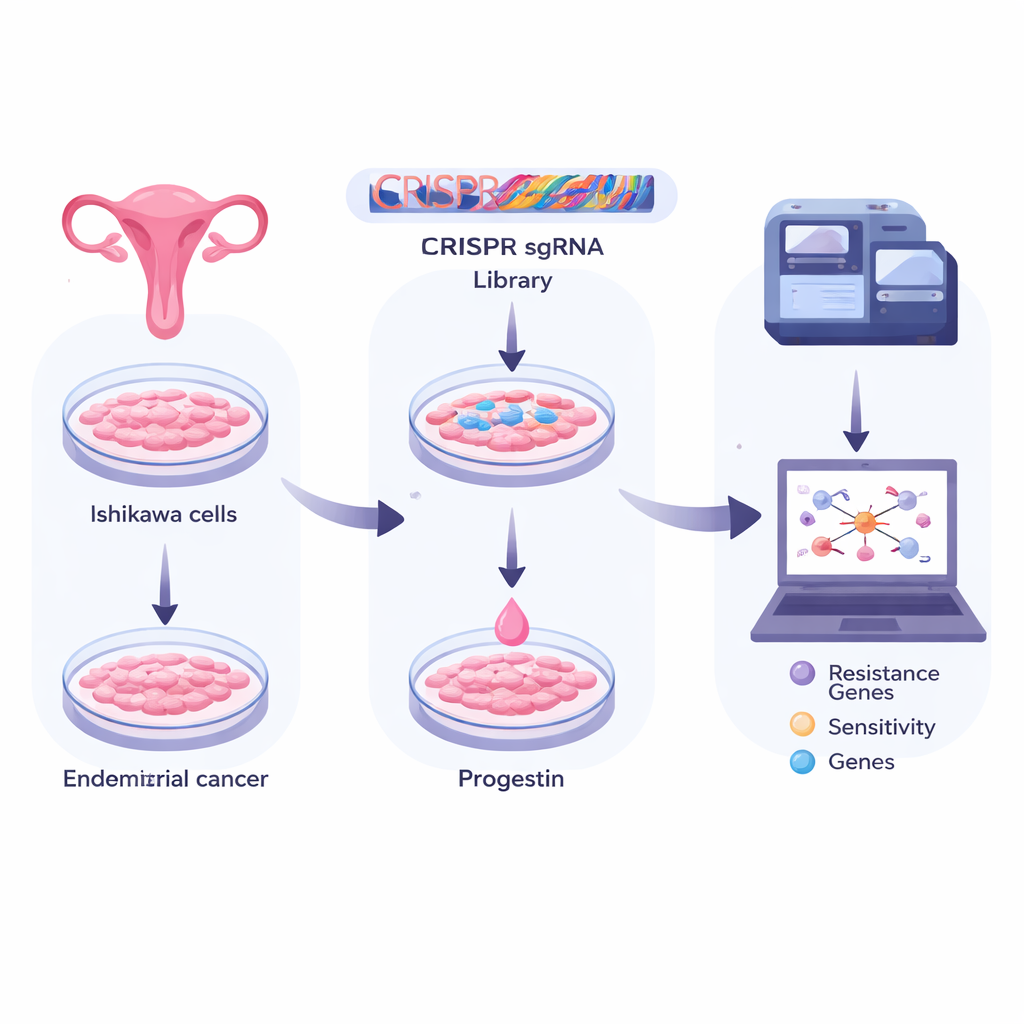
Используя «генные ножницы» для поиска по всему геному
Исследователи работали с клетками Ishikawa, широко используемой моделью рака эндометрия. Они инфицировали миллионы этих клеток библиотекой CRISPR — «генных ножниц», каждая из которых нацелена на выключение отдельного человеческого гена. Это создало огромную популяцию, в которой, по сути, у каждой клетки был деактивирован уникальный ген. Команда затем разделила клетки на группы: одну заморозили как исходную, одну подвергли воздействию лишь безвредного растворителя, и одну лечили в течение многих дней общим синтетическим прогестероном (медроксипрогестерон, MPA). Глубокое секвенирование меток CRISPR, выживших в каждой группе, позволило увидеть, какие нокауты генов помогали клеткам выживать или умирать при лечении прогестероном.
Выделение генов, помогающих или мешающих ответу на препарат
Анализ этого потока данных требовал сложной статистики. Команда применила два взаимодополняющих метода, RRA и MLE, чтобы ранжировать гены по степени их защиты клеток от прогестерона (гены резистентности) или по способности делать клетки более уязвимыми (гены чувствительности). Они нашли по сотням кандидатов в каждом направлении. Многие из этих генов сгруппировались в пути, отвечающие за копирование и ремонт ДНК, синтез и обработку РНК и общий клеточный метаболизм. Иными словами, базовый аппарат, позволяющий клеткам считывать, поддерживать и использовать свою генетическую информацию, тесно связан с тем, будут ли клетки рака эндометрия «слушать» сигнал прогестерона о прекращении роста.
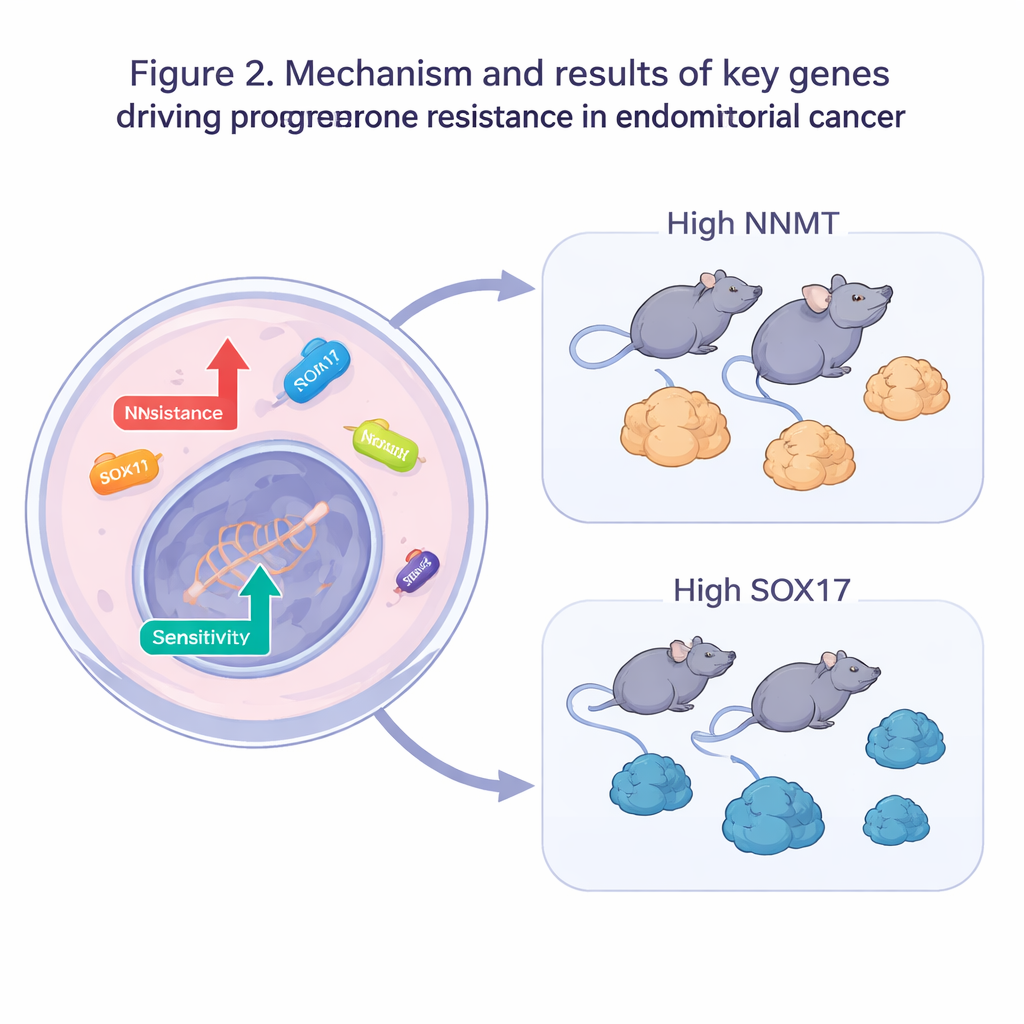
Сужение списка до самых важных участников
Чтобы не гоняться за ложными наводками, ученые сопоставили полученные CRISPR-хиты со старым набором данных из своей лаборатории, где они сравнивали обычные раковые клетки со штаммом, который со временем стал резистентным к прогестерону. Ища гены, встречающиеся в обоих скринингах и демонстрирующие согласованные изменения, они сузили список до пяти генов, которые, по-видимому, способствуют резистентности, и двадцати генов, которые, по-видимому, её подавляют. Публичные онкологические базы данных показали, что многие гены, блокирующие резистентность, более активны в наиболее распространенном типе рака эндометрия, в то время как несколько генов, усиливающих резистентность, коррелируют с худшими исходами у пациентов, что предполагает, что эти сигналы важны в реальных опухолях, а не только в клеточных культурах.
Проверка ключевых генов в клетках и на мышах
Команда затем перешла от больших данных к экспериментам. В клетках, устойчивых к прогестерону, они выключали каждый из пяти подозреваемых генов резистентности или усиливали пять предполагаемых генов чувствительности. При обработке прогестероном такие измененные клетки чаще умирали, и требовались гораздо меньшие дозы препарата, чтобы замедлить рост, что подтвердило, что модификация отдельных генов может восстановить гормоночувствительность. Два гена выделялись особенно ярко: NNMT, вовлеченный в клеточный метаболизм, и SOX17, ген, который помогает контролировать развитие и поведение клеток. В модельных опухолях на мышах повышение экспрессии NNMT делало опухоли менее чувствительными к прогестерону, тогда как усиление SOX17 приводило к большему уменьшению резистентных опухолей при том же лечении.
Что эти результаты могут значить для пациентов
Проще говоря, исследование создает раннюю «проводную диаграмму» того, как клетки рака эндометрия принимают решение — слушать прогестерон или нет. Результаты указывают, что резистентность — это не только потеря рецептора прогестерона, но и более глубокие изменения в обработке ДНК и РНК и в ключевых контрольных генах, таких как NNMT и SOX17. В будущем анализы крови или тканей, считывающие состояние этой генетической сети, могут помочь врачам предсказывать, кто выиграет от гормональной терапии с сохранением фертильности. Еще более перспективно, препараты, подавляющие гены резистентности или усиливающие гены чувствительности, возможно однажды будут комбинироваться с прогестероном, чтобы сделать этот щадящий вариант лечения эффективным для большего числа людей и на более длительный срок.
Цитирование: Li, X., Wang, S., Qiu, Z. et al. Construction and initial validation of key gene network for progesterone resistance in endometrial cancer based on genome-wide CRISPR screening. Sci Rep 16, 8030 (2026). https://doi.org/10.1038/s41598-026-36534-x
Ключевые слова: рак эндометрия, резистентность к прогестерону, CRISPR-скрининг, генетические сети, гормональная терапия