Clear Sky Science · ru
Модификации m6A хозяина формируют микробиоту, которая вызывает клеточно-специфичный ферроптоз как причинный путь к хроническим заболеваниям дыхательных путей
Почему ваши микробы важны для легких
Хронические проблемы с дыханием, такие как астма и хроническая обструктивная болезнь легких (ХОБЛ), обычно связывают с курением, загрязнением воздуха или аллергией. Это исследование указывает на другого, менее очевидного участника: триллионы микробов в нашем кишечнике и на коже. На основе крупномасштабных генетических данных авторы показывают, что некоторые микробы могут не просто сопутствовать заболеваниям легких, но и способствовать их развитию — через тонкие химические изменения в наших клетках и форму повреждения, зависящую от железа. Понимание этой скрытой сети может в перспективе привести к новым способам профилактики или лечения хронических заболеваний дыхательных путей, смещая микробиоту и её молекулярные пути в более здоровое состояние.
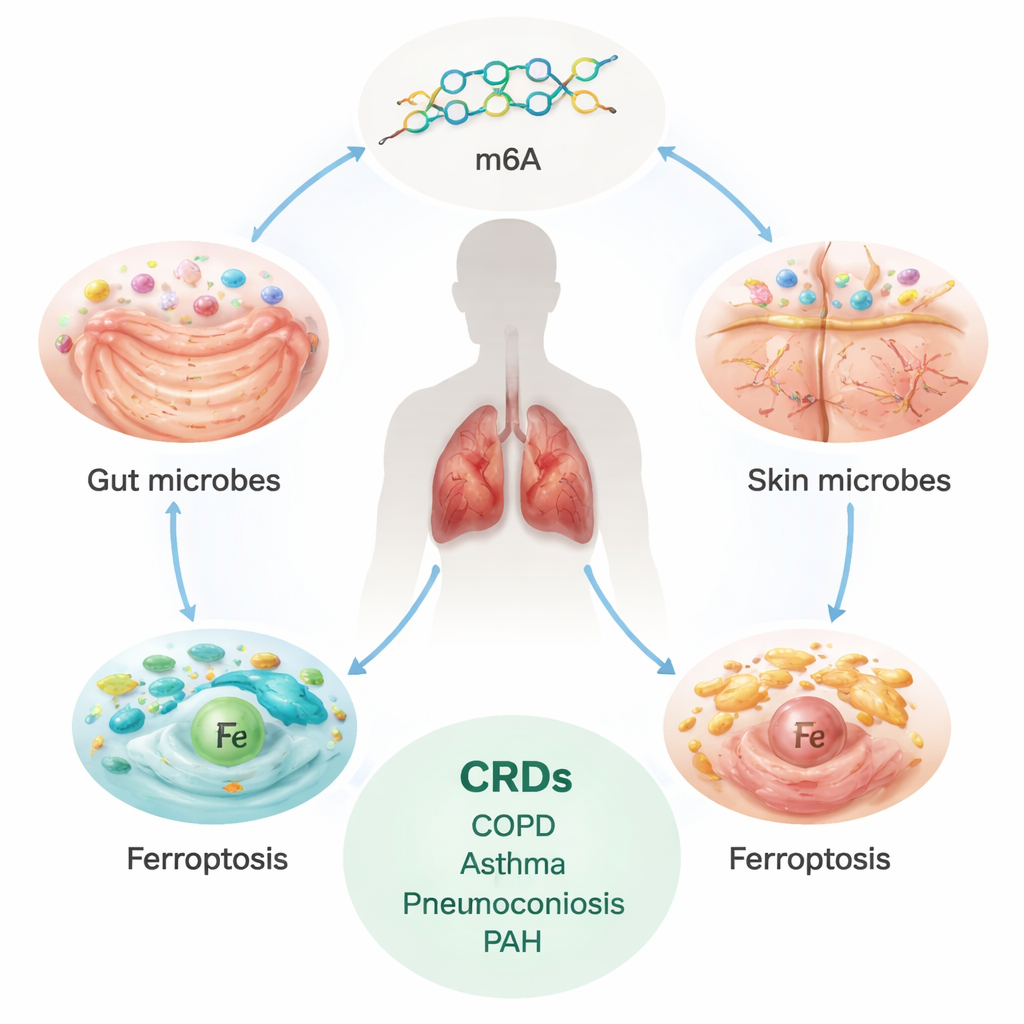
Скрытое бремя хронических заболеваний легких
Хронические заболевания дыхательных путей, включая ХОБЛ, астму, интерстициальные заболевания легких (ИЗЛ), пневмокониозы и лёгочную артериальную гипертензию (ЛАГ), затрагивают сотни миллионов людей во всём мире и ежегодно приводят к миллионам смертей. Эти состояния часто развиваются медленно, но неумолимо, вызывая рубцевание или перестройку легочной ткани и сосудов и приводя к одышке. Современные методы лечения в основном снимают симптомы; они не всегда полностью останавливают или обращают происходящее повреждение. Это побуждает учёных искать более глубокие, корневые причины, особенно те, которые можно изменить до развития тяжёлого заболевания.
Микробные соседи в кишечнике и на коже
Сегодня мы знаем, что кишечник и кожа населены сложными микробными сообществами, которые помогают формировать иммунную систему, влияют на метаболизм и поддерживают барьерные функции. Но действительно ли эти микробы запускают заболевания легких, или они просто меняются по мере прогрессирования болезни? Чтобы распутать причину и следствие, исследователи использовали метод, называемый менделевской рандомизацией, который использует естественные генетические различия между людьми как своего рода пожизненный «эксперимент». Они объединили генетические данные по сотням типов микробов кишечника и кожи с данными по пяти крупным хроническим заболеваниям легких из больших европейских исследований, проверяя, связаны ли наследуемые предрасположенности к более высоким или низким уровням конкретных микробов с риском каждого заболевания.
Микробы, которые помогают или вредят легким
Анализ выявил десятки кишечных микробов, которые либо повышали, либо снижали риск каждого респираторного заболевания, часто в специфичных для болезни паттернах. Например, некоторые виды кишечных бактерий, по-видимому, защищали от ХОБЛ, астмы или ЛАГ, в то время как другие повышали вероятность ИЗЛ или ХОБЛ. Микробы кожи показали более скромные, но всё ещё заметные связи — некоторые виды ассоциировались с повышенным риском, другие — с пониженным, в разных состояниях. Команда также поменяла направление анализа и обнаружила, что генетический риск ХОБЛ, астмы и других заболеваний легких, в свою очередь, предсказывал изменения в микробиоте кишечника и кожи. Эта двунаправленная связь указывает на петлю обратной связи: микробы могут формировать болезни легких, а болезни легких — перестраивать наши микробные экосистемы.
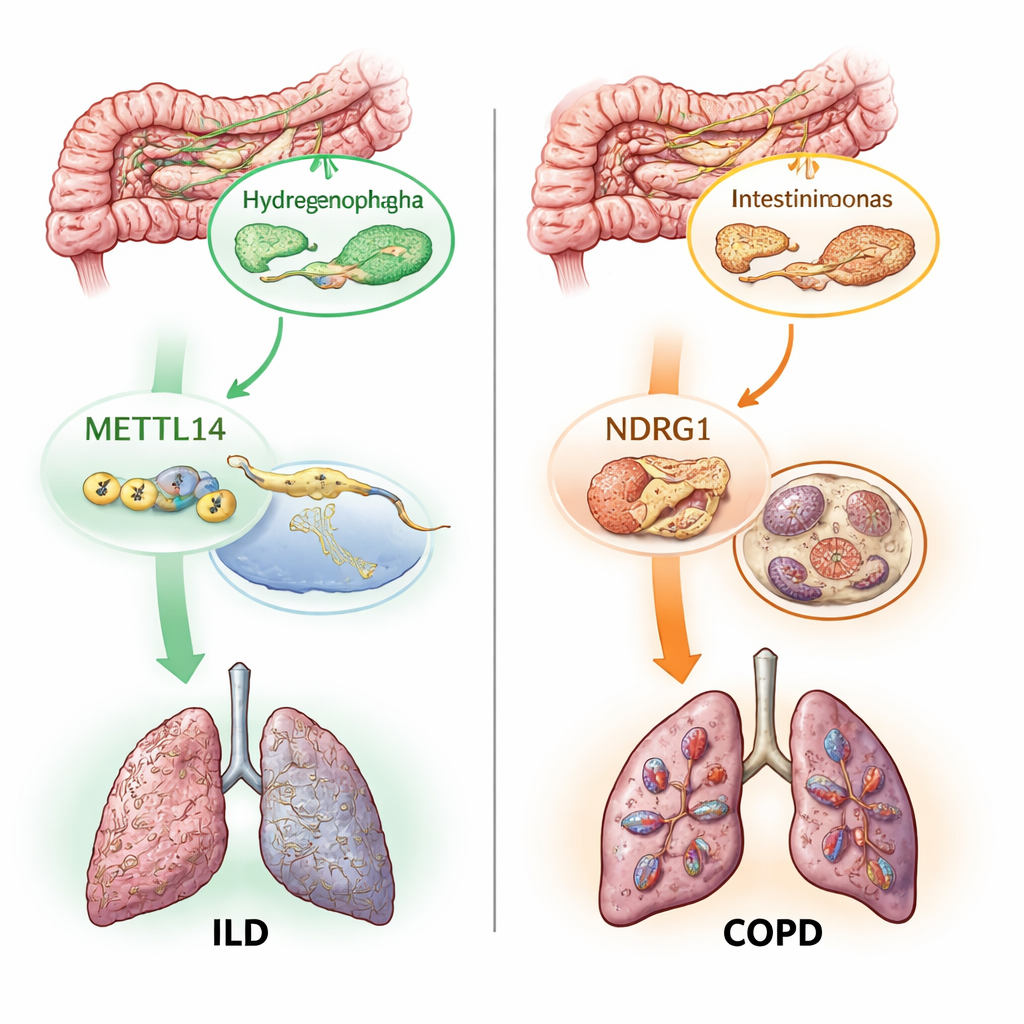
Два молекулярных переключателя: метки РНК и железозависимая смерть клеток
Помимо картирования важных микробов, авторы исследовали, как эти микро-партнёры могут повлиять на ткань легких. Они сосредоточились на двух молекулярных процессах, уже подозреваемых в причине повреждений легких. Первый, называемый модификацией m6A, — это небольшая химическая метка на РНК, которая настраивает, как включаются и выключаются гены. Второй, ферроптоз, — форма клеточной гибели, зависящая от железа и вызванная неконтролируемой окислительной деградацией липидов в мембранах. С помощью генетических прокси для 19 связанных с m6A генов и сотен генов, участвующих в ферроптозе, они проверили, являются ли изменения в этих путях причинно связанными с заболеваниями легких. Они обнаружили, что один ген-писатель m6A, METTL14, связан с пониженным риском ИЗЛ, а несколько генов ферроптоза, включая NDRG1, связаны с повышенным риском ХОБЛ, ИЗЛ и астмы.
Соединяя точки: от микробов к клеткам к болезни
Самое новое в этой работе — отслеживание того, как эти элементы объединяются в цепочки причин и следствий. Статистические медиативные анализы показали, что часть защитного эффекта METTL14 при ИЗЛ проходит через изменения, которые он вызывает в одном кишечном микроорганизме, названном Hydrogenophaga. В другом пути конкретная кишечная бактерия, Intestinimonas massiliensis, по-видимому, влияющая на риск ХОБЛ, частично действует через активацию NDRG1 и программы ферроптоза. Затем команда проверила данные по тканям человеческих легких и подтвердила, что и METTL14, и NDRG1 выражены по-разному в больных по сравнению со здоровыми образцами. Наконец, использовав одноклеточные генетические карты иммунных клеток, они локализовали вредный эффект NDRG1 на ХОБЛ до конкретного поднабора иммунных клеток — типа моноцитов, что указывает на необходимость клеточно-специфической направленной терапии для будущих препаратов против этого гена.
Что это значит для будущих методов лечения
Для неспециалистов основная мысль такова: здоровье легких зависит не только от того, что мы вдыхаем, но и от микробов, живущих в нас и на нас, и от тех молекулярных переключателей, которые они включают в наших клетках. Это исследование не может экспериментально доказать каждое звено цепи, и оно ограничено преимущественно людьми европейского происхождения, но даёт сильные генетические подсказки, что кишечные микробы, метки РНК вроде m6A и железозависимая клеточная смерть образуют связанную цепочку, ведущую к хроническому повреждению легких. В долгосрочной перспективе эта линия исследований может вдохновить новые стратегии, сочетающие микробиом-ориентированные терапии с препаратами, нацеленными на METTL14, NDRG1 или ферроптоз, с целью не просто облегчать симптомы, но и прерывать биологические цепи, заставляющие хронические заболевания дыхательных путей прогрессировать.
Цитирование: Zhang, J., Liu, X., Liu, X. et al. Host m6A modifications shape microbiota that drives cell specific ferroptosis as a causal pathway to chronic respiratory diseases. Sci Rep 16, 5809 (2026). https://doi.org/10.1038/s41598-026-36513-2
Ключевые слова: микробиом кишечника, хронические заболевания легких, астма и ХОБЛ, эпигенетика РНК, пути клеточной смерти