Clear Sky Science · ru
Фосфорилирование кортактина NEK7 модулирует миграционную способность клеток, экспрессирующих EML4-ALK V3
Почему движение клеток важно при раке легкого
Рак становится опасным для жизни, когда клетки учатся перемещаться. При немелкоклеточном раке легкого одни опухоли распространяются по организму быстрее других, и одним из виновников является дефектный белок‑фьюжн EML4-ALK. Его особая версия, известная как вариант 3 (V3), связана с особенно агрессивным течением заболевания и плохим ответом на таргетную терапию. В данном исследовании поставлен простой, но важный вопрос: что позволяет клеткам, движимым V3, так эффективно менять форму и передвигаться, и можно ли выделить молекулярные компоненты, обеспечивающие эту способность?
Гипермигрирующий вариант рака легкого
Врачи давно заметили, что лишь у небольшой доли раков легкого присутствует фьюжн EML4-ALK, но у пациентов с опухолями, экспрессирующими форму V3, прогноз обычно хуже, чем у тех, у кого другие варианты. Под микроскопом клетки с V3 выглядят иначе: вместо компактной брусчаточной формы они вытягиваются в длинные тонкие формы с удлинёнными выростами, напоминающими движущиеся клетки. Предыдущие работы показали, что такое поведение зависит от двух киназ, NEK9 и NEK7, которые действуют как молекулярные переключатели. Однако ключевые эффектыстримы этих переключателей — те, что непосредственно перестраивают внутриклеточный «скелет» — были плохо изучены.
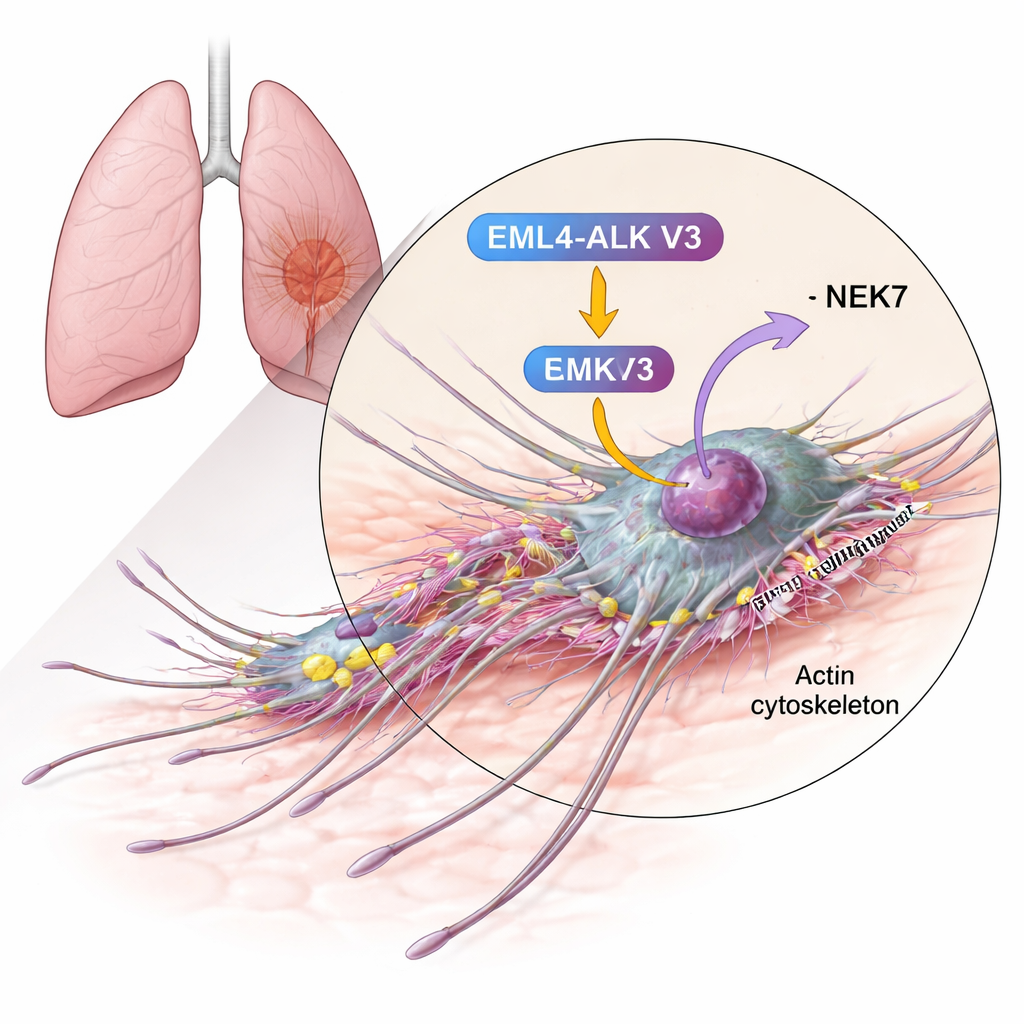
Связь белка движения с агрессивным фьюжном
Авторы сосредоточились на кортактине — белке, известном своей избытком во многих инвазивных опухолях и участвующем в построении сетей актиновых филаментов, которые выталкивают мембрану вперёд. С помощью биохимических тестов они показали, что кортактин может подвергаться химической модификации (фосфорилированию) под действием NEK6 и, ещё сильнее, NEK7. Эти киназы присоединяют фосфатные группы к специфическим сериновым остаткам в актин‑связывающем участке кортактина — как раз тому фрагменту, который захватывает актино‑филаменты и стабилизирует ветвящиеся сети. В присутствии NEK7 кортактин получал больше фосфатных групп и в большем числе позиций, чем при NEK6, что указывает на то, что NEK7 является основным регулятором в этом контексте.
Выключение кортактина останавливает миграцию раковых клеток
Чтобы понять роль кортактина в живых клетках, исследователи снизили его уровень с помощью РНК‑интерференции в клетках, запрограммированных на активацию NEK9 или NEK7, либо на экспрессию самого EML4-ALK V3. В всех трёх условиях характерные удлинённые мезенхимоподобные формы разрушались: клетки становились более плоскими и круглыми, теряли длинные выросты и вместо этого образовывали толстые прямые актиновые «стресс‑фибриллы», пересекающие клетку. Несколько тестов миграции — от закрытия искусственных «ран» в монолайне до слежения за отдельными клетками и измерения движения к химическому сигналу — показали, что при отсутствии кортактина эти высокомобильные клетки значительно замедлялись. Схожие эффекты наблюдались и в устойчивых клеточных линиях рака легкого, естественно несущих EML4-ALK V3, что подчёркивает клиническую значимость пути.
Тонкие филаменты и острые вершины на переднем крае
Высокорезолюционная микроскопия в бронхиальных эпителиальных клетках выявила ещё более детальную картину. Клетки, экспрессирующие EML4-ALK V3, формировали множество тонких, иногда ветвящихся выростов, напоминающих филоподии, покрывающих их протрузии. На кончиках и в местах ветвления этих структур собирались вместе кортактин, EML4-ALK V3, NEK7 и фосфорилированная форма кортактина. Такое тесное колокализование указывает на сфокусированную «стройплощадку», где NEK7 модифицирует кортактин для построения и поддержания тонких ветвящихся актиновых сетей, помогающих направлять клетку. При удалении кортактина эти сложные выросты исчезали, а инвазивный рост 3D‑сфероидов в окружающем геле значительно снижался.
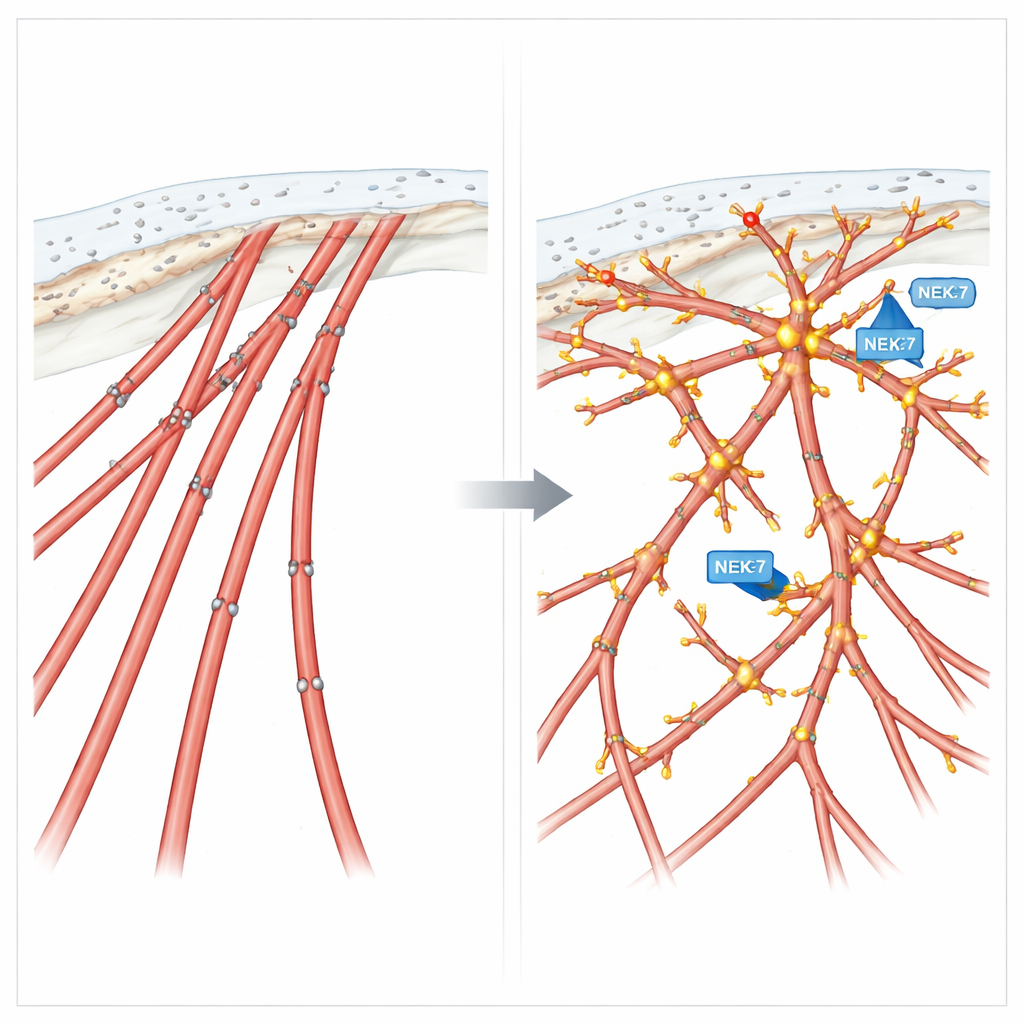
Фосфорилирование как регулятор миграции
Чтобы проверить, как эти химические метки на кортактине влияют на поведение, команда создала две «дизайнерские» версии белка: фосфомиметическую форму, имитирующую постоянное фосфорилирование в четырёх ключевых сайтах, и фосфонулевую форму, неспособную к фосфорилированию в этих местах. Клетки, экспрессирующие миметическую версию, развивали многочисленные филоподийоподобные выросты и демонстрировали усиленную направленную миграцию, подобно клеткам с активным NEK7 или EML4-ALK V3. Напротив, клетки с нефосфорилируемой версией формировали жёсткие стресс‑фибриллы, теряли тонкие выросты и передвигались быстро, но бессистемно — хорошо для блуждания, плохо для следования сигналу. В трёхмерных культурах такой фосфонулевой кортактин вызывал инвазивные отростки, которые были неорганизованы и не имели точной направленности.
Что это значит для понимания — и контроля — распространения
Проще говоря, исследование показывает, что агрессивный вариант рака легкого EML4-ALK V3 присваивает себе нормальную систему формирования клеточной формы. Активация NEK7 приводит к фосфорилированию кортактина в определённых позициях его актин‑связывающего домена. Эта модификация настраивает кортактин так, чтобы он мог строить тонко ветвящиеся актиновые структуры и филоподийоподобные выросты, обеспечивающие быструю направленную миграцию и инвазию. Нарушение кортактина или его фосфорилирования меняет ситуацию: клетки либо почти не двигаются, либо перемещаются хаотично без направленности. Эти данные выявляют конкретную молекулярную цепочку — от онкогенного фьюжна через NEK7 к кортактину и актиновому цитоскелету — которая помогает объяснить, почему некоторые раки легкого настолько эффективно метастазируют, и указывают на новые подходы, чтобы замедлить или исказить их движение.
Цитирование: Richardson, E.L., Knebel, A., Straatman, K.R. et al. NEK7 phosphorylation of cortactin modulates the migratory capacity of cells expressing EML4-ALK V3. Sci Rep 16, 6407 (2026). https://doi.org/10.1038/s41598-026-36484-4
Ключевые слова: немелкоклеточный рак легкого, EML4-ALK V3, миграция клеток, кортактин, актиновый цитоскелет