Clear Sky Science · ru
ATF4 регулирует дисфункцию митохондрий и митофагию, способствуя апоптозу роговичного эндотелия
Почему «окно» глаза может помутнеть
Наши роговицы — прозрачные передние «окна» глаз — сохраняют прозрачность благодаря тонкому, интенсивно работающему слою клеток на их внутренней поверхности. При эндотелиальной дистрофии роговицы Фукса (FECD) миллионы людей постепенно теряют эти клетки, что приводит к отёку, помутнению зрения и часто к трансплантации роговицы. В этом исследовании ставится базовый, но ключевой вопрос: что заставляет эти клетки принимать решение об уничтожении, и может ли выключение одного молекулярного «переключателя» помочь их сохранить?
Хрупкий клеточный слой, который сохраняет зрение
Эндотелий роговицы — это единый слой шестиугольных клеток, который постоянно выкачивает жидкость из роговицы, чтобы поддерживать её прозрачность. При FECD эти клетки испытывают стресс и постепенно исчезают, в то время как на базальной мембране накапливаются выпячивания аномального материала, называемые гуттае. Поскольку одобренных лекарств от FECD нет и основным лечением остаётся трансплантация роговицы, исследователи пытаются понять, как именно внутриклеточный стресс подталкивает эти клетки к гибели. Ранее отдельные работы указывали на напряжение в двух ключевых компартментах клетки — эндоплазматическом ретикулуме (фабрике сворачивания белков) и митохондриях (энергетических станциях) — но оставалось неясным, как эти два ответа на стресс взаимодействуют между собой.
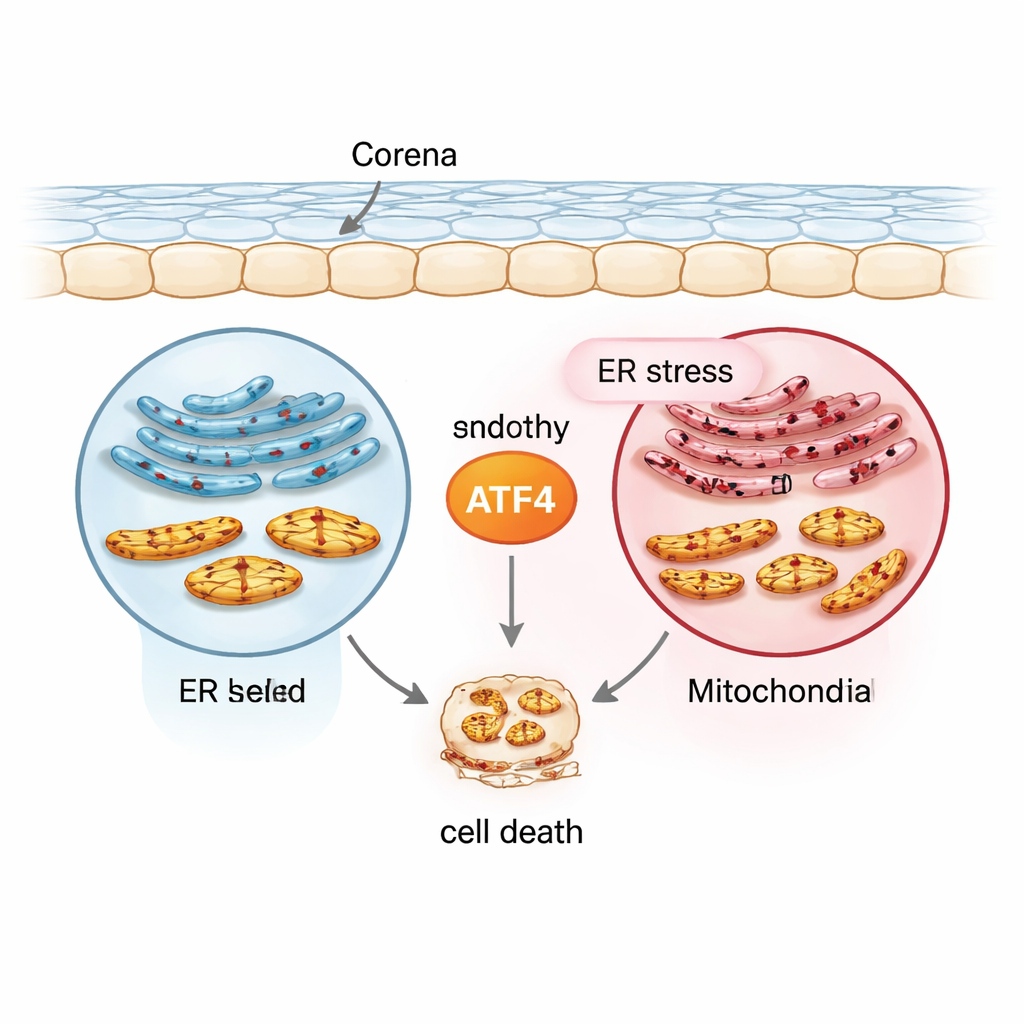
Мессенджер стресса в центре внимания: ATF4
Команда сосредоточилась на белке ATF4 — факторе транскрипции, который включает или выключает множество генов ответа на стресс. Используя нормальную линию человеческих эндотелиальных клеток роговицы (21T), клеточную линию, моделирующую FECD с расширением повтора TCF4 (F35T), первичные человеческие эндотелиальные клетки роговицы и мышиные модели, подвергнутые облучению ультрафиолетом A (UVA), они воссоздали разные состояния, имитирующие хронический стресс. Эндоплазматический ретикулум выводили на стресс с помощью препарата туникамицина и затем измеряли уровни ATF4 и других маркёров. По сравнению с нормальными клетками, клетки, подобные FECD, изначально имели повышенные уровни ATF4 и связанной с ним стресс‑протеомики, а при хроническом стрессе ATF4 возрастал ещё больше как в культивируемых клетках, так и в человеческих роговичных тканях. Такая картина поместила ATF4 на перекрёсток между ранними защитными ответами и поздними, самоуничтожающими сигналами.
От сбоя питания к программной смерти
Далее исследователи изучали, как этот стресс влияет на митохондрии. В клетках, моделирующих FECD, митохондрии вырабатывали меньше АТФ, теряли электрический мембранный потенциал и распадались с длинных сетевидных форм на множество мелких фрагментов. Эти изменения усугублялись при продолжительном стрессе эндоплазматического ретикулума. В то же время классические белки апоптоза — такие как активированные каспазы и белок восстановления ДНК PARP в своём расщеплённом, про‑смертном виде — становились более многочисленными, тогда как защитные белки, например Bcl‑2, снижались. В совокупности эти изменения указывают на то, что при FECD стрессированные клетки эндотелия роговицы смещаются в сторону митохондриально‑опосредованного апоптоза — аккуратной, но необратимой формы программируемой самоубийственной гибели.
Система уборки буксует при хроническом стрессе
Обычно сильно повреждённые митохондрии удаляются посредством рециклинга, называемого митофагией: их помечают и упаковывают в небольшие везикулы для утилизации. Команда обнаружила, что ранние «стартерные» молекулы митофагии (Parkin и LC3) активировались как в нормальных, так и в FECD‑подобных клетках, особенно после стресса. Но ключевые белки‑поддержки были снижены, а электронная микроскопия показала накопление частично переваренных митохондрий, застрявших в везикулах. Это указывало на то, что хотя процесс уборки запускался, он не завершался, оставляя клетки переполненными дефектными «энергетическими станциями», которые ещё больше подпитывают стресс и гибель вместо восстановления.
Выключение ATF4, чтобы спасти клетки
Чтобы проверить, ведёт ли ATF4 этот обвальный процесс, исследователи применили малые интерферирующие РНК для частичного подавления ATF4 в культивируемых эндотелиальных клетках роговицы. При том же хроническом стрессе клетки с пониженным ATF4 демонстрировали более низкие уровни белков, способствующих гибели, более здоровый митохондриальный мембранный потенциал, меньше фрагментации и лучшую выживаемость в тестах жизнеспособности. Важно, что число застрявших структур митофагии уменьшилось, что предполагает, что снижение ATF4 помогло восстановить более эффективный баланс между повреждением и уборкой. У мышей, генетически имеющих только одну рабочую копию гена ATF4, облучение UVA вызывало меньшую активацию про‑смертного партнёра CHOP и сохраняло более нормальную форму эндотелиальных клеток по сравнению с мышами с полным набором ATF4.
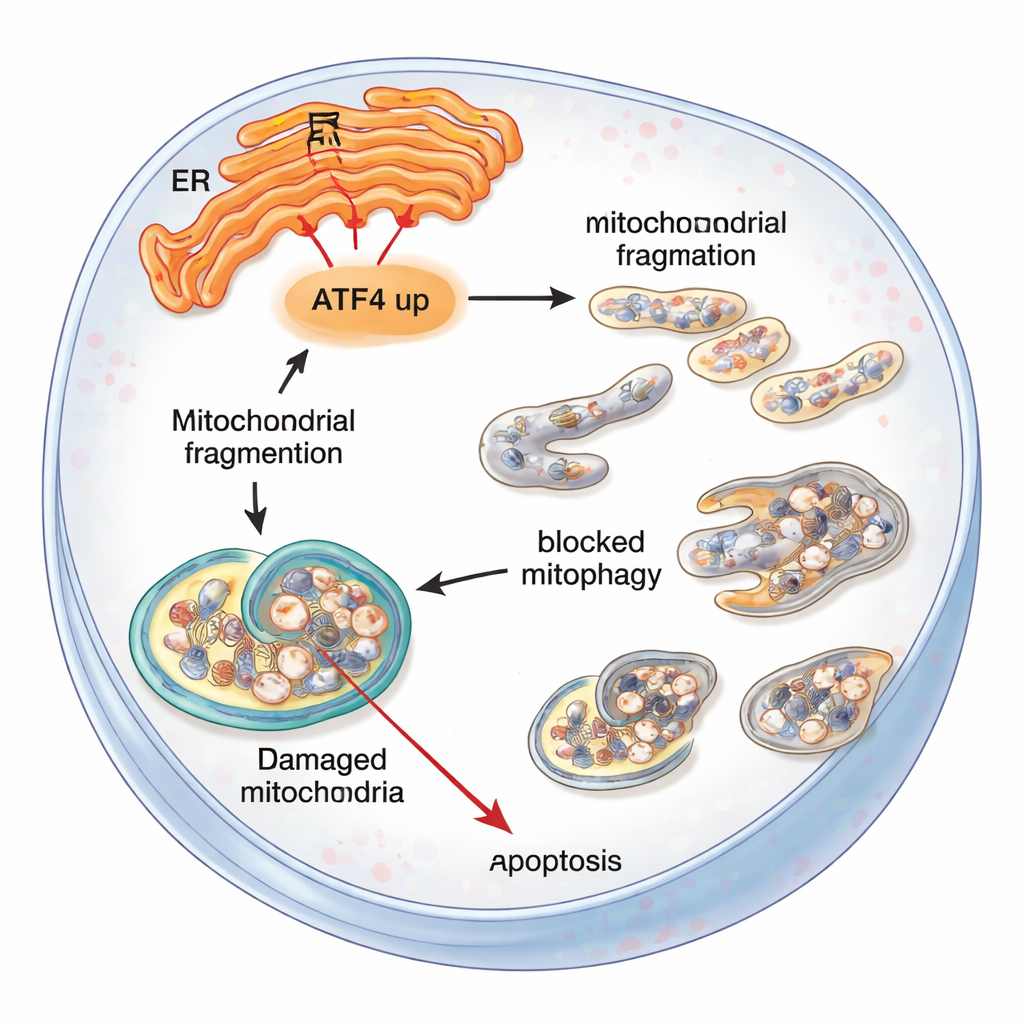
Что это означает для людей с FECD
Для неспециалистов основной вывод такой: один мессенджер стресса — ATF4 — может сдвинуть эндотелиальные клетки роговицы от приспособления к коллапсу. При длительном стрессе эндоплазматического ретикулума ATF4 способствует нарушению работы митохондрий, тормозит систему утилизации и в конечном счёте стимулирует эти жизненно важные клетки к самоуничтожению. Ослабление активности ATF4 — генетически в мышах или с помощью целевых молекулярных инструментов в клетках — защищает митохондрии, улучшает удаление повреждённого материала и сохраняет больше клеток живыми. Хотя эти результаты пока ограничиваются лабораторными и животными моделями, они выделяют ATF4 и связанные с ним стресс‑пути как перспективные лекарственные мишени, которые однажды могут замедлить или предотвратить прогрессирование дистрофии Фукса и снизить потребность в пересадке роговицы.
Цитирование: Qureshi, S., Kim, S.Y., Lee, S. et al. ATF4 regulates mitochondrial dysfunction and mitophagy, contributing to corneal endothelial apoptosis. Sci Rep 16, 5960 (2026). https://doi.org/10.1038/s41598-026-36453-x
Ключевые слова: Эндотелиальная дистрофия роговицы Фукса, эндотелий роговицы, митохондриальный стресс, митофагия, ATF4