Clear Sky Science · ru
Интегративный подход к выявлению новых сетей взаимодействия миРНК–мРНК при кардиомиопатии, связанной с LMNA
Почему важны крошечные регуляторы сердца
Дилатационная кардиомиопатия — серьёзное состояние, при котором сердце увеличивается и слабеет, что часто приводит к сердечной недостаточности, опасным нарушениям ритма и даже внезапной смерти. У многих семей это заболевание наследственное, и изменения в гене LMNA нередко оказываются причиной. В этом исследовании поставлен по виду простой, но важный вопрос: при повреждении сердца мутациями LMNA какие гены включаются или выключаются и какие крошечные молекулы РНК управляют этими переключателями? Точное картирование этих молекулярных «разговоров» указывает на новые пути для прогнозирования, наблюдения и, возможно, в будущем лечения этой агрессивной формы сердечного заболевания.
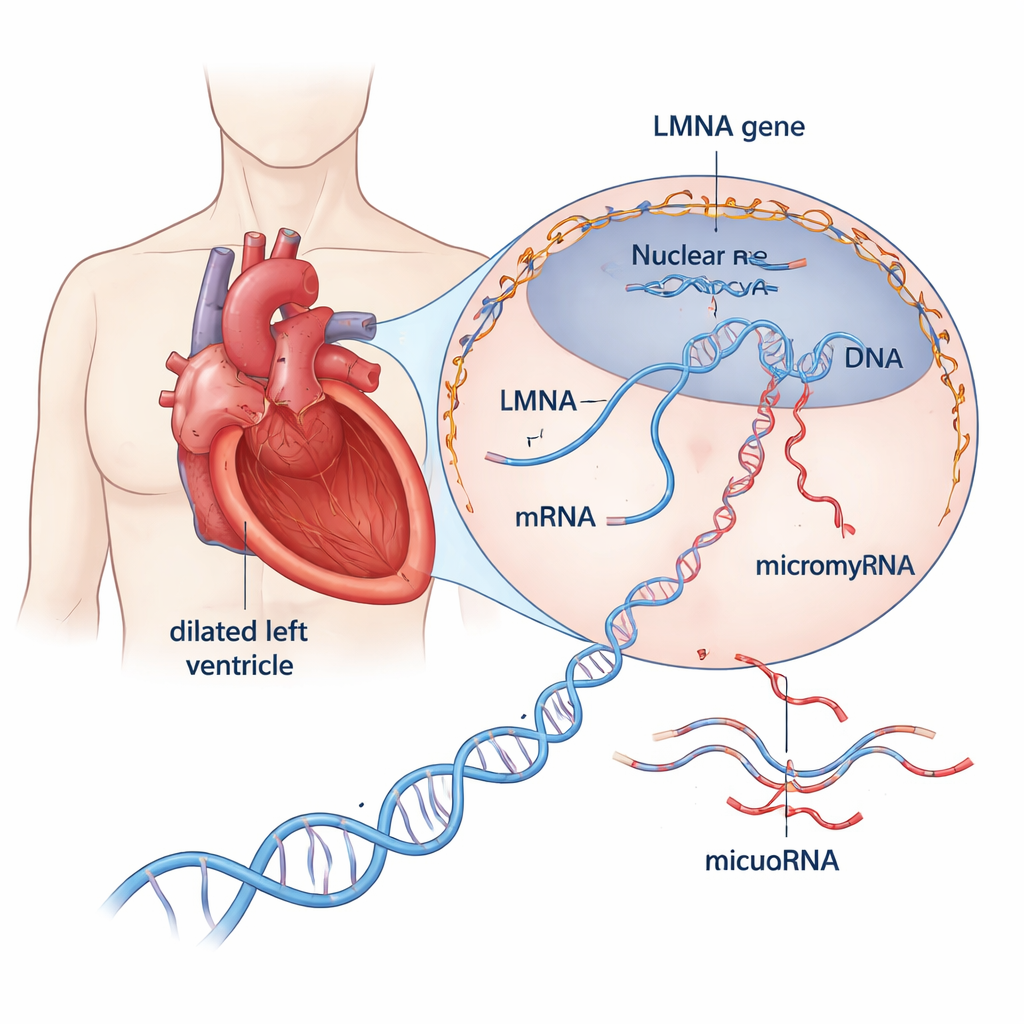
Более пристальный взгляд на опасное сердечное заболевание
Дилатационная кардиомиопатия растягивает и истончает главный насосный отдел сердца, ослабляя его способность выталкивать кровь по телу. Примерно от трети до половины случаев, ранее считавшихся «идиопатическими», теперь имеют генетическую природу. Среди более чем 30 вовлечённых генов особенно выделяется LMNA: вредоносные варианты этого гена составляют около 10% наследственных случаев и связаны с быстрым прогрессированием заболевания, ранними нарушениями ритма и высоким риском внезапной сердечной смерти. Белки, кодируемые LMNA, образуют структурный каркас вокруг ДНК клетки, поддерживают форму ядра и влияют на активность генов. Тем не менее механизмы, с помощью которых дефектные белки LMNA ведут сердце к недостаточности, остаются слабо понятными.
Отслеживая сообщения внутри сердца мыши
Для изучения этого вопросы исследователи использовали модель мыши с известной мутацией LMNA (R249W), у которой развивается форма дилатационной кардиомиопатии, сходная с человеческим заболеванием. В возрасте 50 недель — когда у мышей наблюдаются увеличенные желудочки, сниженная сократительная функция и фибротические рубцы — команда взяла ткани сердца и исследовала два типа РНК: матричную РНК (мРНК), которая несёт инструкции для синтеза белков, и микроРНК (миРНК), короткие некодирующие цепочки, которые тонко настраивают активность генов, блокируя или разрушая определённые мРНК. С помощью высокопроизводительного секвенирования и строгих статистических фильтров они выявили 2148 генов с изменённой активностью в мутантных сердцах и 53 миРНК, уровни которых были повышены или понижены по сравнению со здоровыми мышами.
Что меняется внутри больных сердечных клеток
При группировке изменённых генов по биологическим путям выявились несколько ключевых тем. Многие модифицированные гены были связаны с сокращением сердечной мышцы, межклеточными прикреплениями и взаимодействием с внеклеточным матриксом, проведением электрических сигналов по сердцу и обменом липидов для генерации энергии. Эти результаты хорошо согласуются с клинической картиной связанной с LMNA болезни: жёсткая, фиброзная ткань; нарушение электрической проводимости, благоприятствующее аритмиям; и ухудшение энергетического баланса. Анализы путей с использованием общепризнанных баз данных подтвердили обогащение по ремоделированию внеклеточного матрикса, потенциалозависимым ионным каналам, синапсоподобной коммуникации в сердце и метаболизму жирных кислот — что указывает на то, что мутация LMNA разрушает несколько взаимосвязанных систем, а не один отдельный звеньевый дефект.
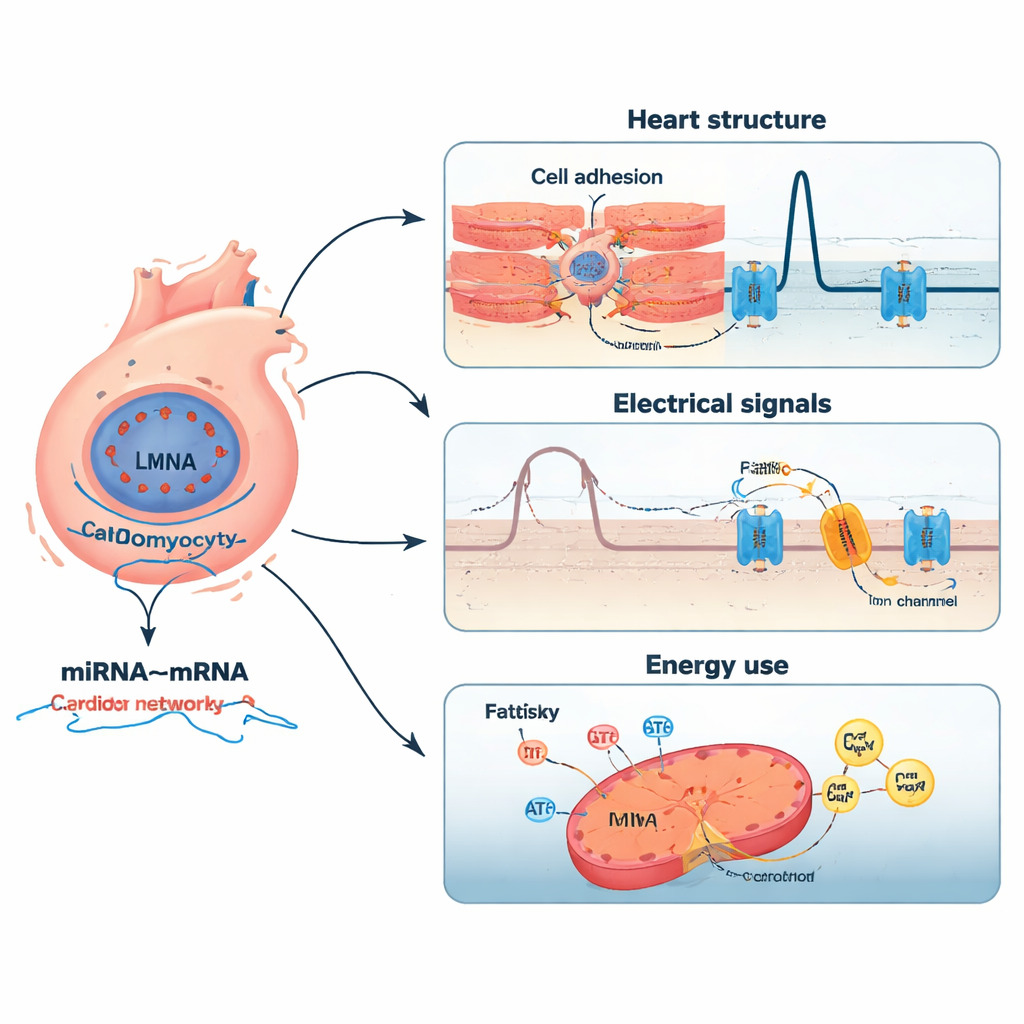
Сети крошечных переключателей и их мишеней
Исследование пошло дальше и сопоставило миРНК с их вероятными мРНК-мишенями. Используя корреляционный анализ и сверку с крупными базами экспериментально подтверждённых взаимодействий, авторы собрали сеть высокого доверия из 2197 пар миРНК–мРНК, включающую 12 ключевых миРНК. Некоторые миРНК были более активны и, по-видимому, подавляли гены, важные для развития сердца, управления кальцием и ответа на окислительный стресс. Другие были менее активны, возможно, снимая тормоза с генов, вовлечённых в клеточную адгезию, воспаление и ремоделирование структурного каркаса сердца. Например, одна миРНК (miR-183-5p) связывалась с рецептором в пути Wnt, который влияет на межклеточную коммуникацию, в то время как другая (miR-3473a) была связана с каналом высвобождения кальция, центральным для ритма сердца. В совокупности эти сети показывают, как тонкие сдвиги в крошечных РНК-регуляторах могут усиливать влияние мутации LMNA.
От молекулярных карт к будущим терапиям
Для неспециалистов итог таков: это исследование предлагает подробную карту того, как мутация LMNA перестраивает внутреннюю «проводку» сердца на уровне регуляции генов. Вместо одного «плохого гена» болезнь представляет собой каскад изменённых сообщений — многие из которых координируются миРНК — влияющих на структуру сердца, электрическую стабильность и энергетический обмен. Хотя работа выполнена на мышах и в значительной степени опирается на вычислительные анализы, она выделяет конкретные пары миРНК–ген как перспективные кандидаты для будущих биомаркеров в крови или для целевых терапий. В долгосрочной перспективе тонкая настройка этих крошечных РНК-переключателей может помочь врачам лучше прогнозировать наивысший риск, точнее отслеживать прогрессирование болезни и разрабатывать более персонализированные методы лечения для семей, затронутых кардиомиопатией, связанной с LMNA.
Цитирование: Córdoba-Caballero, J., Martínez, F.B., Campuzano, O. et al. An integrative approach to identify novel miRNA-mRNA interaction networks in LMNA-cardiomyopathy. Sci Rep 16, 6110 (2026). https://doi.org/10.1038/s41598-026-36439-9
Ключевые слова: дилатационная кардиомиопатия, ген LMNA, микроРНК, регуляция генов, сердечная недостаточность