Clear Sky Science · ru
От in-silico QSAR‑моделирования до in‑vitro MTT‑анализа: экспериментальная валидация новых лидов по uPAR для трёхлонно‑негативного рака молочной железы (TNBC) и рака кожи
Почему это исследование важно
Онкологические заболевания, такие как трёхлонно‑негативный рак молочной железы и некоторые формы рака кожи, особенно трудно лечить: они быстро распространяются и часто устойчивы к стандартной терапии. В этом исследовании изучается перспективная новая мишень на поверхности раковых клеток — uPAR — и показано, как сочетание компьютерного дизайна лекарств и лабораторных экспериментов может выявить кандидатов в препараты, которые способны замедлить или остановить распространение этих агрессивных опухолей.
Дверь, которая помогает раку распространяться
Чтобы опухоль стала смертельной, её клетки должны отделиться от первичного очага, прорвать окружающую ткань, попасть в кровоток и колонизировать отдалённые органы. uPAR играет ключевую роль в этом процессе. Он находится на поверхности раковой клетки и в сотрудничестве с партнёрными белками активирует ферменты, разрушающие внеклеточный матрикс, что облегчает движение и инвазию клеток. Уровни uPAR особенно высоки при трёхлонно‑негативном раке молочной железы и при некоторых раках кожи, а его избыточное выражение связано с более быстрым ростом, повышенной инвазией и худшим прогнозом для пациентов. По этой причине uPAR представляет собой привлекательную, но пока недостаточно используемую мишень для противораковых препаратов.
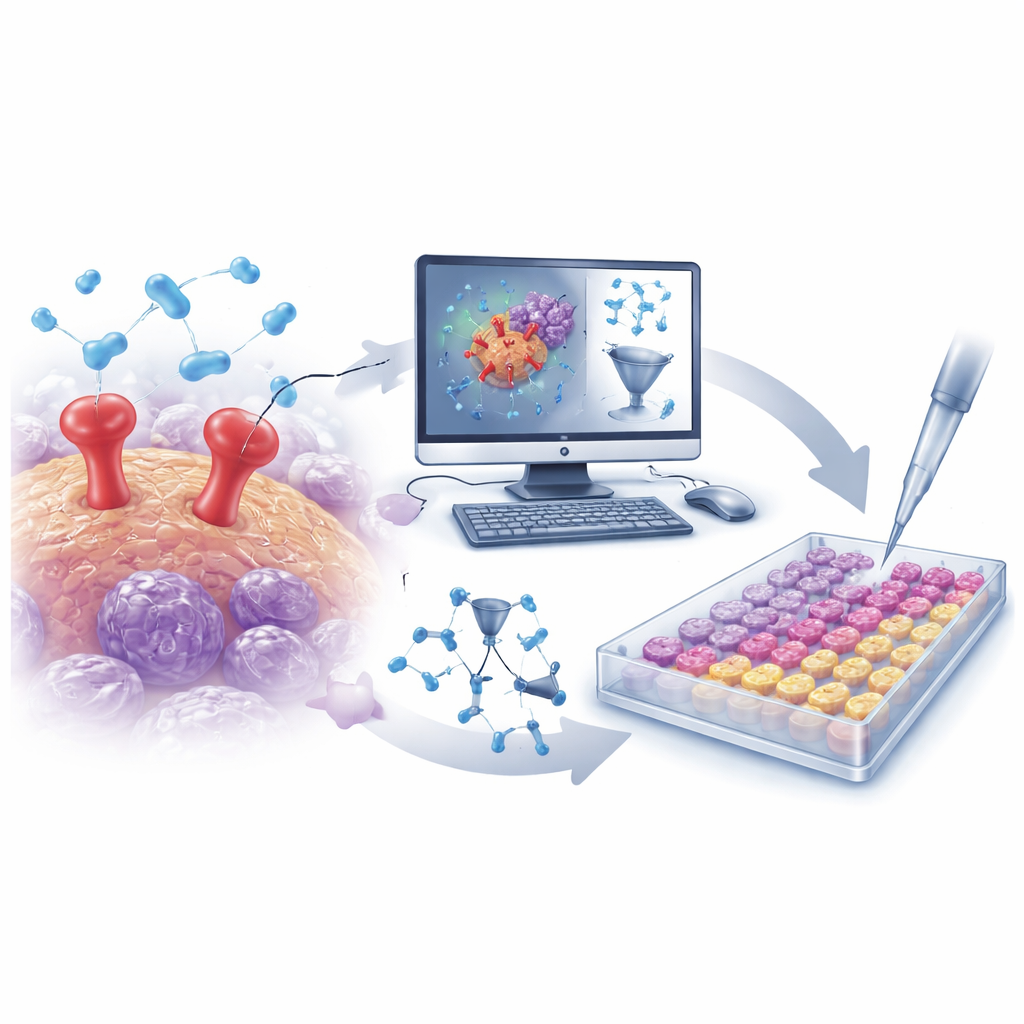
Добыча больших химических данных умными алгоритмами
Исследователи начали с формирования большой коллекции — более 500 известных молекул‑ингибиторов uPAR из публичной базы данных. Структуры каждой молекулы были преобразованы в тысячи числовых дескрипторов, отражающих такие характеристики, как размер, форма, распределение заряда и гибкость. На основе этих данных команда построила модель количественной структуры‑активности (QSAR) — математический инструмент, который учится распознавать структурные признаки, делающие молекулу более сильным ингибитором uPAR. После тщательной валидации для предотвращения переобучения модель показала высокую предсказательную способность на неизвестных соединениях и выделила несколько ключевых признаков, усиливающих или ослабляющих блокирование uPAR. Эти выводы направили поиск новых, лучше сконструированных молекул.
От виртуального скрининга к реальным пробиркам
Вооружившись обученной QSAR‑моделью, команда провела виртуальный скрининг сосредоточенной библиотеки примерно из 30 000 молекул, нацеленных на протеазы. Модель быстро сузила этот огромный пул до небольшого набора потенциальных ингибиторов uPAR. Параллельно проводили компьютерное докирование, чтобы оценить, насколько хорошо каждый кандидат вписывается в сайт связывания uPAR, а молекулярно‑динамические симуляции проверяли, будут ли эти комплексы стабильны с течением времени. Из этой комбинированной in‑silico‑кампании выделились два ярких кандидата: D685‑0061, отмеченный QSAR‑моделью как высокоактивный, и C878‑1660, отмеченный докированием и симуляциями как образующий особенно стабильные взаимодействия с uPAR.
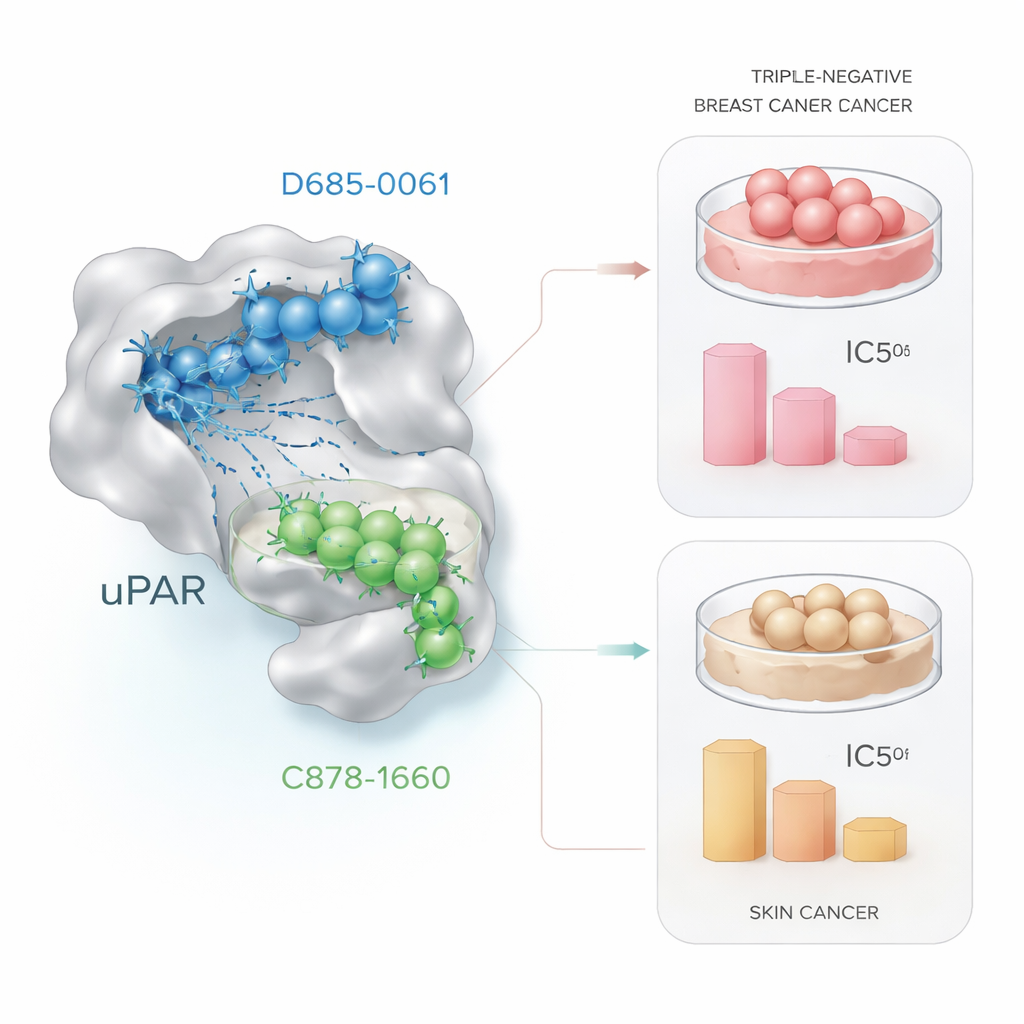
Испытание кандидатов на раковых клетках
Компьютерные предсказания имеют значение только если они сопровождаются реальными биологическими эффектами. Чтобы проверить это, исследователи облучали живые раковые клетки возрастающими дозами двух лид‑молекул и измеряли выживаемость клеток с помощью стандартного лабораторного метода — MTT‑анализа. В клетках трёхлонно‑негативного рака молочной железы (MDA‑MB‑231) D685‑0061 убивал клетки эффективнее, снижая жизнеспособность наполовину при примерно 21 микромоле, тогда как C878‑1660 требовал примерно в четыре раза большей концентрации. В микроскопе клетки, обработанные D685‑0061, демонстрировали явные признаки программируемой гибели: округление, отслоение от поверхности и фрагментацию. Напротив, в клетках рака кожи (A431) сильнейшим оказался C878‑1660 — он вызывал 50% гибели при примерно 19 микромолях по сравнению с примерно 28 микромолями для D685‑0061, также с заметными дозозависимыми повреждениями.
Что это значит для будущих методов лечения рака
Эта работа не даёт немедленного нового лекарства, но предоставляет два перспективных отправных пункта и, не менее важно, мощный план действий для дальнейших поисков. Связывая модели на больших данных, 3D‑симуляции и тщательные клеточные эксперименты, исследование демонстрирует, что uPAR можно селективно таргетировать малыми молекулами, которые повреждают агрессивные клетки рака молочной железы и кожи. D685‑0061 и C878‑1660 теперь служат лид‑соединениями, которые химики могут оптимизировать для повышения активности, улучшения безопасности и фармакокинетики. В долгосрочной перспективе препараты, созданные по этой схеме, могут помочь блокировать распространение опухолей, управляемых uPAR, превращая некоторые из сегодняшних самых опасных опухолей в более контролируемые заболевания.
Цитирование: Badukle, H., Jawarkar, R.D., Shah, U. et al. From in-silico QSAR modeling to in-vitro MTT assay: experimental validation of novel uPAR leads for triple-negative breast cancer (TNBC) and skin cancer. Sci Rep 16, 5786 (2026). https://doi.org/10.1038/s41598-026-36406-4
Ключевые слова: ингибиторы uPAR, трёхлонно‑негативный рак молочной железы, рак кожи, компьютерная разработка лекарств, MTT‑тест жизнеспособности клеток