Clear Sky Science · ru
Исследование в рамках теории функционала плотности адсорбции циклофосфамида и пуринетола на ковалентной триазиновой структуре (CTF-2) для применения в доставке лекарств
Почему умная химиотерапия важна
Препараты химиотерапии спасают жизни, но часто действуют скорее как прожектор, чем как точечный луч — поражая здоровые клетки наряду с раковыми. Это может приводить к серьёзным побочным эффектам: от утомляемости и инфекций до повреждения органов. В рассматриваемом исследовании изучают ультратонкий, высокопористый материал, называемый ковалентной триазиновой структурой (CTF-2), как «умную губку», способную безопаснее и эффективнее переносить два давно применяемых противораковых препарата — циклофосфамид и пуринетол — до нужных участков и затем освобождать их в условиях, подобным опухолевым.
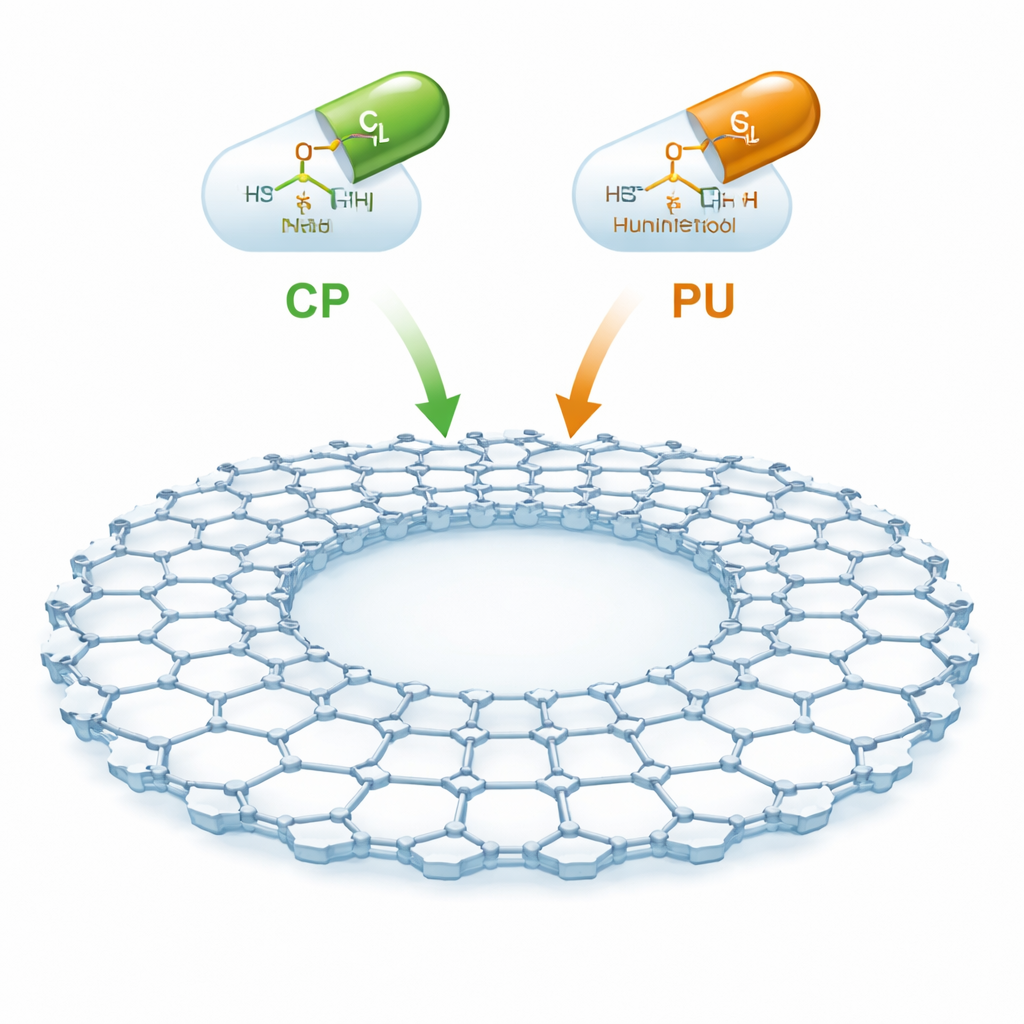
Новый тип молекулярной губки
CTF-2 — это искусственный материал, построенный из колец углерода и азота, связанных в плоскую, листоподобную сеть с большой центральной полостью и множеством свободного пространства. Благодаря своей тонкости, прочности и пористости он обеспечивает огромную внутреннюю поверхность для улавливания молекул лекарств. Авторы сосредоточились на двух важных противораковых препаратах: циклофосфамиде, широко применяемом при онкогематологических заболеваниях и солидных опухолях, и пуринетоле (также называемом меркаптопурином), используемом при лейкемиях и некоторых воспалительных заболеваниях кишечника. Идея состоит в том, чтобы аккуратно «сажать» эти препараты на поверхность CTF-2, чтобы их можно было переносить по кровотоку и освобождать более селективно, снижая вред для здоровых тканей.
Исследование невидимого с помощью компьютерных экспериментов
Вместо работы в мокрой лаборатории команда использовала продвинутые квантово‑уровневые вычисления (теория функционала плотности и родственные методы), чтобы выяснить, насколько прочно каждое лекарство прикрепляется к CTF-2 и что удерживает комплексы вместе. Они оптимизировали геометрии CTF-2 в сочетании с каждым препаратом, измерили расстояния между касающимися атомами и вычислили энергию, выигрываемую при адсорбции препарата на каркасе. Для циклофосфамида рассчитанная энергия адсорбции составила примерно −1,04 электронвольта, что чуть сильнее, чем −0,82 эВ для пуринетола. Эти значения, остающиеся явно благоприятными даже после коррекций технических артефактов и моделирования воды как растворителя, указывают на то, что оба препарата связываются достаточно прочно для загрузки, но не настолько сильно, чтобы их было невозможно затем высвободить.
Мягкие силы, выполняющие важную работу
Исследование показывает, что «клей» между препаратами и CTF-2 — не жёсткая ковалентная связь, а сеть мягких, нековалентных взаимодействий. Используя специализированные анализы плотности электронов — по сути карты распределения общих электронов — исследователи обнаружили, что доминируют ван-дер-ваальсовы притяжения (те же слабые силы, которые позволяют гекконам цепляться за стены) и слабые электростатические взаимодействия. Эти взаимодействия происходят на коротких, но нековалентных расстояниях между атомами водорода, азота, кислорода, серы и углерода в препаратах и на каркасе. Дополнительные расчёты, разделяющие общее притяжение на разные компоненты, подтвердили, что основную стабилизирующую роль играют электростатические и дисперсионные (ван-дер-ваальсовы) силы, тогда как отталкивающие взаимодействия предотвращают слишком глубокое «погружение» препарата или необратимое связывание.
Признаки стабильной загрузки и регулируемого высвобождения
Команда также изучила, как перераспределяются электроны при размещении препаратов на CTF-2 и как это меняет основные электрические свойства. Они наблюдали небольшие, но отчётливые переносы заряда между каждым препаратом и каркасом и незначительное сужение энергетического зазора между заполненными и пустыми электронными уровнями. Это указывает на то, что реакционная способность и проводимость материала слегка меняются при загрузке — полезное свойство для будущих приложений в сенсинге или тераностике. Крайне важно то, что при имитации более кислой среды, характерной для областей вокруг опухолей (добавлением дополнительных протонов), расчётное связывание ослабевало, а контактные расстояния увеличивались. Проще говоря, симуляции предполагают, что CTF-2 способен удерживать препараты при обычных, подобным крови условиях, но легче отпускать их в опухолевой, более кислой среде — именно такое поведение желанно для целевой доставки.
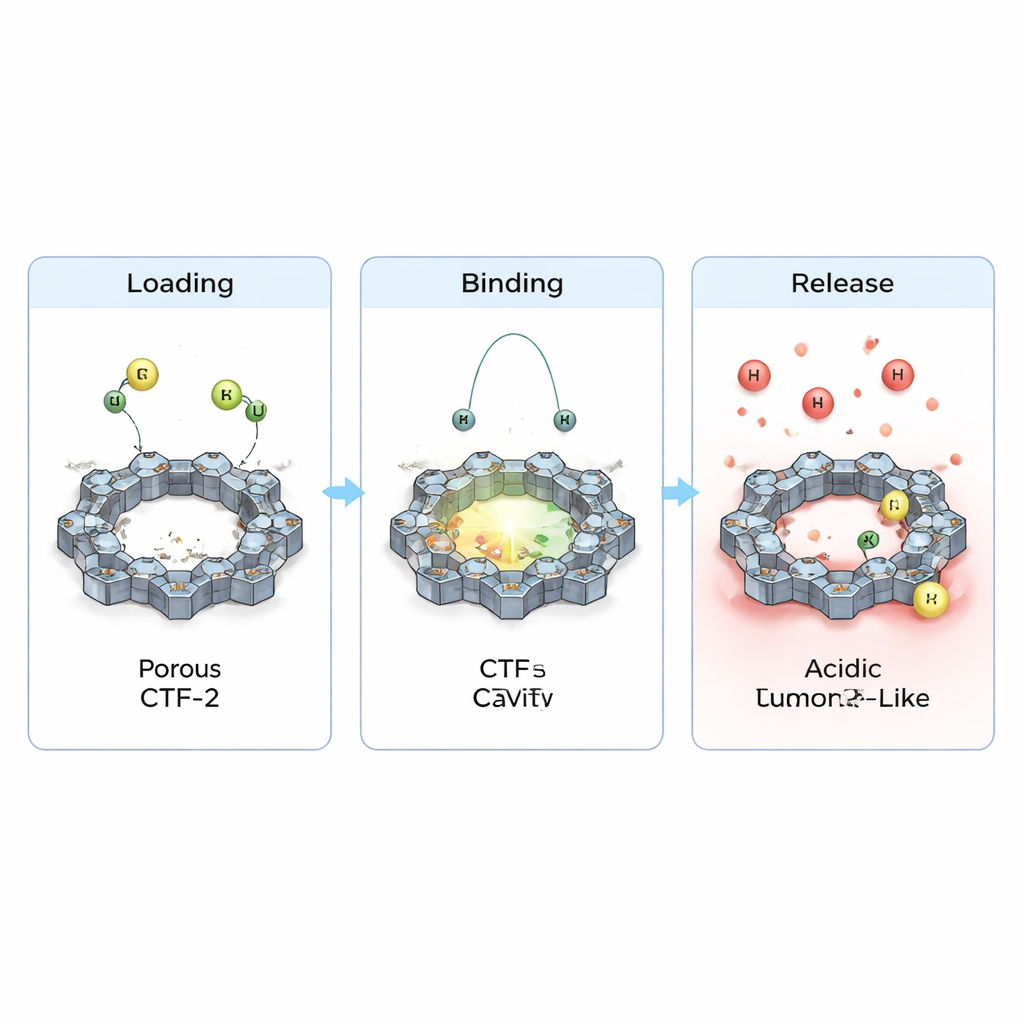
Что это означает для будущих методов лечения рака
В сумме эти расчёты рисуют CTF-2 как перспективный носитель для циклофосфамида и пуринетола: он может стабильно размещать их на своей пористой поверхности, защищать во время циркуляции и затем высвобождать при изменении локальной химии вокруг опухоли. Хотя работа теоретическая и требует экспериментальной проверки, она указывает на то, что тонко спроектированные, богатые азотом каркасы вроде CTF-2 могут помочь превратить старые, но эффективные химиотерапевтические препараты в более умные лекарства — доставляя мощные дозы туда, где они наиболее нужны, и снижая побочный ущерб здоровым клеткам.
Цитирование: Tariq, T., Yar, M., Bayach, I. et al. A density functional theory study of cyclophosphamide and purinethol adsorption on a covalent triazine framework (CTF-2) for drug delivery applications. Sci Rep 16, 6125 (2026). https://doi.org/10.1038/s41598-026-36405-5
Ключевые слова: нанокарриер, доставка лекарств, химиотерапия рака, ковалентная триазиновая структура, компьютерное моделирование