Clear Sky Science · ru
Интерактивная каскадная система глубокого обучения с доработкой эксперта для точной сегментации подрегионов стриатума
Почему важно картировать крошечные участки мозга
Стриатум, небольшая структура, скрытая глубоко в мозге, играет центральную роль в движении и мотивации и сильно поражается при таких заболеваниях, как болезнь Паркинсона. Врачи часто используют ПЭТ‑ и МР‑сканирование для измерения химических изменений в этой области, но стриатум разделён на множество мелких подрегионов, которые трудно увидеть и точно очертить. В этой статье предложен новый компьютерно‑ассистированный метод под названием StriaSeg‑iARM, который помогает специалистам проводить такую разметку точнее и эффективнее, даже у пациентов с изменённой структурой мозга из‑за старения или болезни.
Клиническая проблема на виду
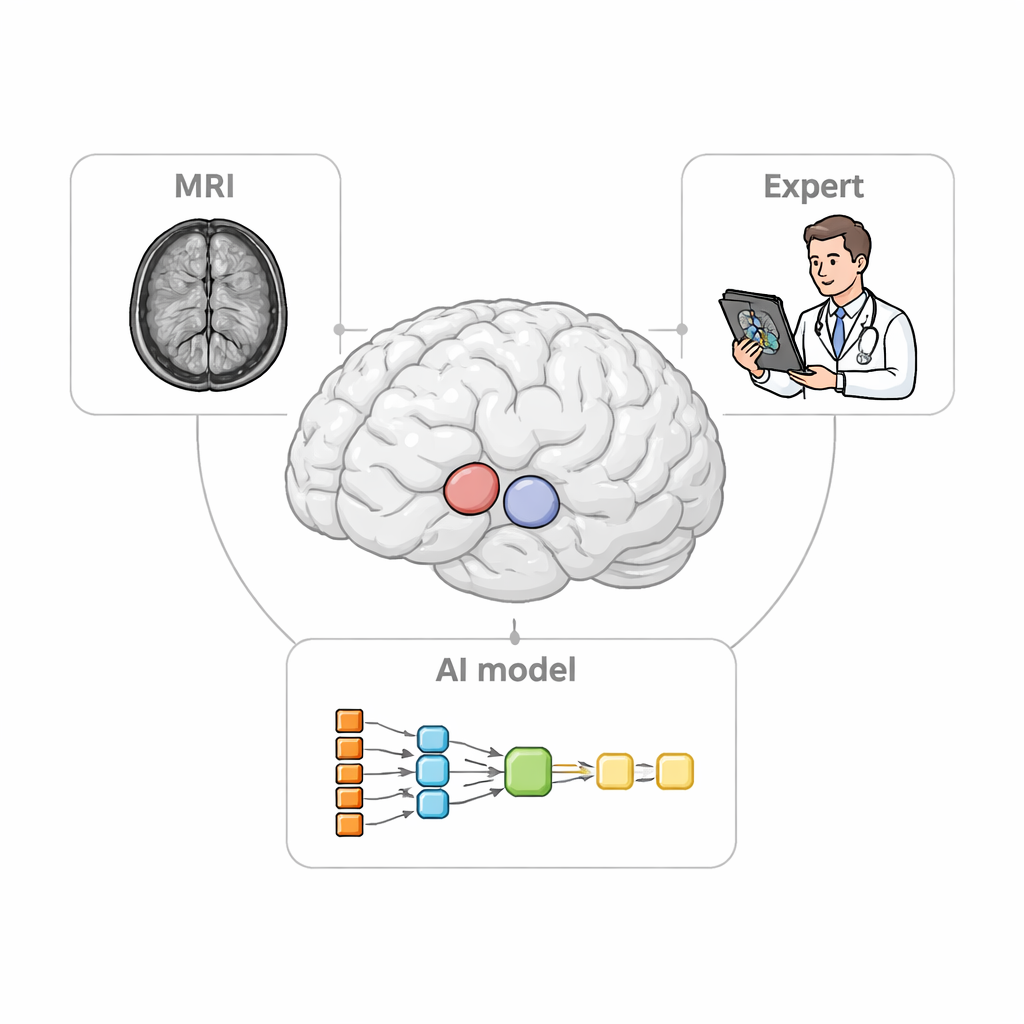
Когда неврологи оценивают состояния вроде болезни Паркинсона, они полагаются на ПЭТ‑сканы, чтобы отслеживать, как сигналы, связанные с дофамином, варьируют в разных частях стриатума. Для этого сначала нужно определить небольшие трёхмерные «регионы интереса» на МРТ, которые служат «мерными стаканчиками» для ПЭТ‑данных. Ручная разметка этих областей занимает много времени, утомительна и может различаться у разных экспертов. Существующее программное обеспечение способно автоматически выделять лишь более крупные структуры и часто испытывает трудности у пациентов с атрофией или деформацией мозга — распространённой ситуацией при прогрессирующих нейродегенерациях. Эти ограничения размывают реальную картину поражения и снижают диагностическую ценность изображений.
Более умный помощник в два шага
Исследователи спроектировали StriaSeg‑iARM как двухступенчатую систему глубокого обучения, работающую прямо в пространстве мозга конкретного человека, а не навязывающую скан в стандартный шаблон. На первом этапе программа находит общий стриатум на трёхмерной МРТ. На втором этапе она делит эту структуру на 12 анатомически определённых подрегионов по обеим сторонам мозга. Между этими этапами находится ключевое новшество: интерактивный шаг, в котором эксперт может быстро проверить и при необходимости исправить грубый контур, созданный первым этапом, прежде чем запускать более детальную разметку. Такой подход сочетает скорость автоматизации с суждением обученного наблюдателя‑человека.
Обучение и тестирование на реальных мозгах
Чтобы научить систему распознавать нужные структуры, команда собрала сотни МРТ‑сканов из нескольких больниц и на разных аппаратах и подготовила аккуратные ручные очертания 12 подрегионов стриатума. Затем они протестировали модель на двух внешних наборах данных, включавших МРТ и ПЭТ‑сканы, связанные с дофамином: один — от пациентов с относительно ранней стадией болезни Паркинсона и здоровых добровольцев, другой — от старшей, более тяжело поражённой клинической группы с выраженной атрофией и смешанными диагнозами. В этих сложных случаях StriaSeg‑iARM последовательно лучше соответствовал ручной разметке экспертов по сравнению с традиционными методами, основанными на атласах, и упрощённой одноэтапной моделью глубокого обучения, демонстрируя более высокое перекрытие, точные контуры и стабильные измерения объёма.
Более точные измерения для химических сканов мозга
Поскольку конечная цель — количественно оценивать сигналы ПЭТ, авторы также изучили, как разные методы сегментации влияют на результирующие ПЭТ‑показатели. Используя стандартную метрику связывания тракера в каждом подрегионе, они сравнили автоматические результаты с теми, что основаны на ручной разметке. Метод на основе атласа склонялся к занижению связывания, особенно у пациентов с более выраженными изменениями, в то время как базовая модель глубокого обучения по‑прежнему демонстрировала заметную систематическую ошибку в некоторых областях. Напротив, каскадные модели — особенно при использовании интерактивного шага коррекции — давали значения ПЭТ, которые тесно соответствовали эталону экспертов, с минимальной смещённостью и рассеянием. Команда также показала, что простая оценка неопределённости с первого этапа позволяет отобрать примерно четверть самых сложных случаев, где действительно требуется доработка эксперта, оставляя остальное полностью автоматическим.
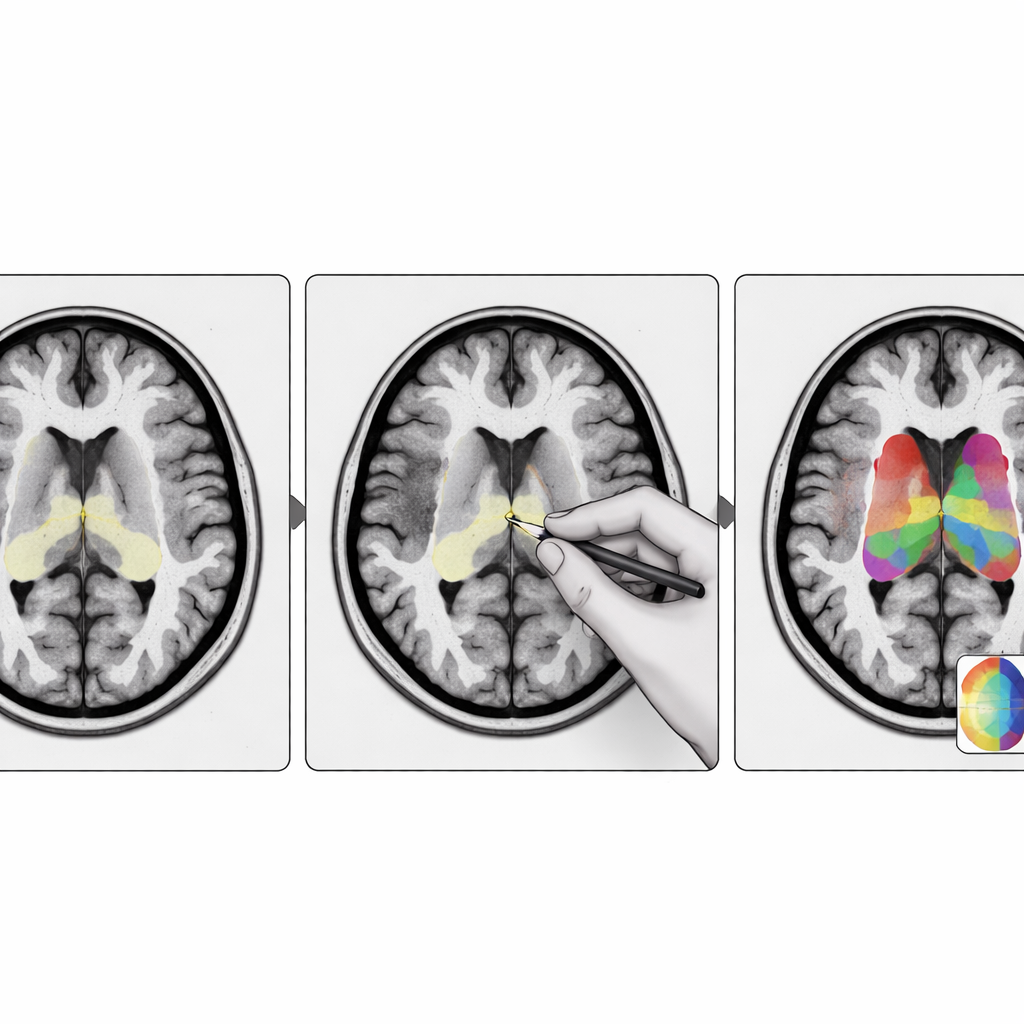
Что это значит для пациентов и клиницистов
Для неспециалистов ключевая мысль такова: более точные цифровые карты мелких участков мозга делают химические сканы мозга более надёжными. StriaSeg‑iARM предлагает гибкую схему, в которой модель глубокого обучения выполняет основную работу, но специалисты могут вмешаться и скорректировать сложные случаи без необходимости дообучать систему. Такое сочетание автоматизации и экспертного контроля повышает точность измерений, используемых для диагностики и мониторинга таких заболеваний, как болезнь Паркинсона, и может быть адаптировано для других органов и патологий, где мелкие, трудноразличимые структуры содержат важные клинические подсказки.
Цитирование: Kim, J., Kim, D., Kim, S. et al. An interactive cascaded deep learning framework with expert refinement for accurate striatal subregion segmentation. Sci Rep 16, 6550 (2026). https://doi.org/10.1038/s41598-026-36399-0
Ключевые слова: изображение при болезни Паркинсона, сегментация стриатума, глубокое обучение в радиологии, ПЭТ МРТ головного мозга, биомаркеры нейродегенерации