Clear Sky Science · ru
Штамм Staphylococcus capitis, продуцирующий два бактериоцина — капидермицин и микрококцин P1, демонстрирует широкий спектр антимикробной активности
Почему крошечные кожные бактерии важны в борьбе с супербактериями
Инфекции, устойчивые к антибиотикам, растут во всем мире, и у врачей заканчиваются надежные препараты. Одна из перспективных идей — задействовать наших «полезных» микробов для борьбы с патогенами. В этом исследовании внимание сосредоточено на обычном кожном бактерии Staphylococcus capitis: показано, что один штамм, обозначенный HBC3, естественным образом продуцирует две мощные молекулы, убивающие микробы. Вместе эти вещества подавляют опасные госпитальные патогены, включая метициллин-резистентный Staphylococcus aureus (MRSA), что указывает на возможность использования дружелюбных кожных бактерий как будущих средств борьбы с инфекциями.
Житель кожи с скрытой «огневой мощью»
S. capitis обычно тихо обитает на нашей коже, особенно на коже головы, и обычно безвреден. Исследователи просеяли 18 штаммов S. capitis, выделенных из носовой полости людей, чтобы выяснить, есть ли среди них те, которые подавляют MRSA — важную причину трудно поддающихся лечению инфекций. Один штамм, HBC3, выделился. В лабораторных тестах он мощно подавлял широкий спектр грамположительных бактерий, включая MRSA, ванкомицин-резистентные энтерококки (VRE), Streptococcus pyogenes, Listeria monocytogenes, а также виды Bacillus и Clostridium, способные вызывать серьёзные заболевания. Примечательно, что он не оказывал влияния на несколько распространённых грамотрицательных бактерий, таких как Escherichia coli и Klebsiella pneumoniae, что указывает на целенаправленное, а не беспорядочное убивающее действие. 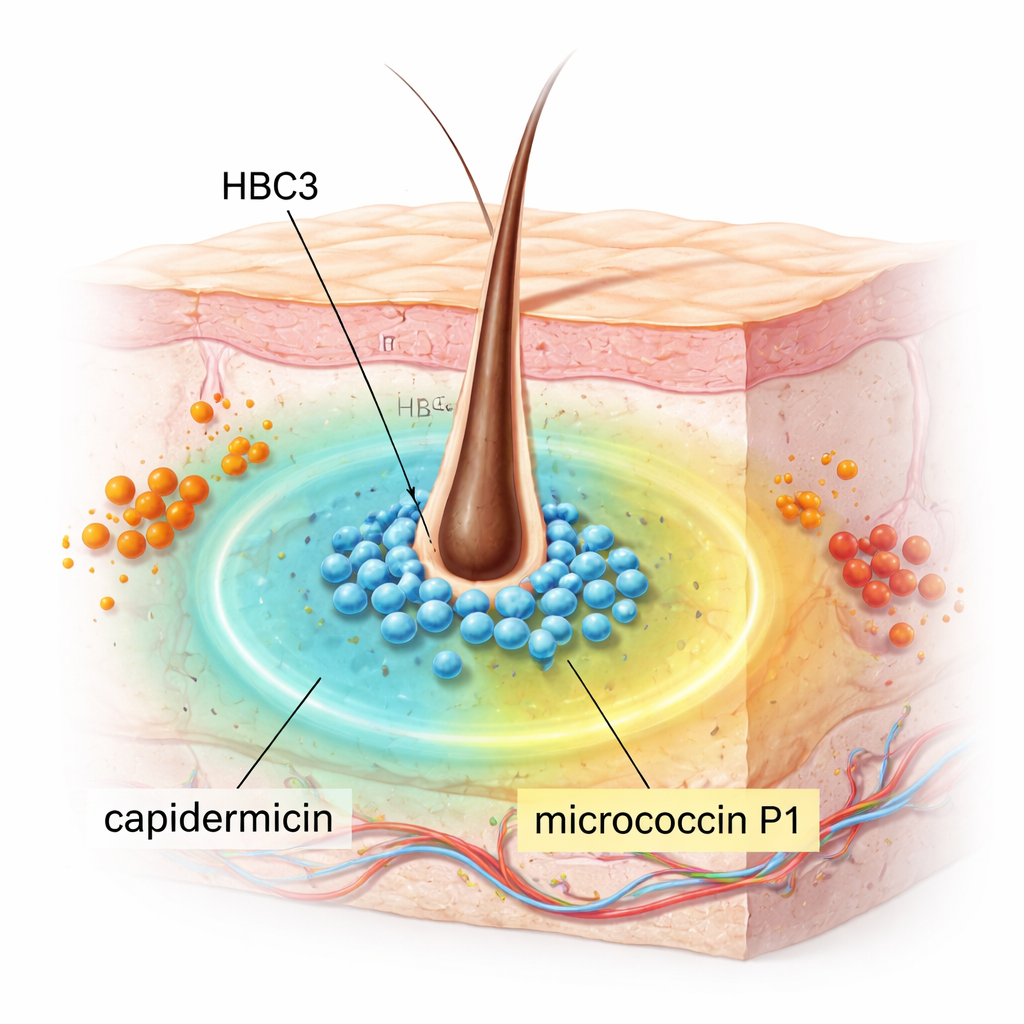
Два природных антибиотика на одном генетическом «мини-хромосоме»
Чтобы выяснить, за счёт чего HBC3 обладает таким широким антимикробным эффектом, команда расшифровала его геном. Они обнаружили небольшую кольцевую ДНК-структуру — плазмиду под названием pHBC3_1, содержащую полные инструкции по синтезу двух разных бактериоцинов — природных пептидов, похожих на антибиотики. Один из них — капидермицин, небольшой положительно заряженный пептид, ранее обнаруженный в других штаммах S. capitis. Другой — микрококцин P1 (MP1), тиопептид, блокирующий белковую синтез в клетках-мишенях и ранее не описанный у S. capitis. После удаления этой плазмиды HBC3 полностью потерял свою антибактериальную активность, что подтверждает, что эти гены необходимы для его защитных свойств.
Разные мишени — общая цель
Очищая каждый бактериоцин отдельно, учёные протестировали их активность против различных микроорганизмов. MP1 показал широкий и сильный эффект против многих грамположительных кокков, включая MRSA и энтерококки, при низких концентрациях. Капидермицин, напротив, был наиболее эффективен против палочковидных грамположительных бактерий, таких как Bacillus coagulans и Listeria, но при условиях этого исследования слабо действовал или не действовал на стафилококки. При сочетании обоих пептидов против B. coagulans наблюдался аддитивный эффект: более низкие дозы в сочетании давали более сильное подавление роста, чем любой из них по‑отдельности. Такое комплементарное нацеливание позволяет HBC3 подавлять более широкий круг конкурентов, используя две разные молекулярные «противоракеты», настроенные на разные формы бактериальных клеток и поверхности. 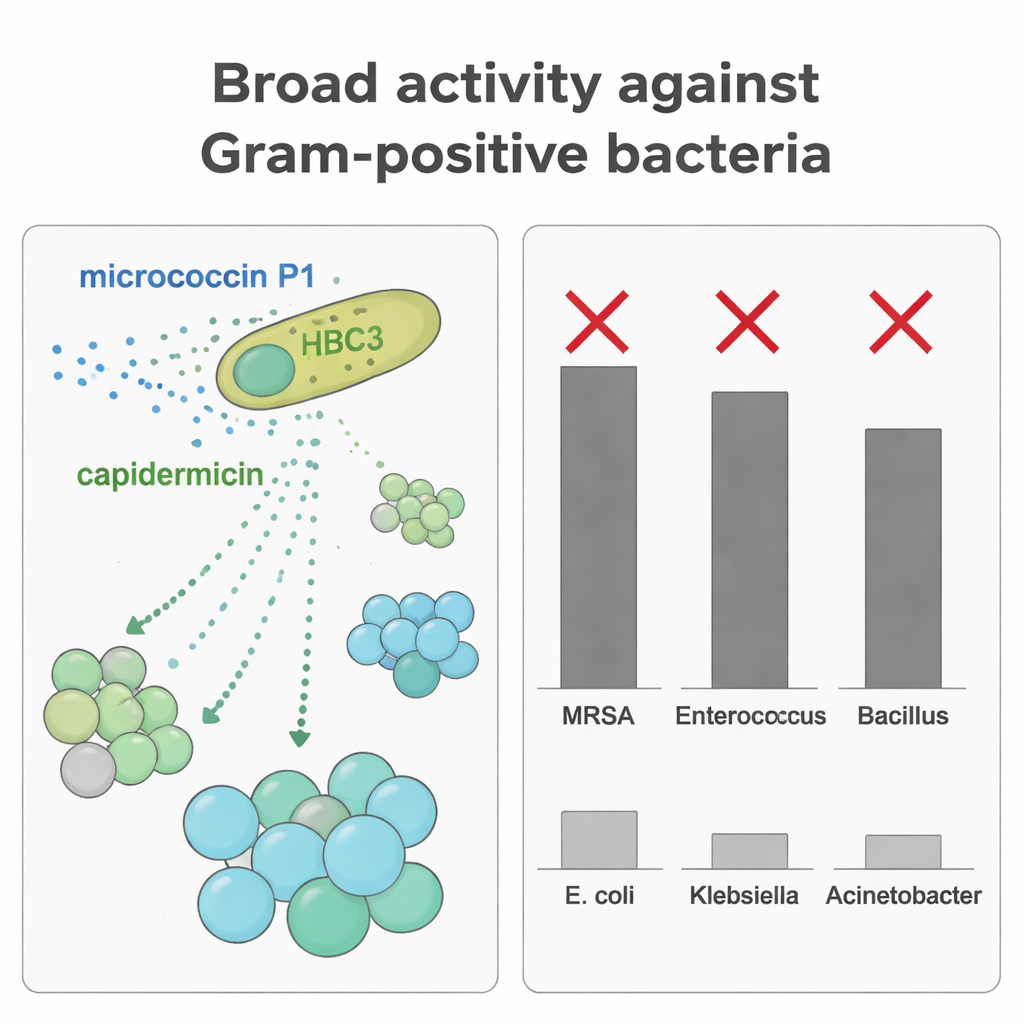
Выигрыш территории в густонаселённых микробных сообществах
Чтобы смоделировать реальную конкуренцию, исследователи совместно культивировали HBC3 с MRSA, VRE и B. coagulans на одних и тех же питательных средах. Нормальный штамм HBC3 почти полностью устранял эти патогены из смешанных сообществ, тогда как версия без плазмиды позволяла им размножаться. Сравнение генов указывает, что плазмида с двумя бактериоцинами, вероятно, образовалась в результате прошлых слияний и перестановок отдельных плазмид с участием подвижных ДНК-элементов, которые могут перемещать генные кластеры между бактериями. Эта составная плазмида даёт HBC3 явное преимущество в плотных средах обитания, таких как кожа или слизистые, где многие микроорганизмы конкурируют за питательные вещества и пространство.
От союзника на коже к возможному пробиотику?
Авторы приходят к выводу, что S. capitis HBC3 оснащён редким сочетанием двух различных бактериоцинов на одной плазмиде, что позволяет ему сильно подавлять несколько клинически важных грамположительных патогенов, включая штаммы, устойчивые к антибиотикам. Поскольку сам HBC3 не относится к известным высокорисковым линиям и не содержит обнаруживаемых генов резистентности к лекарствам, он может рассматриваться как кандидат для разработки целевого пробиотика или средства деколонизации — например, для селективного подавления S. aureus на коже или в носовой полости при сохранении более безвредных обитателей. Прежде чем такие подходы станут реальностью, потребуется тщательное тестирование безопасности, эффективности в животных и людях, а также долгосрочного влияния на нормальную микробиоту, но работа подчёркивает, что наши собственные микробы могут помочь противостоять текущему кризису супербактерий.
Цитирование: Ohdan, K., Suzuki, Y., Kawada-Matsuo, M. et al. Staphylococcus capitis strain producing dual bacteriocins, capidermicin and micrococcin P1, shows broad-spectrum antimicrobial activity. Sci Rep 16, 6835 (2026). https://doi.org/10.1038/s41598-026-36393-6
Ключевые слова: бактериоцины, Staphylococcus capitis, микрококцин P1, капидермицин, устойчивость к антибиотикам