Clear Sky Science · ru
Производные бис‑1,2,4‑триазола как потенциальные антиоксиданты для терапии пневмонии
Почему важно защищать легкие от «ржавчины»
Пневмонию часто воспринимают просто как тяжелую инфекцию легких, которую можно устранить антибиотиками. Но многие люди с тяжелой пневмонией умирают не только из‑за микробов, но и из‑за чрезмерной реакции организма. Когда иммунные клетки борются с бактериями или вирусами, они выделяют высокореактивные молекулы — химические «искра», которые могут повреждать ткань легких так же, как ржавчина разъедает металл. В этом исследовании изучается новая группа синтетических молекул, называемых бис‑1,2,4‑триазолами, спроектированных как мощные антиоксиданты и одновременно блокаторы бактериального арсенала. Цель — разработать дополнительные препараты, которые защищают легкие, пока антибиотики устраняют инфекцию.
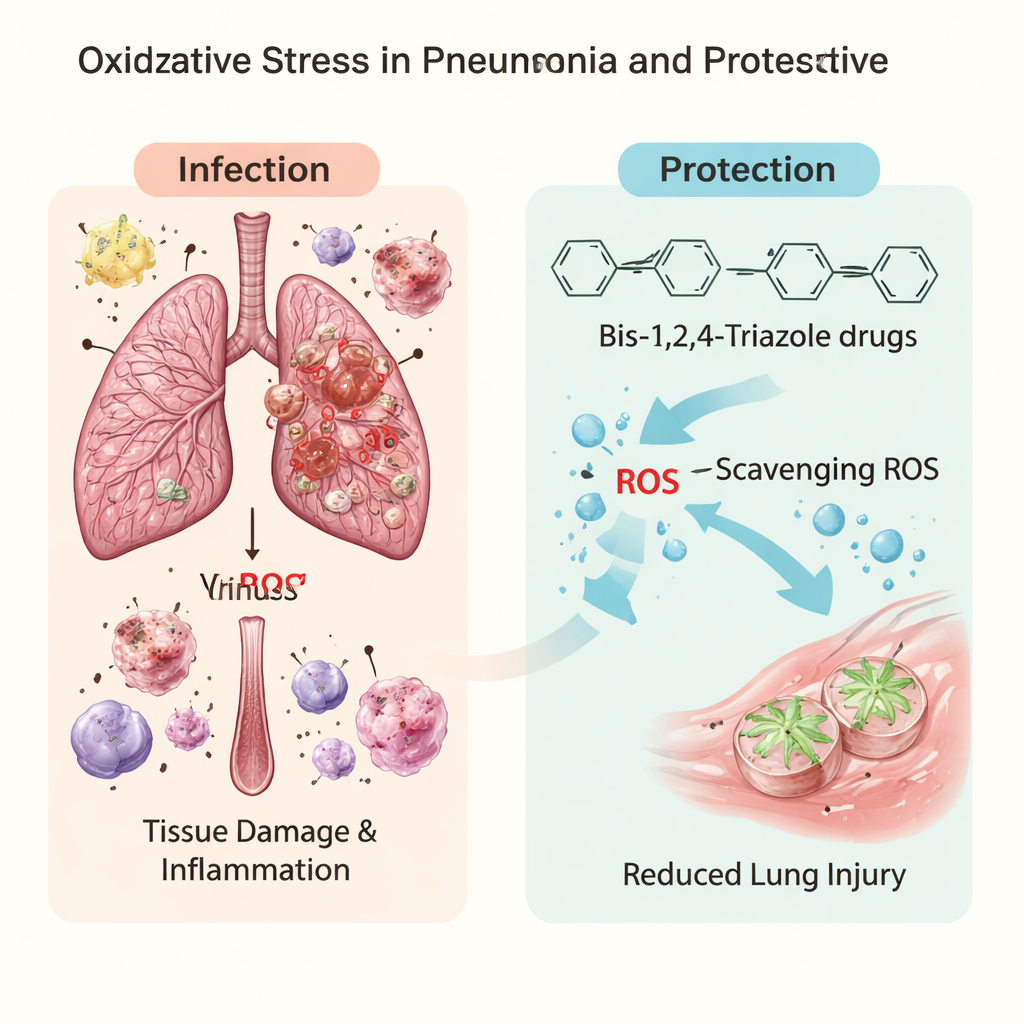
Скрытое повреждение во время инфекции легких
Когда микробы вторгаются в легкие, иммунные клетки выбрасывают вспышки реактивных форм кислорода и азота, или ROS/RNS. В малых количествах они помогают уничтожать патогены; в избытке атакуют собственные жиры, белки и ДНК организма. Последние клинические исследования показывают, что у людей с тяжелой пневмонией, включая пневмонию при COVID‑19, имеются явные признаки оксидативного стресса и нарушения редокс‑баланса. Эта химическая перегрузка ослабляет тонкие воздухообменные альвеолы, поддерживает неконтролируемое воспаление и способствует развитию острой дыхательной недостаточности. Это натолкнуло исследователей на мысль, что целенаправленные антиоксиданты могли бы действовать как брандмауэры — поглощать эти реактивные молекулы прежде, чем они «сожгут» легочную ткань.
Проектирование новых малых молекул для защиты легких
Команда сосредоточилась на кольцевой химической структуре, называемой 1,2,4‑триазолом, уже широко представленной в лекарствах. Вместо одного кольца они связали два кольца вместе, получив бис‑1,2,4‑триазолы, которые могут взаимодействовать как с гидрофильными, так и с липофильными участками клеток и с ионами металлов. Шесть таких соединений ранее были синтезированы и показали антимикробную активность и способность ингибировать фермент, связанный с воспалением и раком. В этой работе авторы задали вопрос, не сделают ли изменение таких характеристик, как длина углеродной цепочки, или добавление нитрогруппы на присоединенном ариле, эти молекулы особенно эффективными в нейтрализации ROS и во вмешательстве в факторы вирулентности бактерий, участвующие в пневмонии.
Испытание антиоксидантной силы в лаборатории
Чтобы оценить, насколько шесть молекул способны улавливать свободные радикалы, исследователи использовали стандартный тест с изменением цвета со стабильным радикалом DPPH. По мере того как антиоксидант удаляет этот радикал, раствор бледнеет с фиолетового до желтого, и степень побледнения можно точно измерить. Все шесть бис‑триазолов показали дозозависимую радикал‑поглощающую активность, но выделились два соединения. Соединение с гибкой шестичленной (гексильной) цепью и другое с пара‑нитрофенильным кольцом приблизились к активности витамина C, классического антиоксиданта. Им потребовалась примерно вдвое большая концентрация по сравнению с витамином C, чтобы достичь той же 50‑процентной отметки блокировки радикалов, но они все равно показали достаточно высокую активность, чтобы рассматриваться как перспективные лиды для лекарств. Их структуры, по‑видимому, помогают им «встраиваться» в липидные мембраны легких и стабилизировать пойманные радикалы.
Блокировка бактериального оружия при сохранении лекарственных свойств
Помимо антиоксидантной активности, команда использовала компьютерное моделирование, чтобы выяснить, могут ли новые молекулы блокировать две ключевые белковые цели Streptococcus pneumoniae: NanA, помогающий бактериям прикрепляться и внедряться в ткани, и пневмолизин (Ply), токсин, пробивающий отверстия в клеточных мембранах. Лучшее связывание в in silico продемонстрировало нитрофенильное соединение, формировавшее несколько водородных связей и стэкинговых взаимодействий в активных карманах белков. Хотя эти молекулы не столь «липкие», как некоторые громоздкие природные полифенолы, бис‑триазолы показали, что их компактный скелет способен занимать те же уязвимые участки NanA и Ply. Параллельные модели абсорбции, метаболизма и токсичности предсказали, что все шесть соединений, особенно два лидера, имеют высокую предполагаемую абсорбцию в кишечнике, низкую токсичность, незначительное вмешательство в основные ферменты метаболизма лекарств и отсутствие склонности нарушать ионные каналы, влияющие на ритм сердца — ключевые признаки «лекоподобного» профиля.
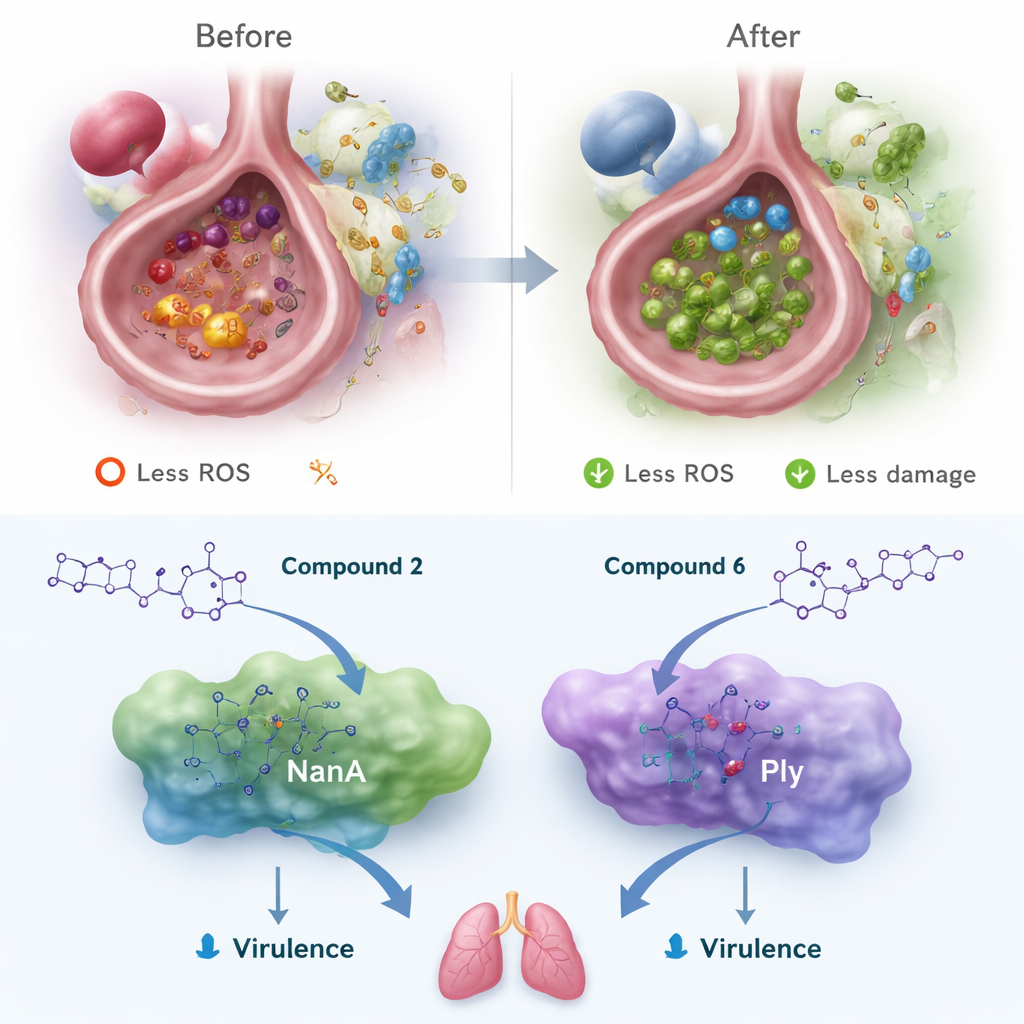
Что это может значить для будущего лечения пневмонии
В совокупности результаты указывают на бис‑1,2,4‑триазолы — особенно на два наиболее эффективных соединения — как на ранние прототипы двойного действия для терапии пневмонии. В принципе такие соединения могли бы одновременно поглощать вредные реактивные молекулы, разрушающие легочную ткань, и притуплять бактериальные инструменты, усугубляющие болезнь, оставаясь при этом достаточно безопасными для приема внутрь и преимущественно не проникая в мозг. Работа остается доклинической: теперь эти соединения должны быть проверены на безопасность в человеческих легочных клетках и на животных моделях пневмонии, а их структуры, вероятно, будут оптимизированы для повышения активности и растворимости. Но исследование дает понятное послание для неспециалистов: будущие методы лечения пневмонии могут опираться не только на антибиотики; они также могут включать малые молекулы, которые защищают наши легкие от побочного ущерба, наносимого собственной иммунной системой.
Цитирование: Korol, N., Symkanych, O., Pallah, O. et al. Bis-1,2,4-triazole derivatives as potential antioxidants for pneumonia therapy. Sci Rep 16, 5640 (2026). https://doi.org/10.1038/s41598-026-36386-5
Ключевые слова: пневмония, окислительный стресс, антиоксиданты, вирулентность бактерий, дизайн лекарств