Clear Sky Science · ru
Понижение экспрессии CDC25C подавляет рост ГЖК за счет митохондриального стресса, индуцирующего аутофагию и апоптоз
Почему это исследование печени важно
Рак печени — один из самых смертоносных видов рака в мире, и многие пациенты диагностируются слишком поздно для эффективного хирургического вмешательства или стандартной терапии. В этом исследовании изучается один внутриклеточный «переключатель», белок CDC25C, который, по-видимому, стимулирует рост рака печени, тогда как для здоровых печёночных клеток он менее критичен. При его подавлении исследователи обнаружили, что опухолевые клетки испытывают стресс и в конечном итоге погибают через собственные механизмы очистки и самоуничтожения, что указывает на перспективную и более селективную стратегию лечения.
Переключатель роста внутри печёночных опухолей
Каждая клетка должна решать, когда делиться, а когда останавливаться. CDC25C — один из ключевых белков, продвигающих клетки через цикл деления. В раке печени этот «переключатель» часто застревает в положении «вкл», помогая опухолям расти и распространяться. Исследователи использовали клетки рака печени мыши и нормальные печёночные клетки мыши, а также мышей с опухолями, чтобы искусственно снизить уровень CDC25C. С помощью стандартных генетических и белковых тестов они подтвердили, что CDC25C резко уменьшился в экспериментальной группе по сравнению с контрольной, создав надёжную модель для изучения последствий подавления этого переключателя роста.
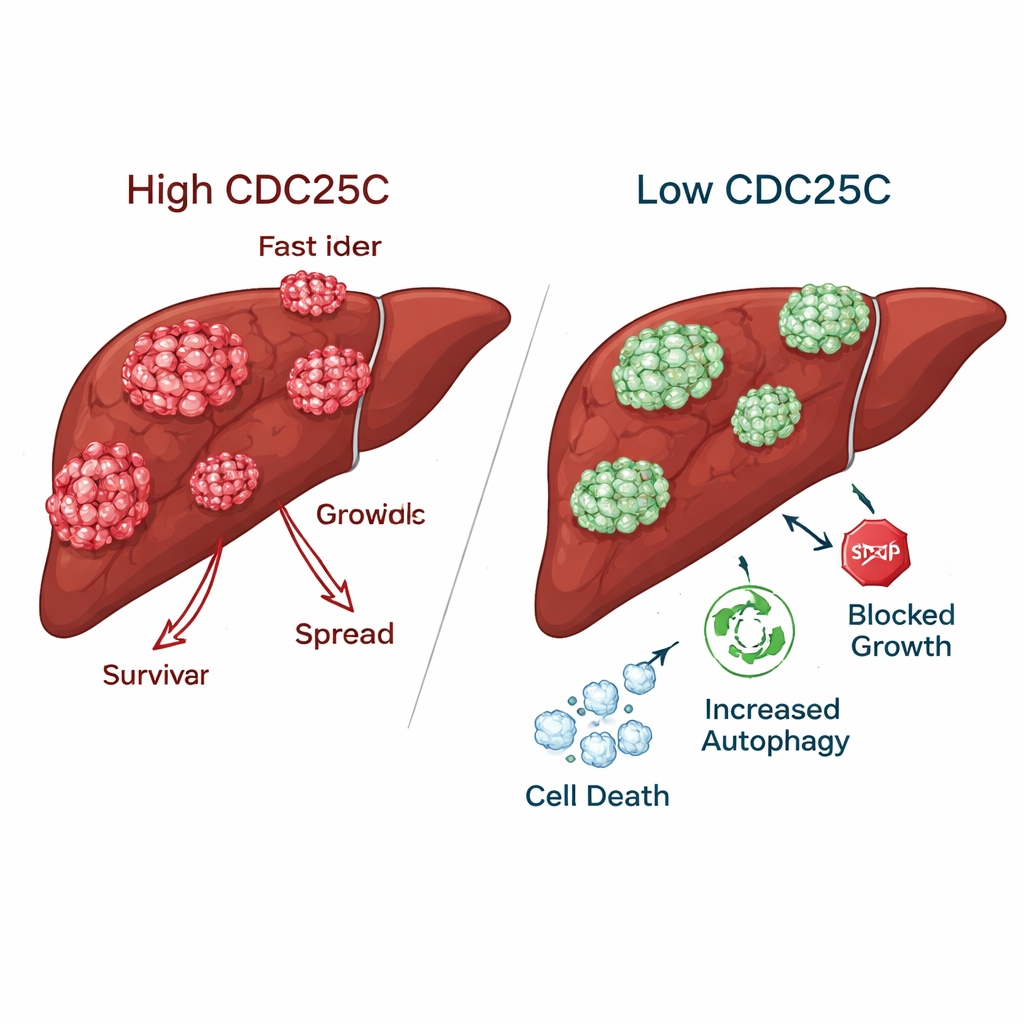
Замедление рака при щажении здоровых печёночных клеток
При снижении CDC25C в клетках рака печени опухоли потеряли многие свои агрессивные черты. Раковые клетки формировали гораздо меньше колоний, мигрировали медленнее по искусственным «ранкам» и хуже преодолевали барьеры в лабораторных тестах. Напротив, нормальные печёночные клетки при понижении CDC25C демонстрировали улучшенный рост и подвижность, что говорит о том, что здоровая ткань может переносить или даже выигрывать от ингибирования CDC25C. У мышей опухоли с пониженным CDC25C показали более низкие уровни этого белка как на уровне гена, так и на уровне белка, подтвердив, что аналогичный эффект возникает и в живом организме.
Стресс энергетических центров и «бригада чистки» клетки
При рассматривании клеток в электронный микроскоп исследователи увидели, что в раковых клетках с низким CDC25C митохондрии были вздутыми и повреждёнными — эти миниатюрные электростанции клетки — наряду с пузырчатыми структурами, называемыми аутофагосомами, которые свидетельствуют об активации системы внутриклеточного «переработки», аутофагии. Исследователи измерили ключевые признаки митохондриального стресса: уровни кальция и реактивных форм кислорода (ROS), оба из которых были повышены в раковых клетках после снижения CDC25C. Маркёры ответа на митохондриальный стресс, включая шапероны вроде HSP60 и два митохондриальных фермента «контроля качества», также оказались повышены, как и CHOP — фактор стресса, связывающий митохондриальные проблемы с более широкими клеточными реакциями. Поразительно, что эти стрессовые сигналы шли в противоположном направлении в нормальных печёночных клетках, что усиливает представление о том, что раковые и здоровые клетки по‑разному реагируют на потерю CDC25C.
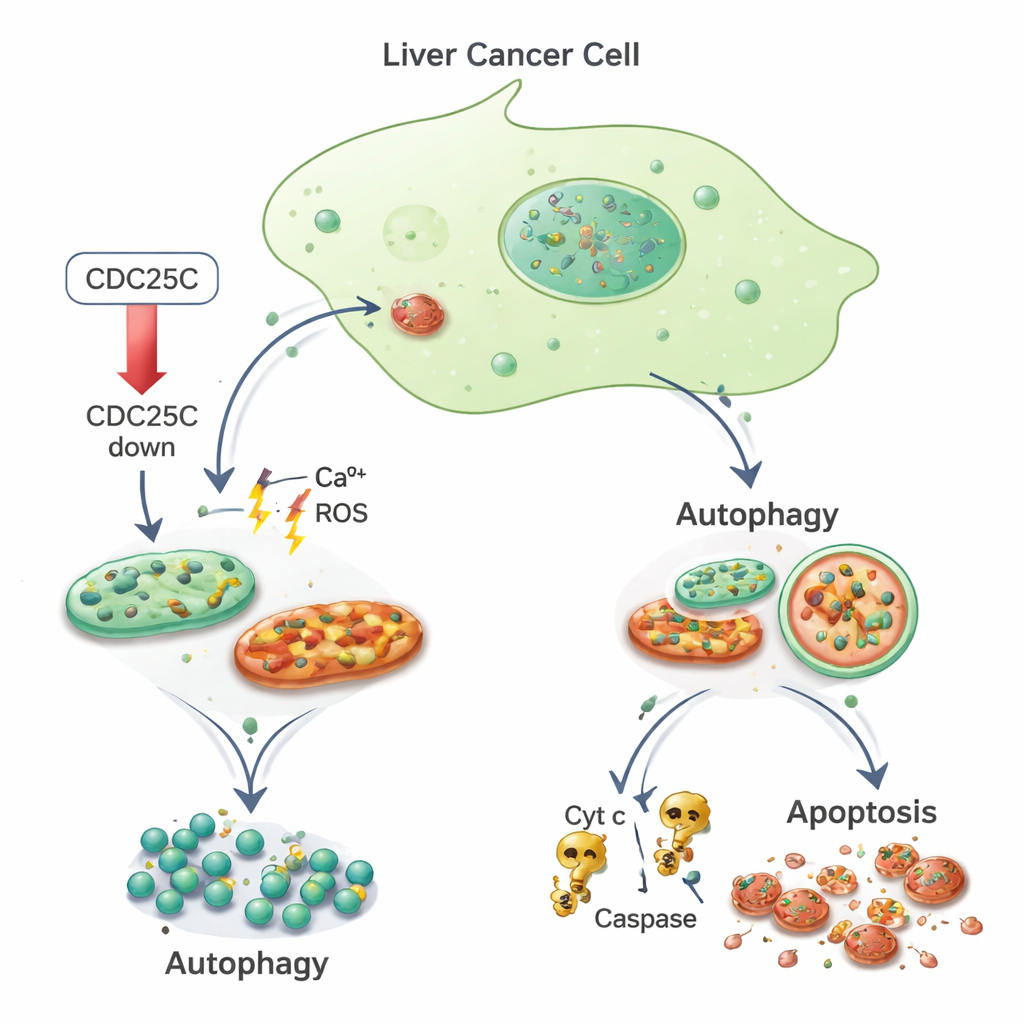
От стресса к самоперевариванию и гибели клетки
Далее команда спросила, как справляются с этим стрессом раковые клетки. Они обнаружили, что маркёры аутофагии повышались как в раковых, так и в нормальных печёночных клетках при снижении CDC25C. Белки, такие как LC3 и p62, отражающие образование и активность аутофагосом, увеличивались, указывая на усиление механизма внутриклеточной очистки. Вместе с тем только в раковых клетках митохондриальное повреждение, по‑видимому, выводило клетки за пределы восстановления и запускало запрограммированную гибель. С помощью флуоресцентных красителей и проточной цитометрии исследователи наблюдали больше раковых клеток с фрагментированными, ярко окрашенными ядрами — признаком апоптоза — и снижением мембранного потенциала митохондрий. Они также обнаружили повышенные уровни цитохрома c и ферментов Caspase-3 и Caspase-9, классических компонентов митохондриально обусловленного пути гибели. Нормальные печёночные клетки, напротив, при тех же условиях пониженного CDC25C демонстрировали меньше апоптоза.
Что это может значить для будущих методов лечения
Для непрофессионального читателя основной вывод таков: подавление CDC25C, по-видимому, поражает раковые клетки печени в их уязвимых местах — перегружая их «электростанции», заставляя механизмы переработки работать сверх меры и в конечном итоге вызывая аккуратную самопереработку и гибель — при этом в основном щадя нормальную печёночную ткань. Авторы заключают, что CDC25C — не просто переключатель роста; он также определяет, как клетки справляются со стрессом, очисткой и гибелью. Поскольку раковые клетки сильно зависят от CDC25C и реагируют на его потерю фатальным митохондриальным стрессом и апоптозом, препараты, нацеленные на этот белок или его нисходящие пути стресса, потенциально могли бы предложить более селективный способ лечения рака печени с меньшим повреждением здоровой ткани.
Цитирование: Miao, X., Zheng, F., Mo, X. et al. CDC25C downregulation suppresses HCC growth via mitochondrial stress-induced autophagy and apoptosis. Sci Rep 16, 5631 (2026). https://doi.org/10.1038/s41598-026-36351-2
Ключевые слова: гепатоцеллюлярная карцинома, CDC25C, митохондриальный стресс, аутофагия, апоптоз