Clear Sky Science · ru
Индуцированная толерантность к УФ-стрессу порождает гетерогенность выживания в изогенных популяциях E. coli
Почему солнечный свет может быть смертельным для микробов
Ультрафиолетовый (УФ) свет от солнца и от дезинфицирующих ламп — мощный способ уничтожения микроорганизмов, включая хорошо знакомую кишечную бактерию Escherichia coli. Тем не менее даже в генетически идентичной группе бактерий некоторые клетки выживают после вспышек УФ, которые уничтожают их соседей. В этом исследовании рассматривается на первый взгляд простой, но важный для дезинфекции и контроля инфекций вопрос: эти выносливые выжившие рождаются иными или же они быстро переключаются в защищённый режим только после того, как повреждение уже началось?
Рождены стойкими или закалены опытом?
В течение многих лет биологи знали, что небольшие субпопуляции бактерий могут временно переносить антибиотики без мутаций, обеспечивающих устойчивость к препаратам. Одна гипотеза говорит, что несколько «праймированных» клеток уже находятся в особом состоянии до появления препарата, в то время как остальные уязвимы. Другая возможность — большинство клеток реагирует только после удара, включая аварийные системы, которые восстанавливают повреждения и сохраняют их в живых. Авторы хотели выяснить, какая из этих историй применима, когда E. coli атакуют не антибиотики, а УФ‑свет, который оставляет шрамы на ДНК клеток.
Хитрый способ проверить скрытые различия
Чтобы отделить предсуществующую жёсткость от моментальных ответов, исследователи применили современную интерпретацию классического эксперимента Лурии–Дельбрюка. Они вырастили много крошечных культур E. coli параллельно. В одних культурах каждая началась с одной клетки, которая размножилась в клон. В других, так называемых контрольных с шумом, каждая культура начиналась с случайной смеси тысячи клеток. Все культуры затем подвергали тщательно дозированным воздействиям УФ‑света от светодиода с длиной волны 262 нанометра и считали выжившие клетки. Если редкое праймированное состояние существовало до УФ‑воздействия, в некоторых культурах, произошедших от одной клетки, по случайности должно было оказаться больше праймированных клеток и демонстрироваться заметно более высокий уровень выживаемости.
УФ‑выжившие становятся таковыми, а не рождаются
При разных дозах УФ выживаемость E. coli варьировала, но не так, как ожидалось, если бы исходная праймированная подгруппа определяла исход. При умеренных и очень сильных УФ‑воздействиях распределение выживших в клонально производных культурах выглядело похоже на распределение в смешанных контрольных культурах. Не выявилось явной подгруппы культур с исключительно высокой выживаемостью, что могло бы указывать на заранее вооружённые клетки. Команда повторила подход с препаратом химиотерапии митомицин C, образующим сшивки в ДНК и повреждающим её иным образом, и снова не нашла признаков стабильной праймированной группы, обладающей широкой толерантностью к повреждению ДНК.
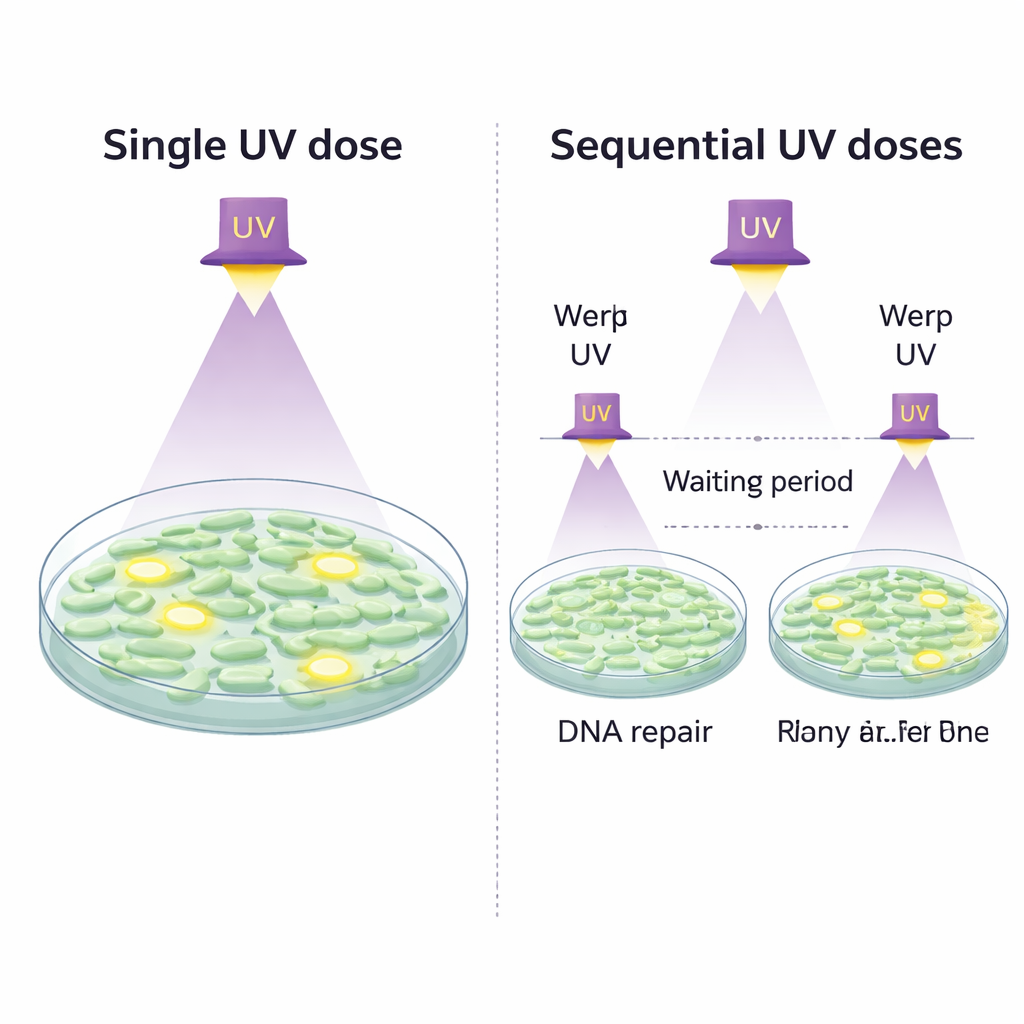
Когда два меньших удара лучше одного большого
Ситуация изменилась, когда команда разделила дозу УФ на две части. Сначала бактериям давали умеренный «первый удар» УФ, затем ждали 30 минут в темноте, чтобы дать время сработать системам ремонта, и затем наносили второе УФ‑воздействие. Если бы выживание было чисто случайным, доля клеток, переживших оба удара, должна была бы равняться произведению выживаемостей при каждой из одиночных доз. Вместо этого фактическая выживаемость после последовательных низких доз оказалась в несколько раз выше, чем простое предсказание, и выше, чем после одного большого импульсного дозирования с тем же суммарным УФ‑энергетическим вкладом. Это указывает на то, что первый удар запускает пути ремонта ДНК, такие как известный SOS‑ответ и нуклеотидный эксцизионный ремонт, которые временно повышают способность клеток справляться с последующими повреждениями.
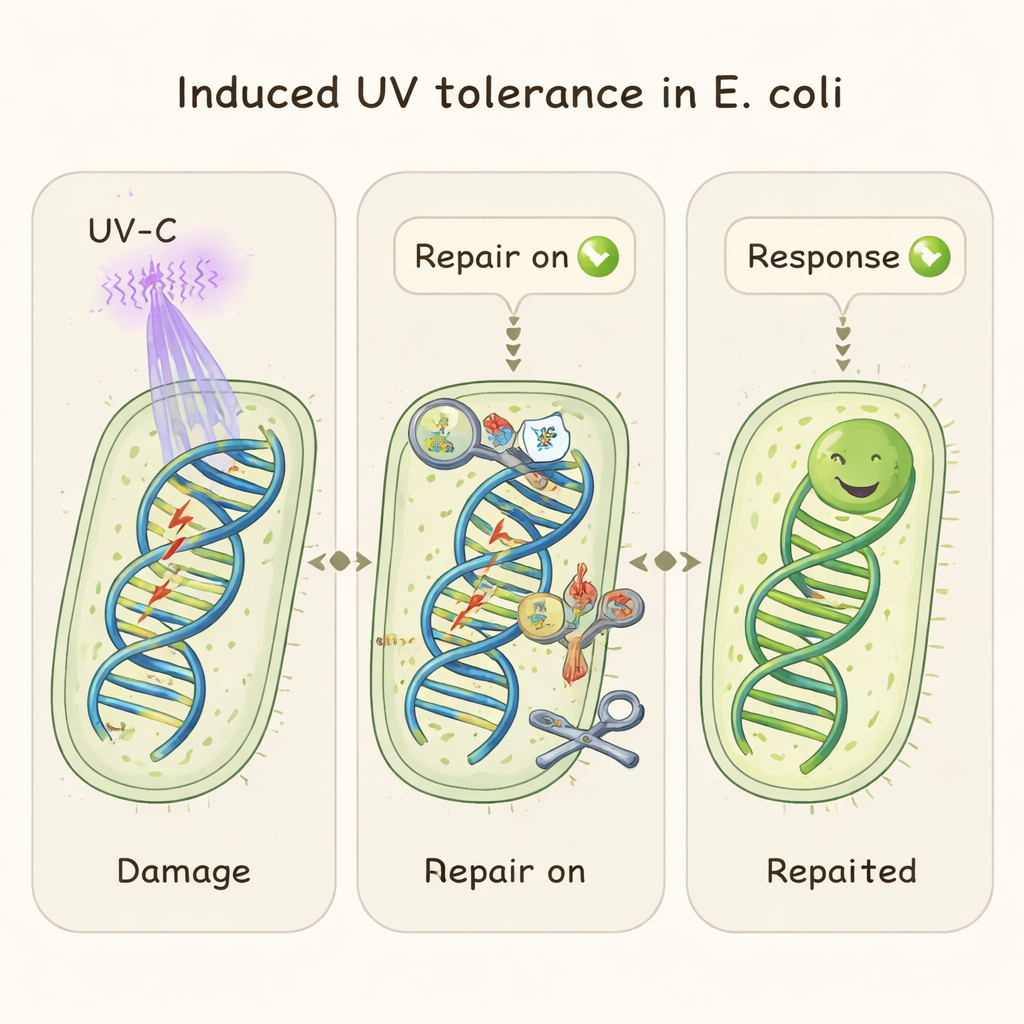
Что это значит для дезинфекции и выживания
Проще говоря, эта работа показывает: генетически идентичные клетки E. coli не защищены от УФ потому, что некоторые из них «рождаются» экранированными; напротив, большинство выживших быстро закаляются после первого воздействия, включая аварийные механизмы ремонта ДНК. Эта индуцированная, кратковременная толерантность помогает им пережить последующие УФ‑воздействия лучше, чем ожидалось. Для технологий, основанных на УФ‑дезинфекции воды, поверхностей или медицинского оборудования, это означает, что важны не только суммарная энергия, но и схема дозирования и временные интервалы. Понимание того, как бактерии динамически восстанавливают ДНК при повторных стрессах, может помочь разработать более надёжные стратегии стерилизации и углубить представления о том, как простые организмы адаптируются к суровым условиям, не изменяя свой генетический материал.
Цитирование: Ichikawa, S., Tanoue, M., Takeuchi, J. et al. Induced tolerance to UV stress drives survival heterogeneity in isogenic E. coli cell populations. Sci Rep 16, 5931 (2026). https://doi.org/10.1038/s41598-026-36328-1
Ключевые слова: Толерантность к УФ-стрессу, Escherichia coli, Ремонт ДНК, бактериальные персистеры, SOS-ответ