Clear Sky Science · ru
Слабоконтролируемая сегментация колоректальных желез посредством самообучения и псевдоразметки на основе внимания
Почему это важно для диагностики рака
Когда патолог рассматривает биопсию толстой кишки под микроскопом, одна из важнейших подсказок о тяжести рака — форма и организация крошечных трубчатых структур, называемых железами. Тщательное ручное обведение каждой железы медленное, дорогое и трудно стандартизируемое между больницами. В этом исследовании показано, как искусственный интеллект может научиться выделять эти железы почти так же хорошо, как эксперты, при значительно меньшей детальной разметке со стороны человека, что потенциально ускоряет и повышает точность диагностики колоректального рака.
Проблема обведения каждой мелкой границы
Колоректальный рак — один из самых распространённых и смертельных видов рака в мире, и оценка его тяжести во многом зависит от внешнего вида желез. В здоровых или ранних стадиях железы выглядят как аккуратные круглые трубки; в агрессивных опухолях они становятся зубчатыми, срастаются или едва узнаваемы. Компьютеры можно обучить сегментировать, то есть «закрашивать», каждую железу для автоматических измерений, но традиционные системы глубокого обучения требуют трудоёмкой покадровой разметки, выполненной экспертами-патологами. В реальной клинической практике гораздо проще получить простые метки на уровне изображения, например указание того, содержит ли фрагмент ткани железы, или является ли он доброкачественным или злокачественным.
Обучение ИИ на немаркированных и слабо размеченных слайдах
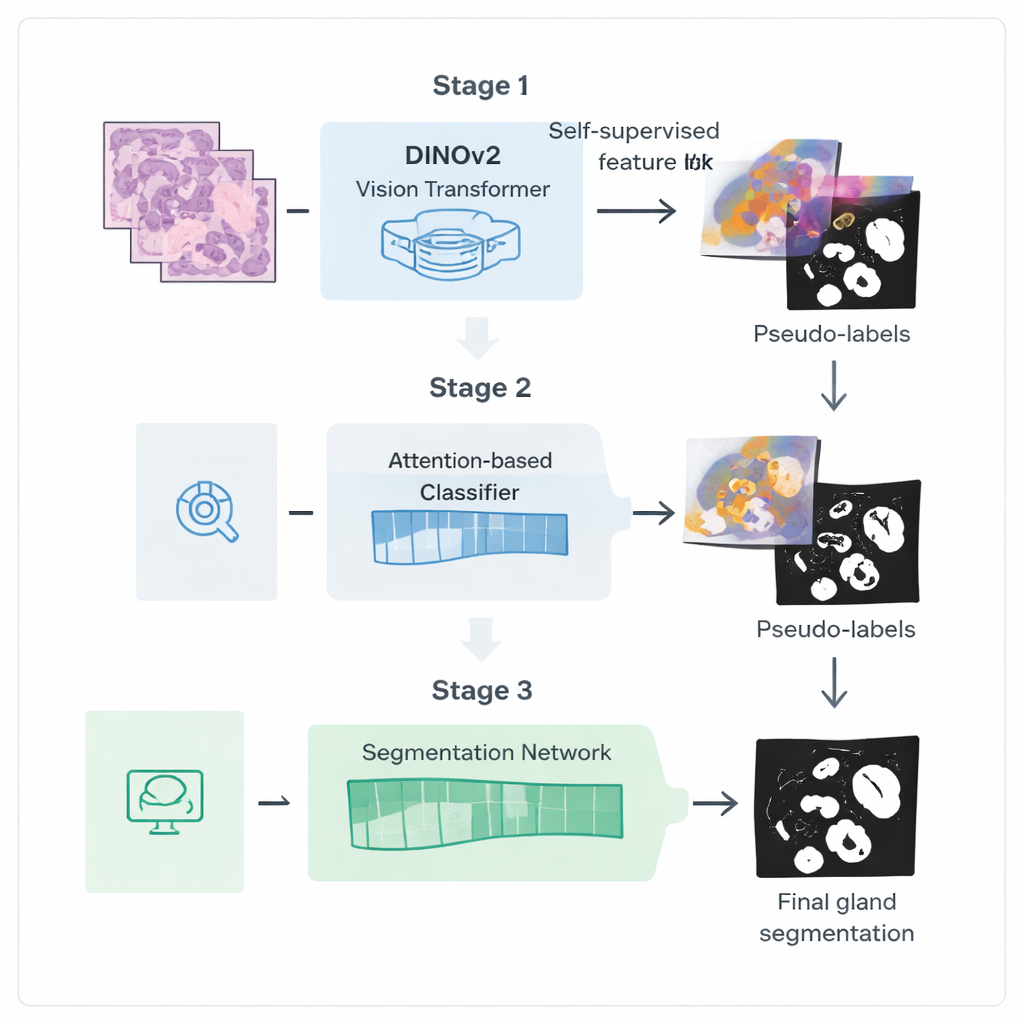
Авторы предлагают трёхэтапный процесс обучения, призванный извлечь больше пользы из таких слабых меток. Сначала они берут мощную модель зрения DINOv2, изначально обученную на натуральных фотографиях, и предоставляют ей тысячи немаркированных изображений биопсий толстой кишки. Требуя от модели сопоставлять разные виды одного и того же фрагмента ткани, они заставляют её выучить визуальные признаки, адаптированные к цветам и текстурам гистологических препаратов, без каких-либо аннотаций. Этот этап создаёт специализированный «энкодер», преобразующий сырые изображения в богатые внутренние представления, фиксирующие структуры, похожие на железы.
Позволяя ИИ показать, куда он смотрит
На втором этапе этот энкодер подключают к классификационной сети, которой нужны только метки на уровне изображения, например наличие желез. Механизм внимания внутри сети учится придавать большие веса тем областям изображения, которые наиболее важны для её решения. Эти карты внимания фактически подчёркивают, где сеть «считает», что находятся железы. Исследователи превращают эти мягкие тепловые карты в грубые бинарные маски с помощью смешивания и пороговой обработки, затем дополнительно очищают их с помощью вероятностной сглаживающей техники, называемой условным случайным полем (CRF). Результатом становится набор уточнённых псевдоразметок: сгенерированных компьютером контуров желез, которые не идеальны, но достаточно хороши, чтобы направлять более специализированную модель сегментации.
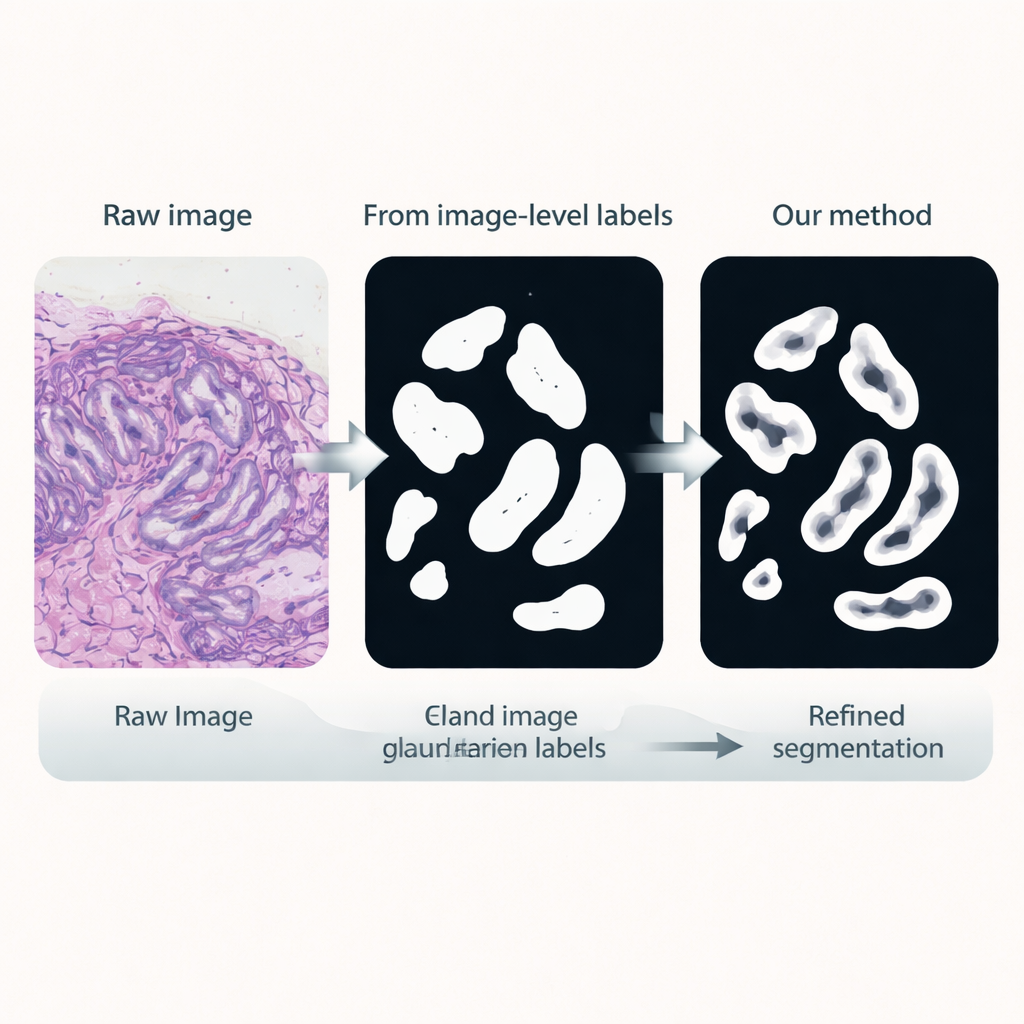
Уточнение границ желез
На третьем этапе посвящённая задача сегментации обучается с использованием этих псевдоразметок в качестве замены ручных аннотаций. Она повторно использует донастроенный энкодер, но добавляет лёгкую декодирующую голову, которая преобразует признаки обратно в подробную маску железы. Важный момент — функция потерь во время обучения обращает особое внимание на границы: ошибки, искажающие края желез, штрафуются сильнее, чем погрешности внутри структуры. Такое обучение, учитывающее границы, стимулирует чёткие, анатомически правдоподобные контуры, что необходимо для точного измерения формы и разделения желез.
Насколько это работает на практике?
Команда протестировала свой метод на двух стандартных бенчмарках колоректальной ткани. На наборе GlaS их слабоконтролируемый подход не только превзошёл другие методы с ограниченными метками, но по ряду показателей приблизился или превзошёл классические полностью контролируемые системы, опирающиеся на полные покадровые аннотации. На более сложном наборе CRAG, содержащем сильно нерегулярные, злокачественные железы, производительность всех методов снизилась, однако новая схема по-прежнему опередила конкурентов со слабыми метками и сократила отставание от полностью контролируемых моделей. Абляционные исследования показали, что каждый компонент — самообучающее донастроивание, псевдоразметка на основе внимания с постобработкой и функция потерь, учитывающая границы — вносит значимый вклад в улучшения.
Что это значит для будущих инструментов в патологии
Для неподготовленного читателя главный вывод таков: эта работа указывает путь к системам ИИ, способным выдавать высококачественные, с чёткими границами карты микроскопических структур желез, опираясь в основном на простые метки на уровне слайда, которые уже доступны в архивах больниц. Сократив зависимость от кропотливой ручной разметки, подход может сделать продвинутую градацию изображений и количественный анализ более реалистичными для многих центров, помогая патологам ставить диагноз колоректального рака более последовательно и эффективно, а в перспективе — применяться и к другим типам тканей и структур.
Цитирование: Wen, H., Wu, Y., Huang, D. et al. Weakly supervised colorectal gland segmentation through self-supervised learning and attention-based pseudo-labeling. Sci Rep 16, 5771 (2026). https://doi.org/10.1038/s41598-026-36256-0
Ключевые слова: колоректальный рак, цифровая патология, сегментация желез, слабоконтролируемое обучение, самообучение в компьютерном зрении