Clear Sky Science · ru
Перепрофилирование дапаглифлозина с помощью полимерных наногелей для терапии колоректального рака
Почему препарат от диабета может помочь в борьбе с раком толстой кишки
Колоректальный рак — одна из ведущих причин смертности от онкологических заболеваний в мире, и у многих пациентов рецидивы возникают несмотря на операцию и химиотерапию. В этом исследовании рассматривается неожиданное средство против этой болезни: дапаглифлозин, распространённая таблетка для лечения сахарного диабета 2-го типа. Упаковывая препарат в крошечные мягкие частицы, которые в желудке превращаются в нежный гель, исследователи стремятся доставить большую его часть в толстую кишку — там, где растут опухоли — сохранив при этом пероральную дозу, сопоставимую с существующими таблетками.
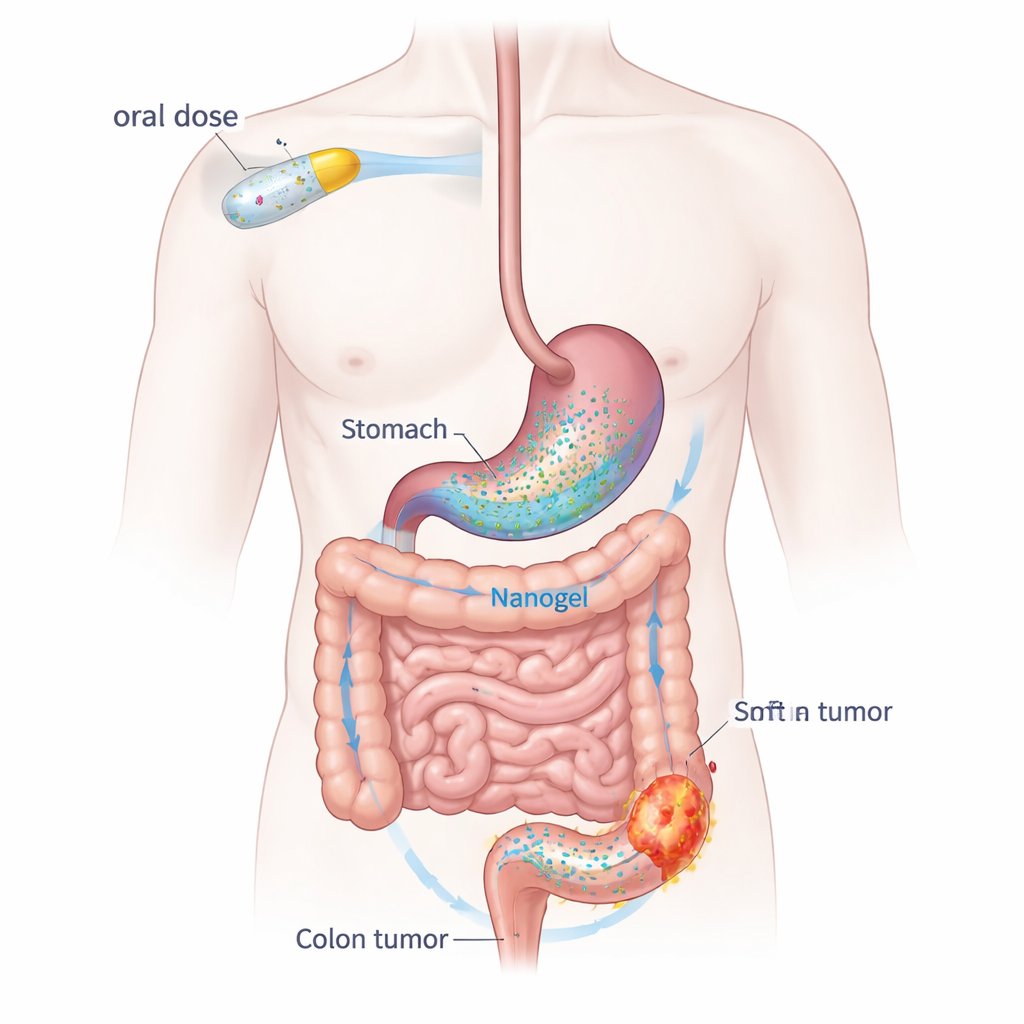
Превращая повседневную таблетку в целевой противораковый груз
Дапаглифлозин обычно действует в почках, снижая уровень сахара в крови, но он также уменьшает воспаление и замедляет рост клеток — два процесса, от которых зависят раковые опухоли. Однако сам по себе препарат плохо растворим в воде и быстро выводится из организма. Чтобы преодолеть эти ограничения, группа создала систему доставки «наногель», используя два пищеподобных полимера: натрий альгинат, получаемый из морских водорослей, и поливиниловый спирт, широко используемый биосовместимый загуститель. Лекарство захвачено внутри наночастиц примерно в одну десятитысячную долю миллиметра. Когда эти частицы попадают в кислую среду желудка, они оседают и сцепляются в мягкую гидрогелевую массу, которая задерживается и затем постепенно высвобождает препарат по мере продвижения к толстой кишке.
Повышение растворимости препарата и замедление его вымывания
Учёные сначала оптимизировали процесс получения частиц, точно подобрав соотношение двух полимеров, чтобы наночастицы оставались мелкими, однородными по размеру и стабильными в жидкости. Они подтвердили, что препарат хорошо внедрён в полимерную сеть и частично перешёл из кристаллической в более аморфную форму, которая обычно растворяется лучше. В тестовых растворах, имитирующих желудочный и кишечный соки, формула наногеля повысила видимую растворимость дапаглифлозина примерно в 1,7–1,8 раза по сравнению с исходным веществом. При контроле скорости выхода препарата наногель демонстрировал мягкий профиль «замедленного высвобождения» в течение нескольких часов вместо быстрого выброса, характерного для простого препарата. Одна из рецептур, обозначенная как F2, образовывала компактный, прочный гель, который сохранялся как минимум два часа в кислых условиях, при этом равномерно высвобождая лекарство.
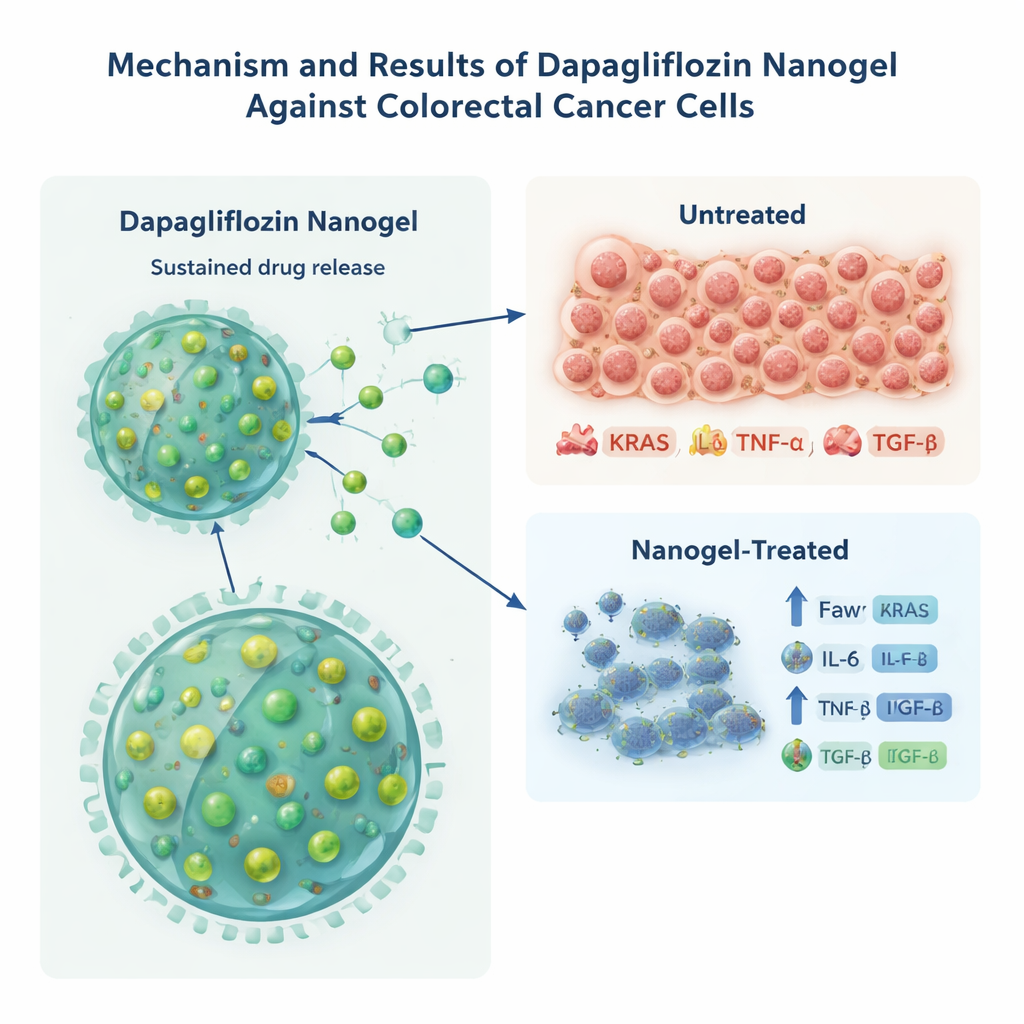
Нагружая раковые клетки стрессом в лаборатории
Чтобы выяснить, может ли новая форма дапаглифлозина действительно повредить раковым клеткам, исследователи испытали её на клетках колоректального рака HCT-116, выращенных в чашках Петри. По сравнению с эквивалентным количеством свободного препарата наногель убивал раковые клетки при более низких концентрациях — дозу, уменьшающую рост клеток вдвое, удалось сократить примерно на треть. Затем группа изучила молекулы, связанные с агрессивным поведением опухолей и хроническим воспалением, включая KRAS (ключевой онкопротеин) и сигнальные белки IL-6, TNF-α и TGF-β. Клетки, обработанные загруженным препаратом наногелем, показали значительно более низкие уровни всех этих маркёров, чем клетки, обработанные свободным препаратом или пустыми частицами, что указывает на то, что длительная экспозиция из наночастиц эффективнее подавляла сигналы, связанные с раком и воспалением. Поскольку используемая клеточная линия уже несёт фиксированную мутацию KRAS, авторы отмечают, что снижение уровня белка KRAS может отражать ответ на стресс, а не прямую коррекцию генетики, но тем не менее это подтверждает сильное биологическое воздействие.
Изменение фармакокинетики препарата в организме
Далее исследователи перешли к животной модели, давая крысам либо простую суспензию порошка дапаглифлозина, либо оптимизированный наногель, оба перорально в одинаковой дозе. В группе наногеля пиковые уровни препарата в крови появлялись позже и были ниже, но препарат дольше оставался в циркуляции. Общая экспозиция (площадь под кривой) выросла умеренно — примерно на 7%, а кажущаяся период полувыведения приблизительно удвоился. Эти изменения означают, что организм получает более плавную, растянутую по времени дозу вместо острого пика и быстрого спада. Такое поведение соответствует дизайну геля: удерживать препарат в кишечнике, медленно высвобождать его и потенциально поддерживать более высокую концентрацию в нижних отделах кишечника и толстой кишке, где образуются опухоли.
Что это может значить для будущей онкотерапии
Проще говоря, это исследование берёт хорошо известный препарат от диабета и оснащает его новой «системой доставки», чтобы он лучше достигал и задерживался рядом с опухолями толстой кишки. Наногель облегчает растворение препарата, замедляет его выведение из кишечника и, по-видимому, делает его более токсичным для клеток колоректального рака при одновременном снижении ключевых сигналов воспаления и роста. У крыс он мягко растягивает присутствие препарата в крови без резкого увеличения общей дозы. Работа всё ещё находится на ранней стадии — ограничена одной клеточной линией и краткосрочными испытаниями на животных — и ещё не показала прямого сокращения опухолей в живых животных или у людей. Тем не менее она закладывает подробную основу для перепрофилирования дапаглифлозина как части будущих подходов к лечению колоректального рака с помощью умных пероральных наногелей, превращающих знакомую таблетку в более прицельный противораковый инструмент.
Цитирование: Abdullah, S., Thiab, S., Altamimi, A.A. et al. A repurposing Dapagliflozin via polymeric nanogels for colorectal cancer therapy. Sci Rep 16, 5625 (2026). https://doi.org/10.1038/s41598-026-36232-8
Ключевые слова: колоректальный рак, репрофилирование препаратов, наночастицы, пероральная доставка лекарств, дапаглифлозин