Clear Sky Science · ru
Национальный геномный надзор за карбапенем- и колистин-резистентными штаммами Klebsiella pneumoniae из крови в Таиланде (2020–2024)
Рост смертельных инфекций крови
Больницы по всему миру сталкиваются с тревожной тенденцией: обычные бактерии, которые когда‑то поддавались самым мощным антибиотикам, становятся почти не поддающимися лечению. В этом исследовании рассматривают Klebsiella pneumoniae — микроорганизм, способный проникать в кровоток и вызывать жизнеугрожающие инфекции — и отслеживают, как он эволюционировал по всей территории Таиланда, становясь устойчивым даже к препаратам последней инстанции. Понимание того, куда распространяются эти супербактерии и как они ускользают от препаратов, крайне важно для защиты пациентов, помощи врачам в выборе терапии и выработки мер общественного здравоохранения.
Отслеживание внутрибольничного супермикроба по всей стране
Исследователи проанализировали 227 образцов Klebsiella pneumoniae, взятых из крови пациентов в больницах Таиланда в период с 2020 по 2024 год. Образцы поступили из национальной сети наблюдения, которая регулярно собирает данные об инфекциях, устойчивых к лекарствам. Лабораторные тесты показали, что более 93% этих изолятов из крови были устойчивы к карбапенемам — мощному классу антибиотиков, который применяют, когда другие препараты неэффективны. Тревожно, что почти треть карбапенем-резистентных штаммов также была устойчива к колистину, одному из последних средств, к которым прибегают врачи. Сочетая стандартные тесты чувствительности с секвенированием целых геномов, команда увидела не только какие препараты не работали, но и какие генетические механизмы бактерии использовали для выживания.
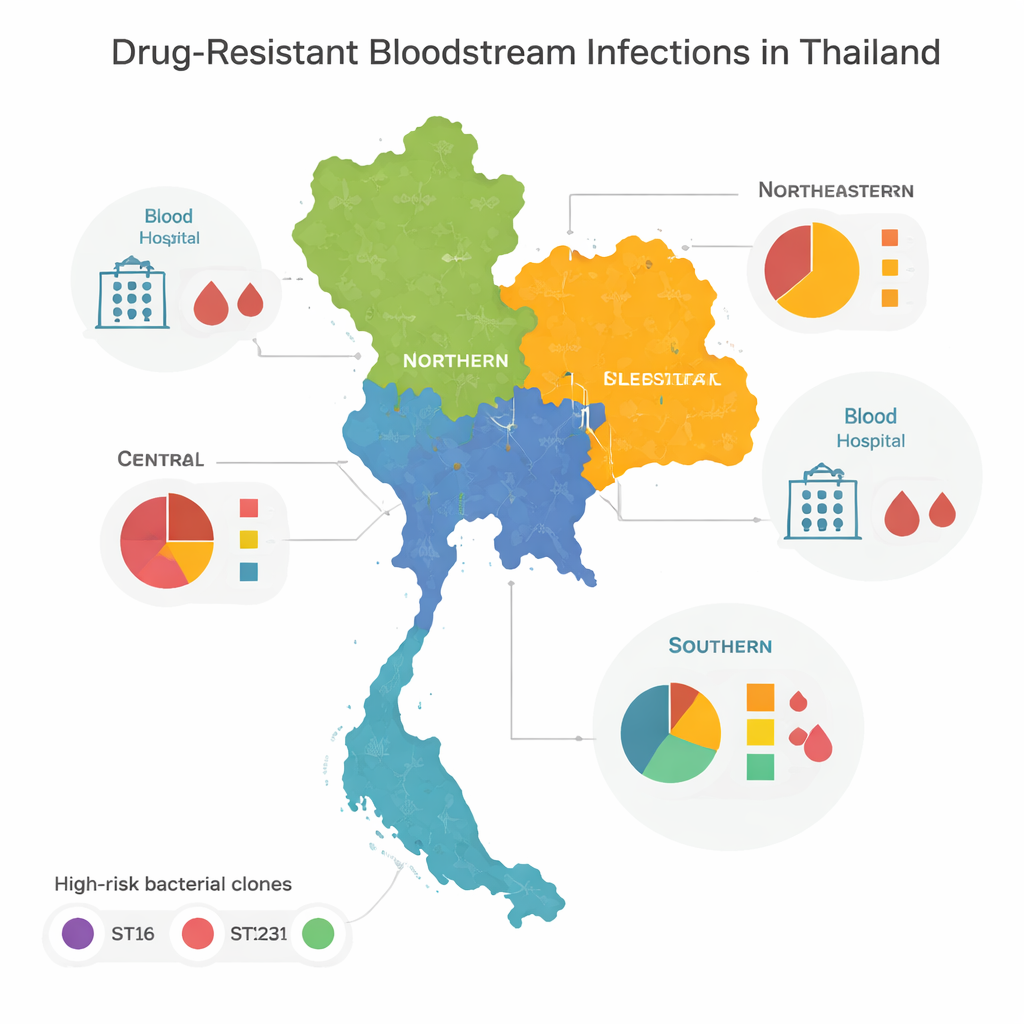
Клоны высокого риска и региональные закономерности
При сравнении геномов команда обнаружила, что большинство резистентных бактерий принадлежали нескольким «высоко-рисковым» семействам или клонам, известным в мире как причины внутрибольничных вспышек. Три из них — ST16, ST147 и ST231 — доминировали в центральной, северной и северо-восточной частях Таиланда. Эти клоны широко распространялись по регионам, что указывает на частое перемещение пациентов, персонала или самих бактерий между больницами. Южная часть страны выглядела иначе: вместо доминирования нескольких типов там наблюдалось большое разнообразие линий бактерий, многие из которых встречались лишь один раз. Такое разнообразие указывает на более сложную комбинацию локальных очагов, экологических источников и трансграничного перемещения, а не на один‑две доминирующие линии.
Как бактерии перехитривают антибиотики
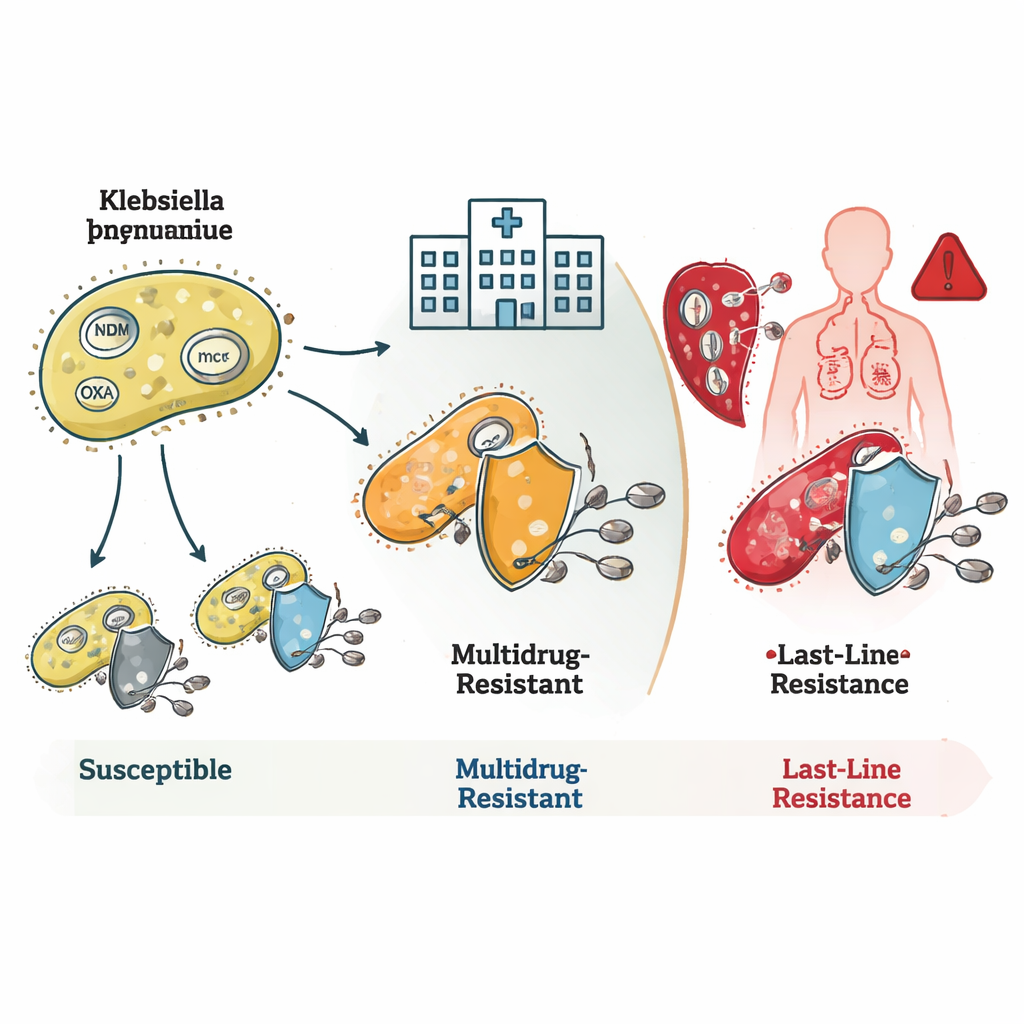
Исследование показало, как эти бактерии накапливают несколько механизмов резистентности. Многие штаммы ST16 и ST231 несли гены, известные как blaNDM и blaOXA, которые кодируют ферменты, разрушающие карбапенемы до того, как те успевают подействовать. У некоторых также были изменения во внешней мембране, уменьшающие вход препаратов, — сочетание этих факторов приводило к очень высокой степени устойчивости. Штаммы ST231 часто несли дополнительный ген rmtF1, блокирующий важную группу препаратов — аминогликозиды, что ещё больше сужало варианты терапии. ST147 выделялся своей генетической гибкостью: он смешивал разные гены резистентности и плазмиды — маленькие мобильные кольца ДНК — что делает его потенциальным центром передачи признаков резистентности другим бактериям.
Отказ препаратов последней инстанции и скрытые угрозы
Наиболее тревожный вывод касался резистентности к колистину — препарату, который врачи резервируют для отчаянных случаев. Некоторые редкие семейства бактерий несли гены mcr, которые могут переходить между видами на плазмидах и напрямую вызывать устойчивость к колистину. Другие, особенно в клонe ST16, были устойчивы к колистину, хотя у них не обнаруживались известные гены или мутации, обеспечивающие такую устойчивость. Это указывает на то, что учёным ещё не полностью известны все механизмы, с помощью которых бактерии нейтрализуют этот препарат последней инстанции. Команда также выявила гипервирулентные штаммы — бактерии, особенно эффективно вызывающие тяжёлые заболевания, — включая одну линию, которая сочетала высокую вирулентность с устойчивостью ко всем исследованным карбапенемам, что представляет собой особенно опасную комбинацию.
Почему геномный надзор важен
Чтобы понять, как генетические изменения отражались в реальных лабораторных неудачах терапии, исследователи использовали статистические модели, связывая конкретные гены резистентности с результатами тестов in vitro. Гены, такие как blaNDM-1 и близкие к нему варианты, показали чрезвычайно сильную связь с карбапенем-резистентностью, подтвердив их ключевую роль в провалах лечения. Однако для колистина большинство резистентных изолятов не имели признанных маркеров резистентности, что указывает на скрытые механизмы, которые ещё предстоит открыть. Авторы утверждают, что регулярное применение секвенирования целых геномов в госпитальном надзоре может работать как система раннего оповещения: выявлять новые клоны высокого риска, отслеживать их перемещение по регионам и границам и направлять оперативные меры по контролю инфекций.
Что это значит для пациентов и политики
Для широкой публики послание жёсткое, но ясное: некоторые инфекции крови в Таиланде теперь вызываются бактериями, устойчивыми почти ко всем доступным врачам препаратам, и несколько опасных семей этих микробов широко распространяются. В то же время исследование показывает, что при наличии правильных инструментов — национального отбора образцов, генетического анализа и быстрой передачи данных — системы здравоохранения могут предвидеть эти угрозы и адаптироваться. Расширение геномного надзора, разработка быстрых молекулярных тестов и ужесточение мер контроля инфекций могут помочь замедлить распространение этих супермикробов и выиграть время для разработки новых лечений и вакцин.
Цитирование: Krobanan, K., Kamjumphol, W., Leethongdee, P. et al. Nationwide genomic surveillance of carbapenem- and colistin-resistant Klebsiella pneumoniae bloodstream isolates in Thailand (2020–2024). Sci Rep 16, 5853 (2026). https://doi.org/10.1038/s41598-026-36228-4
Ключевые слова: антибактериальная резистентность, Klebsiella pneumoniae, инфекция крови, геномный надзор, здравоохранение Таиланда