Clear Sky Science · ru
Пиридиний- и бромзамещённые дистирил-BODIPY красители для митохондрио-таргетной фотодинамической терапии
Освещая раковые клетки изнутри
Фотодинамическая терапия — это метод лечения рака, который использует специальные фотоактивируемые препараты для уничтожения опухолевых клеток при относительном сохранении здоровых тканей. В этом исследовании рассматривается новая семья флуоресцентных красителей, разработанных для направленного накопления в энергетических «станциях» клетки — митохондриях — и при облучении глубоким красным светом генерирующих токсичные формы кислорода, способные уничтожить раковые клетки. Работа демонстрирует как перспективы, так и сложности молекулярного проектирования таких красителей.
Почему нацеливаться на энергетические станции клетки?
Митохондрии играют ключевую роль в выработке энергии и участвуют в решении о выживании или гибели клетки. У раковых клеток мембрана митохондрий обычно обладает более высокой электрической поляризацией по сравнению с нормальными клетками, что делает их более притягательными для положительно заряженных молекул. Исследователи воспользовались этим свойством, присоединив к известному флуоресцентному каркасу BODIPY положительно заряженную пиридинийную группу. Такая конструкция помогает направлять красители в митохондрии, где светозапускные химические реакции могут нанести максимальный вред раковым клеткам при ограничении повреждений в других участках ткани.
Проектирование более умных фотоактивируемых красителей
Команда синтезировала три близких по структуре красителя — PyBHI, PyBMI и PyBBrI, которые главным образом различаются числом атомов брома (нет, один или два). Все они имеют удлинённую конъюгированную структуру, сдвигающую их поглощение и излучение в ближнюю инфракрасную область — полезное окно, где свет проникает глубже в ткань. В теории эти красители могли бы использовать два внутренних пути для достижения триплетного возбужденного состояния, производящего реактивный синглетный кислород: один, обусловленный тяжёлыми атомами брома, и другой, вызванный временным перераспределением заряда внутри молекулы. 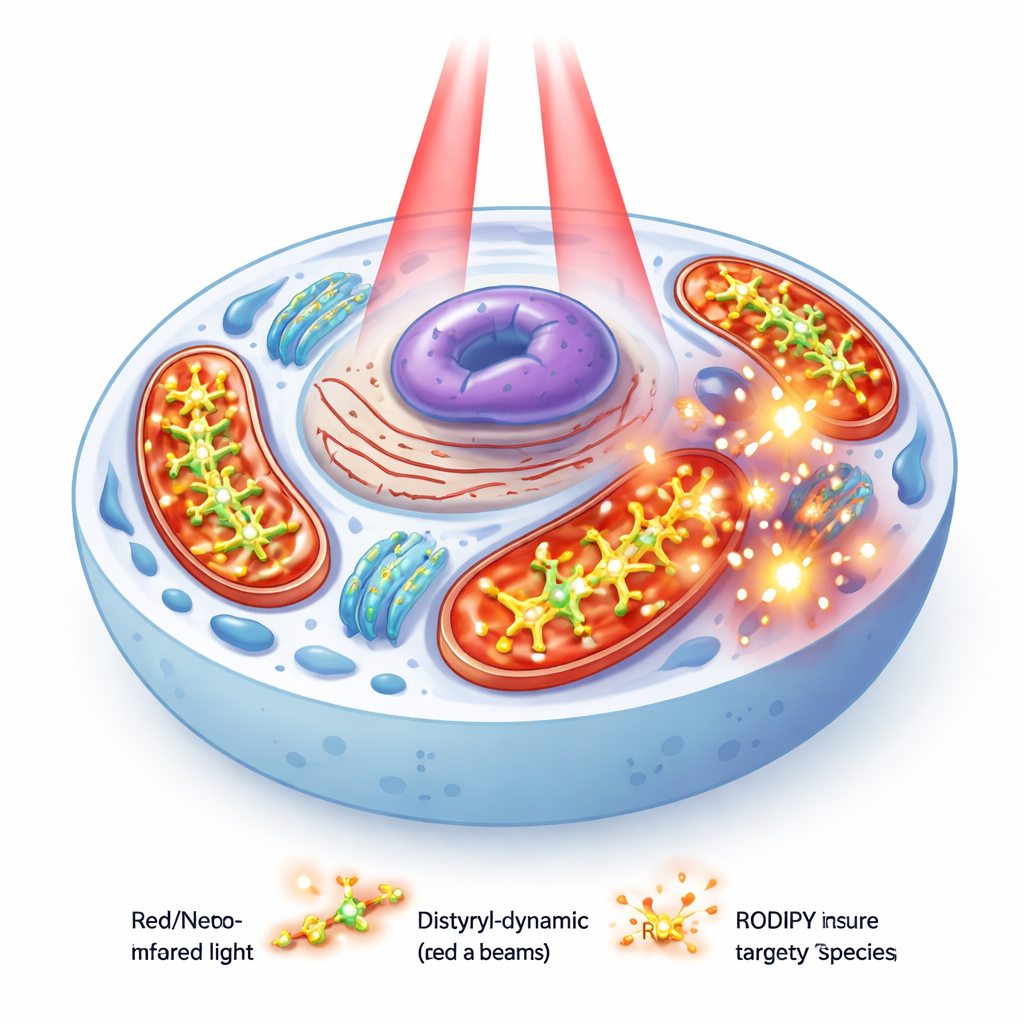
Когда теория сталкивается с экспериментом
Несмотря на изящную концепцию, детальные испытания показали, что красители генерируют синглетный кислород не так эффективно, как ожидалось. С помощью химических проб, теряющих окраску при реакции с синглетным кислородом, исследователи измерили очень низкие выходы генерации кислорода для всех трёх красителей, с лишь умеренным улучшением при добавлении большего числа атомов брома. Ультрабыстрые лазерные эксперименты объяснили причину: после поглощения света красители быстро переходят в состояния со смещением заряда, которые в основном рассеивают энергию в виде тепла, а не преобразуются в желаемое триплетное состояние. В бромированных версиях тяжёлые атомы действительно открывают путь к триплету, но этот путь значительно медленнее конкурирующей релаксации энергии, что ограничивает общую эффективность.
Нацеливание на митохондрии опухоли в живых клетках
Ситуация меняется в биологической среде. В культурах человеческих раковых клеток молочной железы (MCF-7) и шейки матки (HeLa) конфокальная микроскопия показала, что все три красителя интенсивно накапливаются в митохондриях, совпадая по локализации со стандартным митохондриальным маркером. Тесты токсичности в темноте показали, что без света красители в основном безвредны. Однако при облучении красным светом ди-бромированный краситель PyBBrI вызвал значительную гибель раковых клеток: низконаномолярные дозы сокращали жизнеспособность клеток наполовину. Другие два красителя оказались значительно менее эффективны. 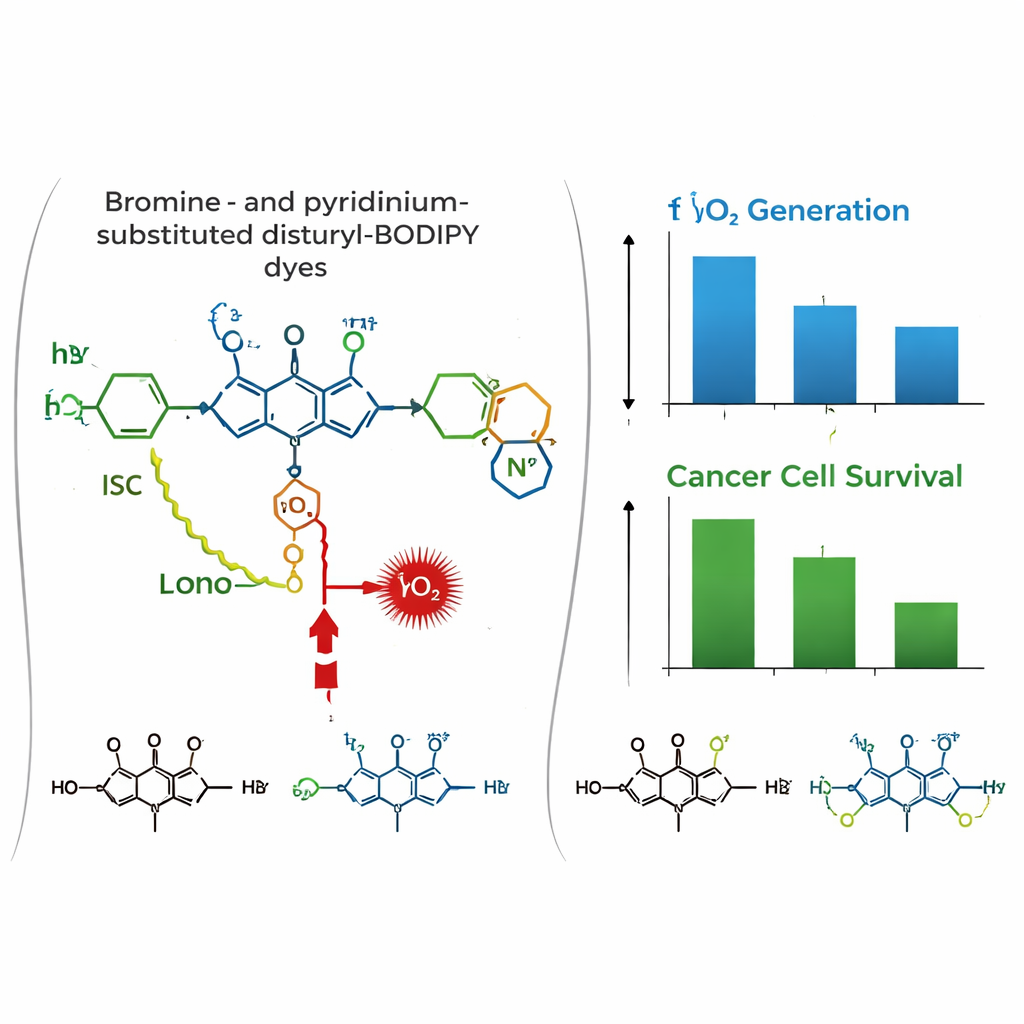
Что это значит для будущих противораковых терапий
Для неспециалиста ключевая мысль такова: небольшие химические модификации могут радикально изменить поведение фотоактивных противораковых препаратов, и их эффективность в живых клетках может оказаться как лучше, так и хуже, чем предсказывают базовые измерения. В данном случае наиболее модифицированный краситель PyBBrI показал лишь скромное образование реактивного кислорода в пробирке, но оказался очень эффективным против раковых клеток, достигнувших их митохондрий. Работа подчёркивает важность направленного доставки препаратов к уязвимым структурам внутри раковых клеток и сложность прогнозирования фотодинамической эффективности. Она указывает путь к следующему поколению митохондрио-таргетных терапий, которые используют ближний инфракрасный свет для селективного «включения» клеткоубивающей химии именно там, где это необходимо.
Цитирование: Kim, C., Badon, I.W., Jo, J. et al. Pyridinium- and bromine-substituted distyryl-BODIPY dyes for mitochondria-targeted photodynamic therapy. Sci Rep 16, 6789 (2026). https://doi.org/10.1038/s41598-026-36213-x
Ключевые слова: фотодинамическая терапия, красители, нацеленные на митохондрии, BODIPY, синглетный кислород, раковые клетки