Clear Sky Science · ru
γ‑излучение вызывает регионально‑специфические субклеточные изменения маркеров бокового амиотрофического склероза и фронтотемпоральной деменции в мозге свиней
Почему важны маленькие дозы радиации и мозги свиней
Большинство из нас мыслит о радиации как о чем‑то исключительно вредном, особенно для мозга. Однако наш мир наполнен низкими уровнями радиации от медицинских сканирований, авиаперелётов и окружающей среды. В то же время учёным всё ещё предстоит разгадать причины бокового амиотрофического склероза (БАС) — смертельного заболевания, которое парализовало бейсбольную звезду Лу Герига — и его близкого «родственника», фронтотемпоральной деменции (ФТД), поражающей поведение и личность. В этом исследовании поставлен удивительно обнадёживающий вопрос: может ли одна скромная доза гамма‑излучения тонко перестроить химию мозга не только в ущерб, но и, возможно, защитно относительно молекулярных изменений, связанных с БАС и ФТД?
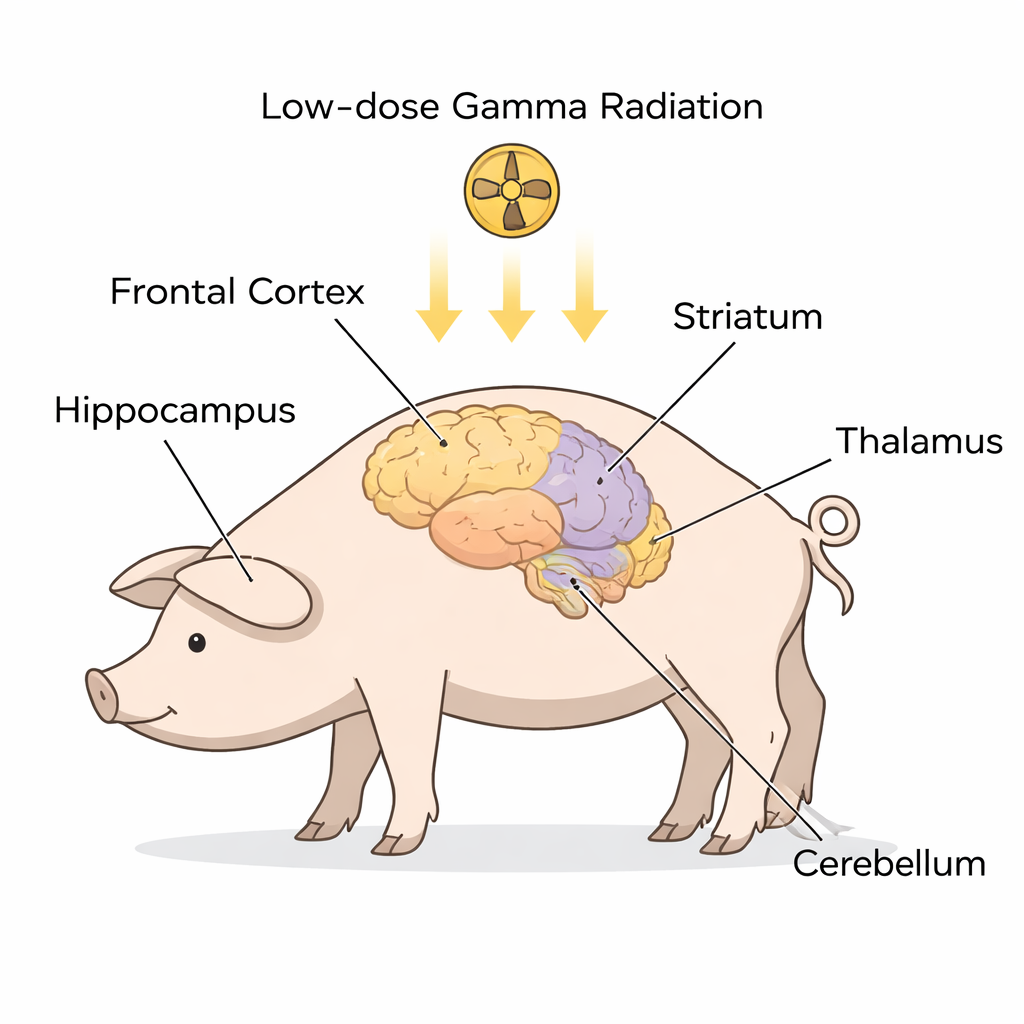
Внимательнее к предвестникам БАС в мозге
Вместо того чтобы изучать пациентов с уже развившимся БАС, исследователи работали со здоровыми гёттингенскими мини‑свиньями, чьи мозги анатомически похожи на наши. Девяти животным однократно провели тотальное облучение низкой дозой гамма‑излучения, тогда как шесть животных были анестезированы, но не облучены и служили контрольной группой. Примерно через месяц учёные выделили пять ключевых областей мозга, часто вовлекаемых при БАС и ФТД — фронтальную кору, гиппокамп, стриатум, таламус/гипоталамус и мозжечок. В каждой области они разделили содержимое клеток на два основных компартмента: цитоплазму (жидкую внутренность клетки) и ядро (компартмент, содержащий ДНК). С помощью метода вестерн‑блоттинга они измерили уровни нескольких белков, тесно связанных с БАС и БАС‑ФТД, включая SOD1, FUS, C9orf72, STMN2, убиквитин, TDP‑43 и модифицированную форму — фосфорилированный TDP‑43.
Радиация оставляет некоторые маркеры без изменений — другие смещает
Одно обнадёживающее наблюдение заключалось в том, что суммарные уровни SOD1, белка, мутации которого вызывают часть наследственных форм БАС, не изменились ни в одной области после облучения. Аналогично, основные формы TDP‑43 — белка, чаще всего обнаруживаемого в характерных мозговых агрегатах при БАС — оставались стабильными как в ядре, так и в цитоплазме во всех областях. Но не всё оставалось неизменным. Команда отметила регионально‑ и компартмент‑специфические сдвиги в ряде других белков. Так, FUS — белок, обычно локализованный в ядре, но способный при БАС неправильно распределяться и образовывать агрегаты — уменьшился в цитоплазме таламуса/гипоталамуса после облучения, в то время как его уровни в ядре возросли во фронтальной коре и упали в гиппокампе. Белок, связанный с БАС, C9orf72 не изменялся в клеточной жидкости, но показал снижение внутри ядер гиппокампа. STMN2, белок, важный для поддержки нервных волокон, также уменьшился в гиппокампальных ядрах, что намекает на согласованную реакцию между этими двумя молекулами в регионе, связанном с памятью.
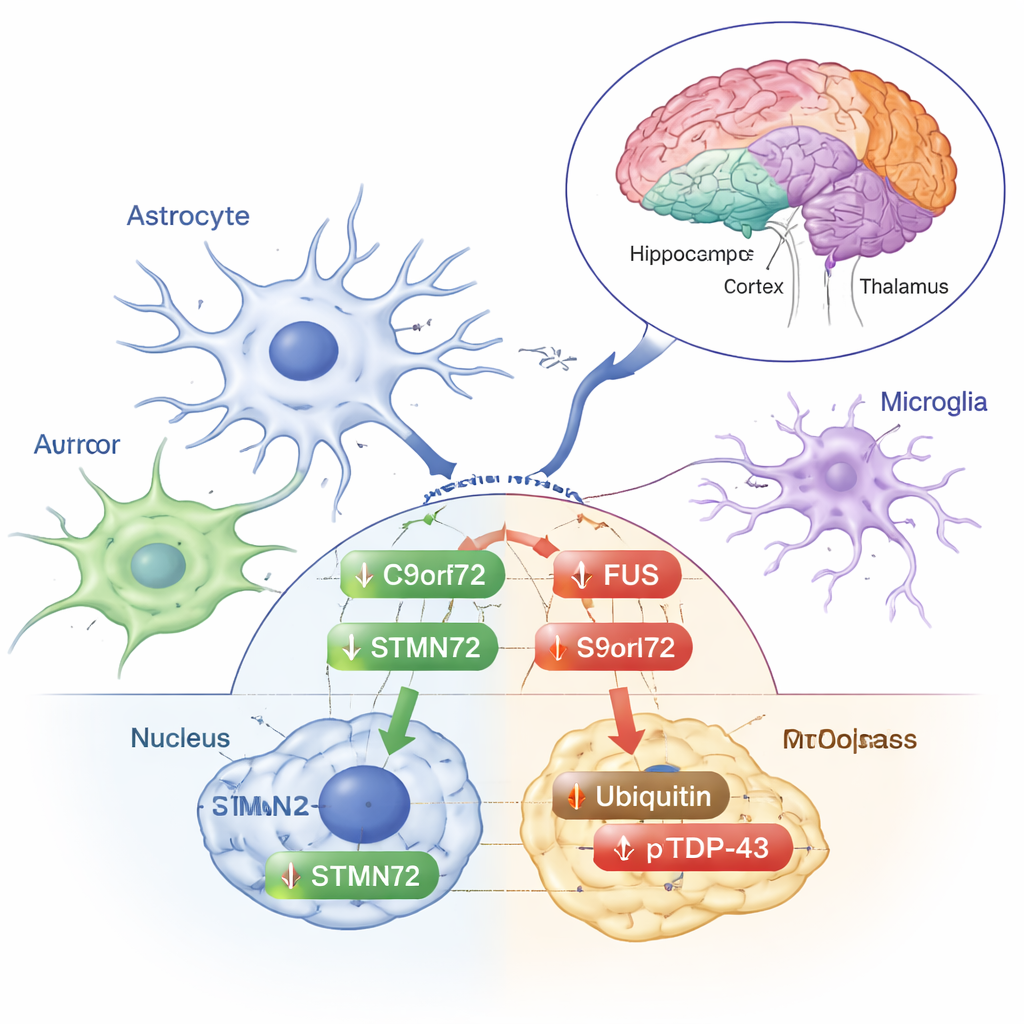
Сигналы стресса или ранняя защита?
Другие изменения больше походили на классические стресс‑ответы. Убиквитин — маленькая метка, которую клетка использует для пометки повреждённых белков с целью их утилизации — увеличился в цитоплазматической фракции фронтальной коры. Фосфорилированная форма TDP‑43, часто обогащённая в аномальных отложениях при БАС и ФТД, повысилась в цитоплазме фронтальной коры, стриатума и таламуса/гипоталамуса, хотя общий TDP‑43 оставался неизменным. Эти сдвиги указывают на то, что низкодозовая радиация подталкивает систему обработки белков мозга, не вызывая при этом полного развития типов неправильного сворачивания и агрегации, определяющих болезнь. Авторы подчёркивают, что эти реакции различаются по областям мозга и по локализации белка внутри или вне ядра, что подчёркивает тонкую настройку реакции мозга на стресс.
Что это может означать для риска БАС — и возможных преимуществ
Означает ли это, что низкодозовая радиация вызывает БАС? Данные скорее против простого «да». Исследователи не выявили характерной для болезни миграции белков или их накопления, а многие изменения указывают на модификацию регуляции, а не на прямое повреждение. Любопытно, что эти результаты согласуются с более ранними работами той же группы и других исследователей, показывающими, что небольшие дозы радиации иногда могут вызывать «гормезис» — феномен, при котором лёгкий стресс активирует пути ремонта и снижает вредные белки, например связанные с болезнью Альцгеймера или Паркинсона, в модельных животных. Текущее исследование намекает, что по крайней мере в краткосрочной перспективе одна низкая доза гамма‑излучения перестраивает маркеры, связанные с БАС, скорее в адаптивном, чем в разрушающем направлении.
Крупные вопросы и осторожная надежда
Для неспециалистов основной вывод таков: связь между радиацией и здоровьем мозга более нюансирована, чем «всякая радиация вредна». В этой модели крупного животного низкодозовое гамма‑облучение вызвало тонкие, регионально‑специфические сдвиги в белках, связанных с БАС и ФТД, не воспроизведя при этом паттерны повреждения, наблюдаемые в мозге пациентов. Эти изменения могут отражать попытки мозга справиться со стрессом и восстановить повреждения, и в ряде случаев даже оказаться полезными. Однако исследование рассматривало только период в один месяц после единственной экспозиции и только мозг (не спинной мозг, где БАС наносит наибольший ущерб). Необходимы долгосрочные исследования и исследования с повторными дозами, прежде чем такие выводы можно будет переносить на людей. Тем не менее работа открывает новое окно в понимание того, как радиация уровней повседневной жизни взаимодействует с молекулами, лежащими в основе разрушительных нейродегенеративных заболеваний, и ставит вопрос о том, могут ли в контролируемых условиях малые дозы однажды быть использованы для стимулирования собственных защитных механизмов мозга.
Цитирование: Iacono, D., Murphy, E.K., Perl, D.P. et al. γ-Radiation induces region-specific subcellular alterations of amyotrophic lateral sclerosis and frontotemporal dementia markers in swine brain. Sci Rep 16, 5627 (2026). https://doi.org/10.1038/s41598-026-36208-8
Ключевые слова: боковой амиотрофический склероз, фронтотемпоральная деменция, низкодозовая радиация, белки мозга, модель мини‑свиньи