Clear Sky Science · ru
Цитоплазматический TDP-43 вызывает ранние поведенческие нарушения без нейродегенерации в модели C. elegans с селективным поражением серотонинергических нейронов
Почему маленькие черви важны для изучения больших заболеваний мозга
Такие состояния, как боковой амиотрофический склероз (БАС) и фронтотемпоральная деменция (ФТД), постепенно лишают людей движения, речи и личности. Главный подозреваемый в этих болезнях — белок TDP-43, который образует скопления в неправильном месте внутри нервных клеток. В этом исследовании используется крошечный червь Caenorhabditis elegans, чтобы наблюдать вживую, что происходит, когда TDP-43 покидает своё обычное место и попадает в цитоплазму. Сфокусировавшись на небольшой, хорошо изученной группе серотонин-продуцирующих нейронов, авторы показывают, как поведение нарушается задолго до видимой гибели нейронов — открывая окно к ранним, наиболее потенциально излечимым стадиям болезни. 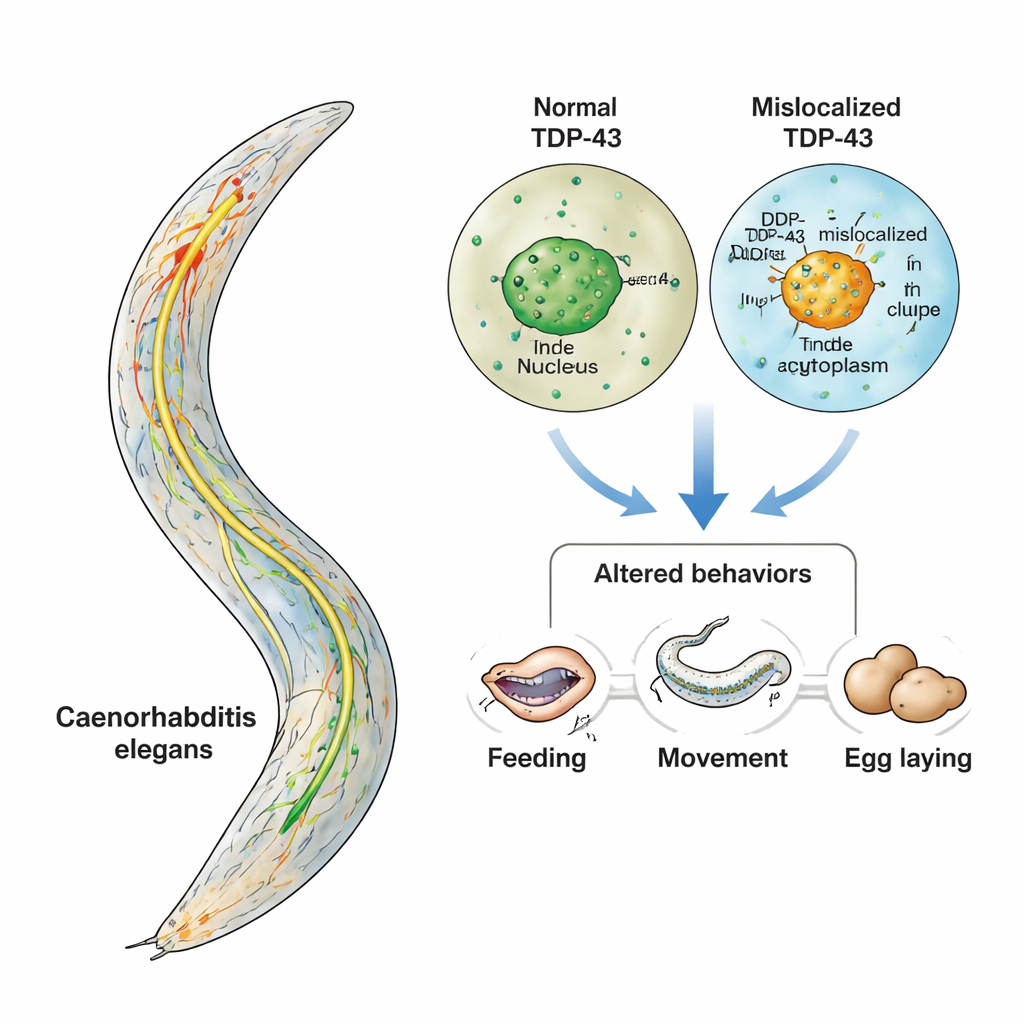
Склеивающийся белок и химический мессенджер
В норме TDP-43 находится в ядре и участвует в управлении РНК, рабочими копиями генетических инструкций клетки. Однако при БАС и ФТД TDP-43 часто покидает ядро, накапливается в цитоплазме и образует липкие агрегаты. Параллельно данные от пациентов и мышиных моделей указывают на то, что серотонин — нейромедиатор, более известный по своей роли в настроении — также нарушен при этих заболеваниях. Поскольку серотонин влияет на множество поведенческих функций — от кормления до управления движением — авторы задали конкретный вопрос: если TDP-43 неправильно локализован именно в серотонинергических нейронах, нарушается ли их работа таким образом, что изменяется поведение даже до дегенерации?
Перестройка простой нервной системы
Исследователи обратились к C. elegans — микроскопическому червю, у которого вся нервная система из 302 нейронов была тщательно картирована. Только три пары этих нейронов синтезируют серотонин, и каждая пара контролирует чётко определённое поведение: кормление (фазовый насос), замедление при обнаружении пищи и откладывание яиц. С помощью генетических инструментов учёные создали червей, у которых только эти серотонинергические нейроны продуцировали человеческий TDP-43. Одна линия синтезировала нормальную, ядерно-локализованную форму; другая — мутантную версию без «адресной метки» для ядра, что заставляло TDP-43 накапливаться в цитоплазме. Поскольку все остальные нейроны оставались не затронутыми, любые поведенческие изменения можно было напрямую связать с нарушениями в этой одной, небольшой цепи.
Поведение нарушается прежде, чем нейроны умирают
В ряде тестов изменённые черви вели себя ненормально по образцу частичной или сильной потери серотонина. Черви с цитоплазматической формой TDP-43 демонстрировали замедление ритмики кормления, слабее замедлялись при встрече с пищей после голодания и реже откладывали яйца. Черви, экспрессирующие нормальную, ядерную форму TDP-43, тоже показали ухудшение по сравнению с немодифицированными животными, но не так выраженное, как у тех, у кого TDP-43 находился в цитоплазме, что выявляет чёткую градацию нарушений. Важно, что в тесте в контексте, где серотонин не нужен — плавание в жидкости — их перемещение было нормальным. Это показало, что базовый локомоторный аппарат оставался неповреждённым, а дефекты были специфичны для серотонин-зависимых поведений, а не отражали общий упадок здоровья. 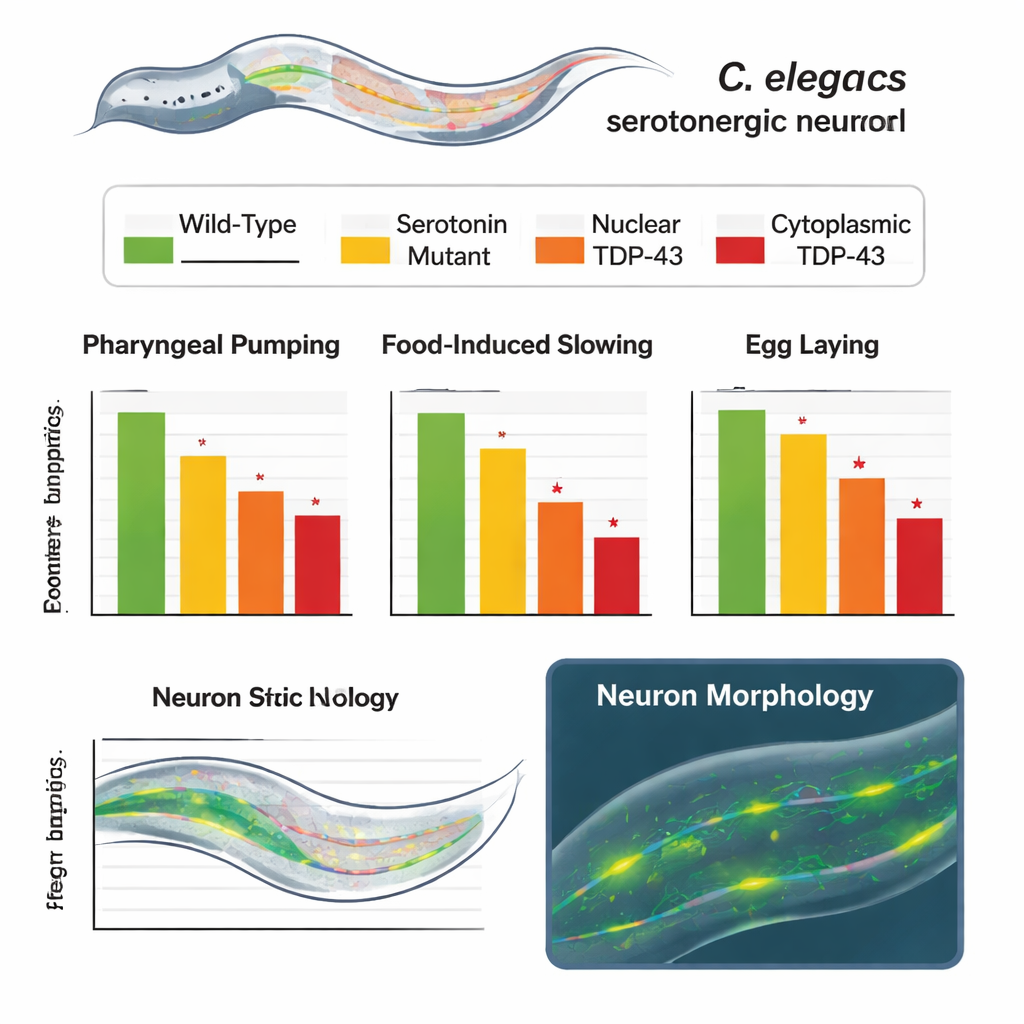
Скрытый ущерб выявлен тестом с препаратом
Чтобы понять, оставались ли затронутые нейроны живыми и функциональными, исследователи использовали флуоксетин, более известный как Прозак — препарат, усиливающий серотонинергическую передачу. У нормальных червей флуоксетин резко повышал частоту откладывания яиц. У генетически модифицированных червей препарат также увеличивал яйцекладку, но ответ был приглушён — особенно у тех, у кого TDP-43 находился в цитоплазме. Этот паттерн указывает на то, что серотонинергические нейроны всё ещё могли высвобождать сигналы, но делали это менее эффективно. Микроскопическая визуализация показала аналогичную картину: серотонин-продуцирующие нейроны выглядели структурно нормальными, без потерь тел клеток или крупных деформаций их ветвей, а их общая флуоресценция — прокси показателя здоровья клеток — соответствовала контролю.
Ранние предупреждающие знаки и новые возможности
В сумме результаты рисуют картину, в которой смещение TDP-43 нарушает работу серотонин-нейронов, оставляя их внешне невредимыми. У червей поведение нарушается — кормление, адаптация движений и размножение — ещё до появления видимой гибели нейронов. Это созвучно клиническим наблюдениям, что тонкие поведенческие и эмоциональные изменения часто предшествуют явной атрофии мозга при нейродегенеративных заболеваниях у людей. Предоставляя простую, генетически контролируемую систему, в которой ранние, специфичные для цепи дефекты можно точно измерить, эта модель червя может помочь исследователям понять, как TDP-43 нарушает работу нейронов, и протестировать терапии, направленные на спасение нейронов в уязвимом пре- дегенеративном окне.
Цитирование: Lacour, A., Vassallu, F., Romussi, S. et al. Cytoplasmic TDP-43 leads to early behavioral impairments without neurodegeneration in a serotonergic neuron-specific C. elegans model. Sci Rep 16, 6068 (2026). https://doi.org/10.1038/s41598-026-36138-5
Ключевые слова: TDP-43, серотониновые нейроны, C. elegans, БАС и ФТД, нейродегенерация