Clear Sky Science · ru
Комплексная оценка генотоксичности, вызванной золотыми наностержнями, с использованием многомодельных биологических систем
Почему крошечные золотые стержни важны для нашей ДНК
Золото может ассоциироваться с ювелирными изделиями или финансами, но в современной медицине его также формуют в крошечные стержни, в тысячи раз тоньше человеческого волоса. Эти «золотые наностержни» помогают врачам лучше видеть опухоли, нагревать и уничтожать раковые клетки и доставлять препараты с высокой точностью. Однако те же необычные свойства, которые делают эти частицы столь эффективными, порождают важный вопрос: повреждают ли они генетический материал внутри наших клеток? В этом исследовании дается широкий обзор взаимодействия золотых наностержней с ДНК на примере бактерий, дрожжей и человеческих печеночных раковых клеток, чтобы понять, что это может означать для медицинских методов и правил безопасности. 
От пробирок к живым клеткам
Чтобы изучить риски и пользу золотых наностержней, исследователи сначала приготовили однородные частицы в форме стержней длиной около 50 нанометров — слишком маленькие, чтобы видеть невооруженным глазом, но легко проникающие в клетки. Затем они протестировали эти частицы в нескольких биологических системах, которые вместе образуют своего рода «конвейер токсичности». Две распространенные бактерии, Salmonella typhimurium и Escherichia coli, использовали как быстрые и простые датчики повреждений ДНК. Специально сконструированные штаммы дрожжей, у каждого из которых отсутствовал один ген, связанный с реакцией на стресс или программируемой гибелью, дали более «человеко-подобную» модель, поскольку дрожжи разделяют с нами многие фундаментальные пути. Наконец, человеческие печеночные раковые клетки (HepG2), широко используемые для тестирования лекарств и химических веществ, подвергались воздействию золотых наностержней, чтобы команда могла отслеживать изменения в ключевых генах, связанных с раком.
Наблюдая, как ДНК рвется в кометные хвосты
В бактериях и дрожжах ученые использовали чувствительный метод, называемый кометным анализом, чтобы «увидеть» повреждение ДНК по отдельным клеткам. В этом методе клетки внедряют в гель, осторожно разрушают оболочки и помещают в электрическое поле. Неповрежденная ДНК в основном остается на месте, а разорванные нитки вытягиваются, образуя форму, напоминающую комету с яркой головкой и хвостом. По длине и интенсивности хвоста исследователи оценивают степень генетического повреждения. В Salmonella и E. coli золотые наностержни вызывали явные дозозависимые изменения во всех параметрах кометы: больше клеток с хвостами, длиннее хвосты и большая доля ДНК, вытянутая в хвост. Штаммы дрожжей с нокаутированными генами показали ту же картину: некоторые штаммы — особенно лишенные генов, связанных со стрессом и митохондриальной функцией — демонстрировали заметно большее фрагментирование ДНК по сравнению с нормальными дрожжами. 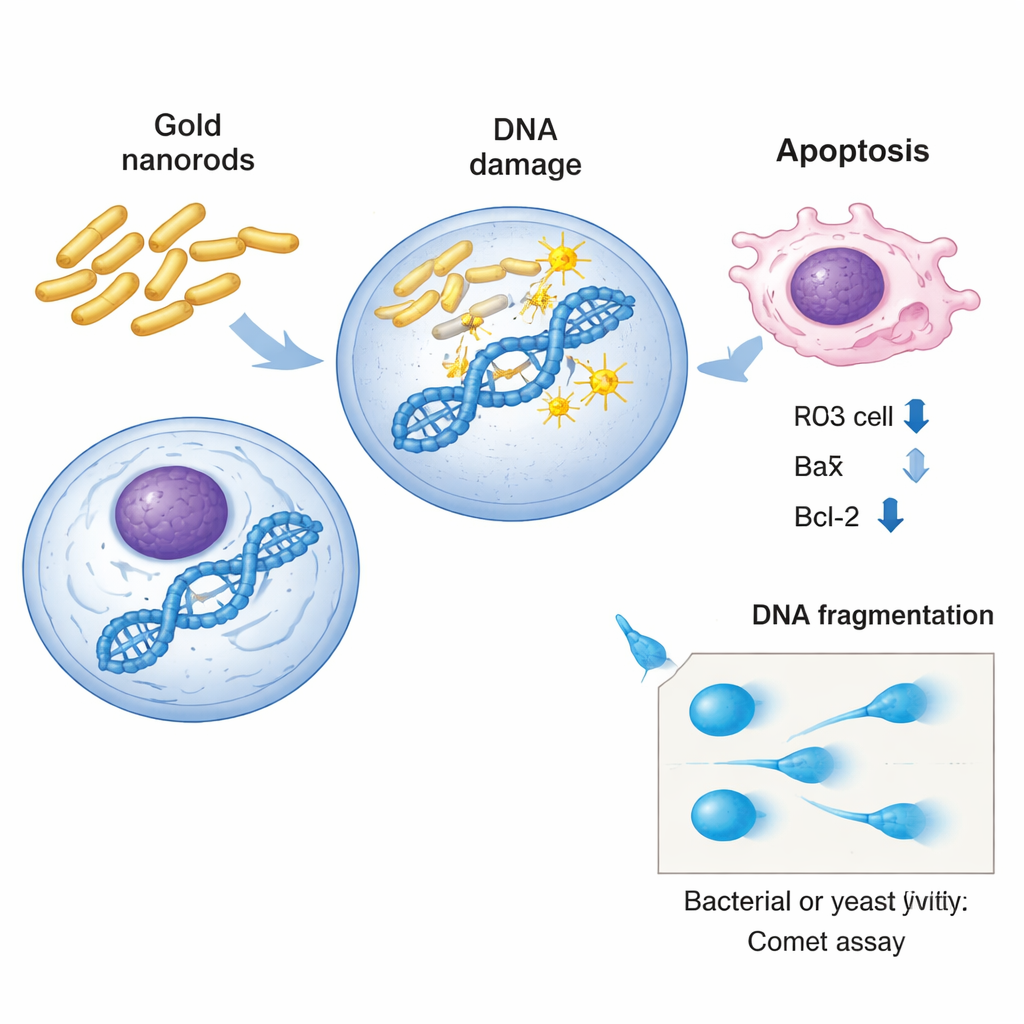
Генные сети и сигналы смерти в человеческих клетках
В человеческих печеночных клетках команда пошла глубже: помимо физических разрывов ДНК они изучали, как реагируют внутренние системы контроля клеточного состояния. С помощью количественной ПЦР в реальном времени измеряли активность трех хорошо известных стражей и исполнителей судьбы клетки: p53 и Bax, которые стимулируют гибель клетки при обнаружении повреждений, и Bcl-2, способствующий выживанию. После воздействия полудоз токсичных концентраций золотых наностержней уровни p53 и Bax возросли, а Bcl-2 снизился — молекулярный знак программируемой клеточной гибели (апоптоза). Иными словами, наностержни не только повреждали ДНК, но и сдвигали раковые клетки в сторону самоуничтожения. Чтобы связать результаты дрожжей с биологией человека, исследователи использовали платформу GeneMANIA для построения сетей взаимодействий вокруг удаленных дрожжевых генов. Этот анализ показал плотные сети физических и генетических взаимодействий, связанные с реакцией на стресс, репарацией ДНК и митохондриальной функцией, что усиливает идею о том, что одни и те же типы путей уязвимы и у дрожжей, и у человеческих клеток.
Баланс между медицинскими перспективами и генетическим риском
В совокупности эти эксперименты дают нюансированную картину золотых наностержней. С одной стороны, они явно могут повредить ДНК у очень разных организмов, и масштаб повреждений растет с увеличением дозы. Определенные генетические фоны, например штаммы дрожжей, лишенные специфических генов стресса или митохондриальной функции, особенно чувствительны, что намекает на то, что люди с определенными генетическими особенностями тоже могут реагировать иначе. С другой стороны, в человеческих печеночных раковых клетках это повреждение ДНК и последующая активация путей смерти могут быть как раз тем, чего желают врачи при нацеливании на опухоль. Для неспециалиста ключевое послание таково: золотые наностержни — мощный инструмент, который может и помогать, и вредить: они способны уничтожать раковые клетки, но также представляют генетические риски для других клеток и окружающей среды. Авторы работы делают вывод, что при будущем медицинском применении этих частиц необходимо тщательно взвешивать дозировку, направленную доставку и генетические особенности пациентов, чтобы использовать их преимущества и одновременно строго контролировать генотоксический потенциал.
Цитирование: Rashad, S.E., Haggran, A.A. & Abdoon, A.S.S. Comprehensive assessment of gold nanorod-induced genotoxicity using multi-model biological systems. Sci Rep 16, 5429 (2026). https://doi.org/10.1038/s41598-026-36119-8
Ключевые слова: золотые наностержни, повреждение ДНК, нанотоксикология, терапия рака, тестирование генотоксичности