Clear Sky Science · ru
Позиции R5 и R7 на фторхинолоновых остовах определяют разрушение филаментов F-актина
Превращение антибиотиков в помощников мозга
Многие распространённые заболевания мозга, от болезни Альцгеймера до болезни Паркинсона, имеют скрытого виновника: миниатюрные структурные стержни внутри нейронов, которые со временем застревают и становятся жёсткими. Эти стержни состоят из белка актин, который в норме — гибкая часть внутреннего каркаса клетки. В этом исследовании рассматривается неожиданная возможность — что хорошо известный класс антибиотиков, фторхинолоны, можно переработать так, чтобы они мягко разрушали эти вредные пучки актина и потенциально защищали мозг.
Когда клеточный каркас даёт сбой
Здоровые клетки мозга постоянно перестраивают свой внутренний скелет для образования и реорганизации связей. Филаменты актина центральны в этом процессе, они формируются и распадаются по мере необходимости. При стрессе актин может зафиксироваться в упрямых стержнеобразных агрегатах, которые загромождают клетку, нарушают транспорт жизненно важных грузов и способствуют накоплению белков, связанных с болезнью, таких как амилоид и тау. Со временем эти стержни могут созревать в плотные структуры, известные как тела Хирано, которые часто наблюдаются в мозге людей с рядом нейродегенеративных состояний. Поскольку существующие препараты, нацеленные на актин, часто чрезвычайно токсичны, исследователи стремятся найти более безопасные малые молекулы, способные ослабить эти агрегаты, не повреждая клетки.
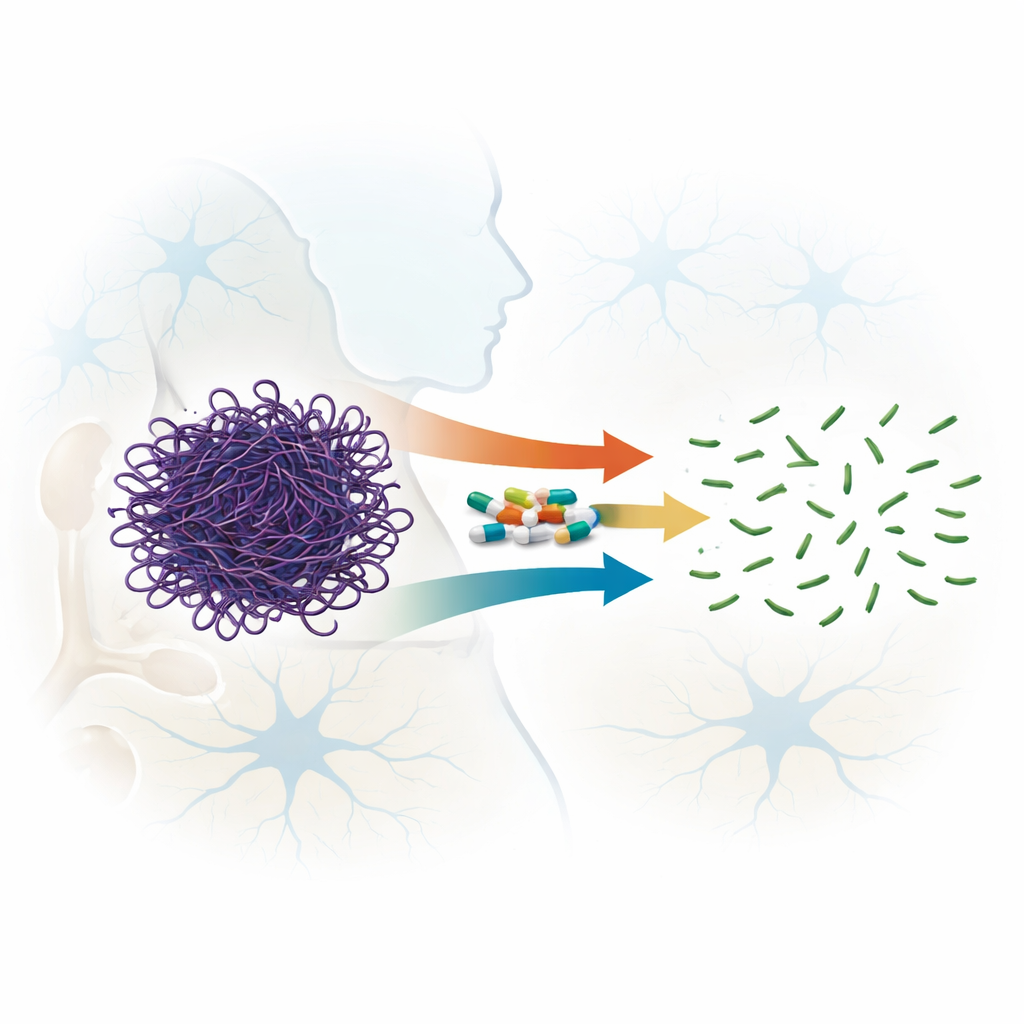
Неожиданный талант знакомых препаратов
Фторхинолоны — это антибиотики широкого спектра действия, используемые во всём мире для лечения инфекций, и некоторые современные представители этого семейства способны проникать через гематоэнцефалический барьер. Ранние данные подсказывали, что определённые фторхинолоны могут дестабилизировать филаменты актина. В этой работе авторы систематически сравнили семь родственных соединений, охватывающих четыре поколения препаратов, чтобы оценить, насколько эффективно они расщепляют уже сформированные филаменты актина, а не просто препятствуют их образованию. С помощью измерений рассеяния света, электронной микроскопии и гелевой фильтрации они показали, что все протестированные препараты способны нарушать филаменты актина, но с очень разной эффективностью. Два препарата — спарфлоксацин (третье поколение) и моксифлоксацин (четвёртое поколение) — выделялись тем, что быстро и необратимо дробили длинные филаменты на гораздо меньшие фрагменты даже при относительно низких соотношениях препарата и белка.
Наблюдая за распадом филаментов
Высокодетализированная визуализация и биофизические тесты показали, как филаменты меняются под действием препаратов. Электронная микроскопия продемонстрировала, что необработанный актин образует длинные непрерывные нити, тогда как эффективные фторхинолоны превращают их в короткие разрозненные фрагменты. Менее мощные члены группы вызывали образование согнутых и изломанных нитей, но не полное их разрушение. Измерения тепловой стабильности белка подтвердили это физическое разрушение: после обработки актин вел себя больше похоже на свою свободную, несобранную форму с пониженными температурами плавления, при этом его базовая структура строительного блока оставалась практически неизменной. Это указывает на то, что препараты не разворачивают и не повреждают сам актин — они главным образом разъединяют способ, которым единицы сцепляются в филаменты.
Приближая молекулярный захват
Чтобы понять, почему некоторые фторхинолоны работают лучше других, команда объединила продвинутые эксперименты ядерного магнитного резонанса с компьютерными моделями взаимодействий препарата и белка. Они обнаружили, что все соединения опираются на общий кольцевой «ядро», которое контактирует с актином, особенно в двух позициях на этом ядре, которые неоднократно взаимодействуют с филаментом. Однако дополнительные химические группы, прикреплённые в специфических местах — обозначенных как R5 и R7 — сильно влияют на то, насколько прочно и в каких точках каждая молекула связывается. У наиболее эффективных разрушителей эти позиции несут аминогруппу и объёмные колечные системы, которые проникают в небольшую карманную область на интерфейсе между соседними актиновыми нитями. Там они мешают ключевым стабилизирующим контактам, включая важный сольный мост, который обычно помогает удерживать филаменты вместе.
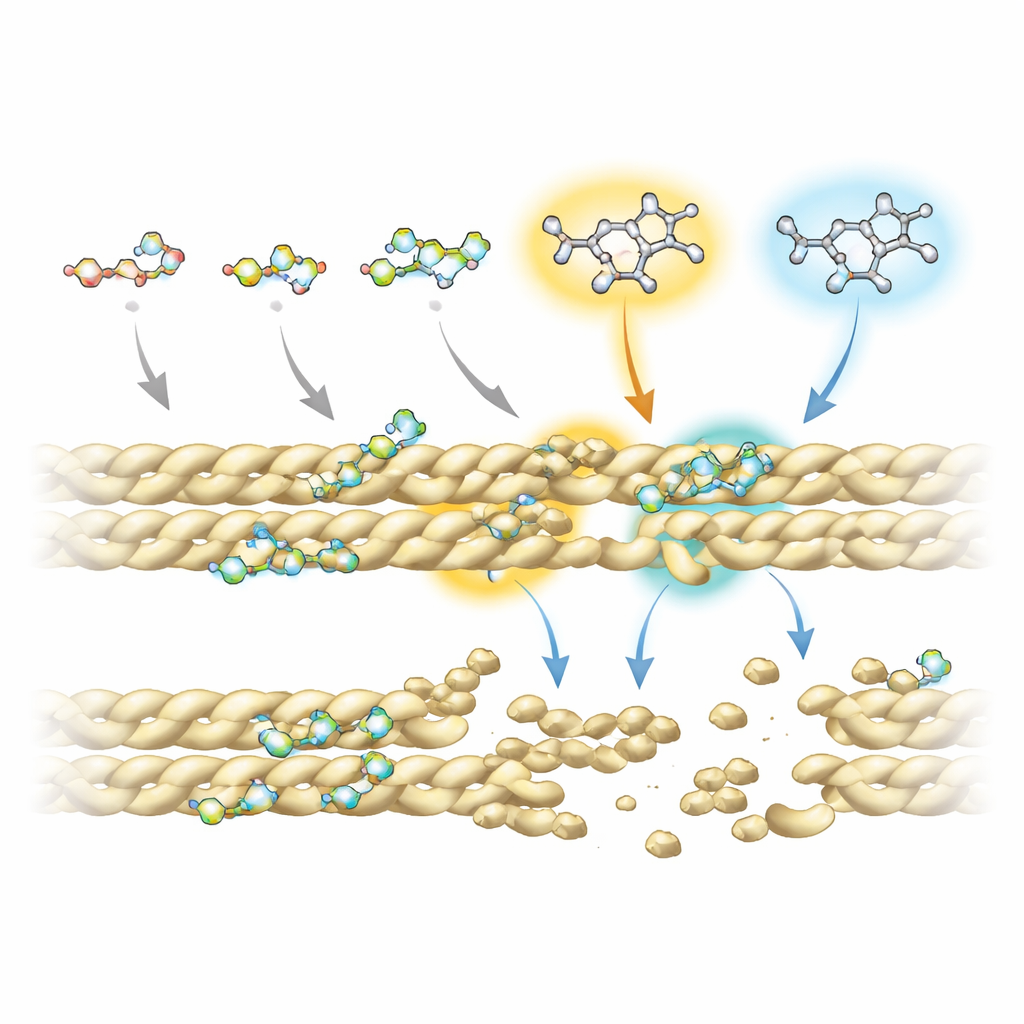
От дрожжевых клеток к будущим терапиям
Исследователи также проверили препараты в штамме дрожжей, который естественным образом накапливает пучки актина, моделируя некоторые аспекты патологических клеток. Под микроскопом необработанные дрожжи показывали большие яркие скопления актина, тогда как клетки, обработанные фторхинолонами — особенно спарфлоксацином, моксифлоксацином и, при более высоких дозах, налидиксовой кислотой — демонстрировали значительно более рассеянные, пунктирные узоры, что указывало на разрушение пучков. Важно, что действие препаратов казалось относительно мягким: они ослабляли укладку филаментов без грубого искажения базовой формы актина, и их связывание было слабее, чем у классических токсинов актина, что потенциально снижает риск серьёзных побочных эффектов.
Проектирование более умных препаратов, нацеленных на актин
В целом это исследование показывает, что незначительные изменения в структуре хорошо известных антибиотиков могут кардинально изменить их взаимодействие с внутренним каркасом клетки. Указав позиции R5 и R7 в качестве ключевых «регуляторов» как для разрушения актина, так и для проникновения в мозг, авторы намечают план создания новых молекул, вдохновлённых фторхинолонами, которые селективно разрушают вредные агрегаты актина. Хотя эти результаты представляют собой раннее лабораторное доказательство принципа, они дают надежду на то, что будущие препараты, производные от знакомых антибиотиков, смогут очищать токсичный каркас в нейронах и замедлять или предотвращать некоторые формы нейродегенерации.
Цитирование: Gupta, R.J., Nair, H., Sarhadi, T.R. et al. R5 and R7 positions on fluoroquinolone scaffolds drive F-actin filament disruption. Sci Rep 16, 9517 (2026). https://doi.org/10.1038/s41598-026-36089-x
Ключевые слова: агрегаты актина, фторхинолоновые антибиотики, нейродегенеративные заболевания, переназначение препаратов, цитоскелет