Clear Sky Science · ru
Экспрессия ACE2 в эпителиальных клетках толстой кишки связана с вирусной инфекцией, иммунитетом и энергетическим метаболизмом
Почему кишечник важен при респираторном вирусе
Когда мы думаем о COVID-19, перед глазами чаще возникают легкие, наполненные жидкостью, и люди, которым трудно дышать. Тем не менее у многих пациентов с инфекцией SARS-CoV-2 появляются также боли в животе, диарея и длительные проблемы с кишечником. В этом исследовании объясняется, почему кишечник — особенно толстая кишка — может быть важной мишенью для вируса. Исследователи, внимательно изучив отдельные клетки из детских биопсий толстой кишки, показывают, что ключевая «дверь» для вируса, белок ACE2, сильно активна в определенных кишечных клетках и связана не только с вирусной инфекцией, но и с иммунной защитой и способностью клеток управлять энергией.
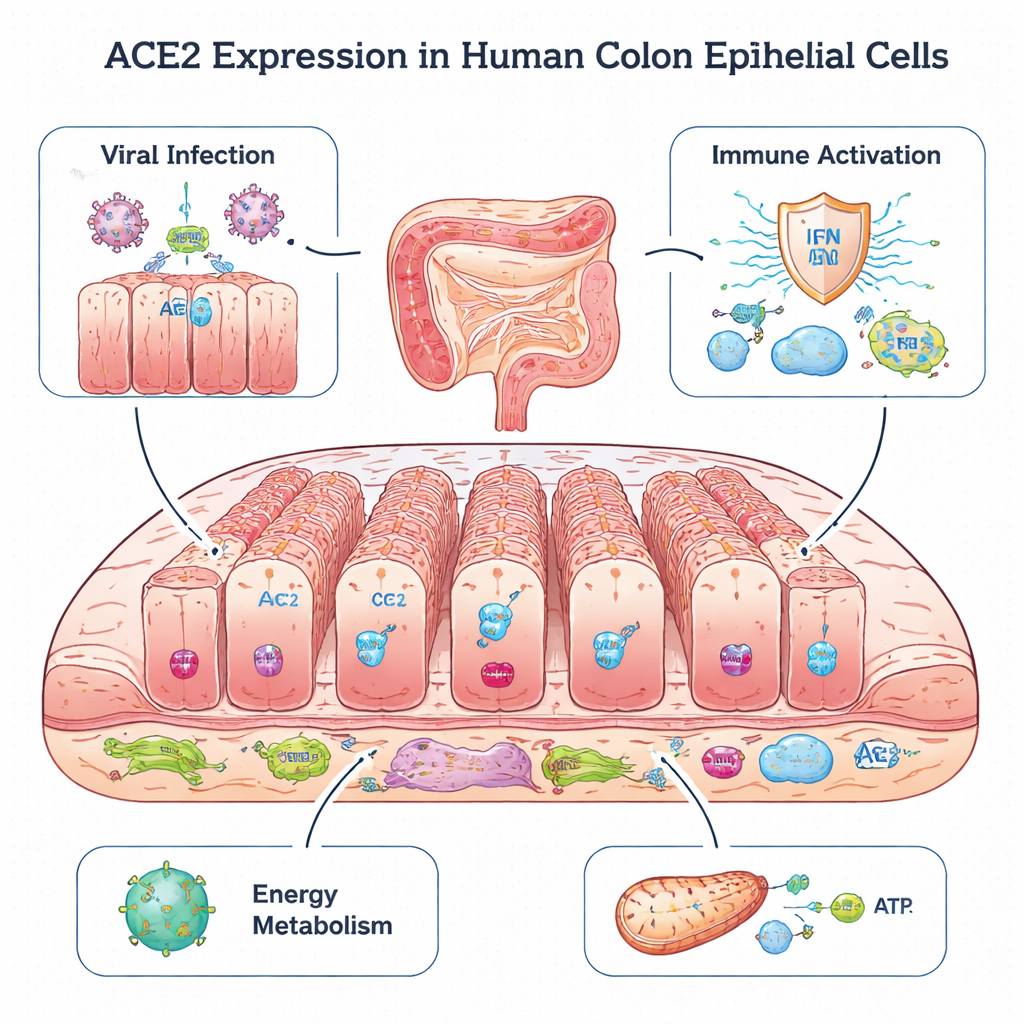
Клеточная «дверь» в толстой кишке
ACE2 прежде всего известен как основной входной путь, который использовали и оригинальный вирус SARS, и SARS‑CoV‑2 для заражения клеток легких. Парадоксально, но исследования на животных показывают, что ACE2 также может защищать ткани от повреждений, помогая поддерживать в равновесии гормональную систему, контролирующую кровяное давление. В кишечнике ACE2 уже связывали с поддержанием здоровой микробиоты и предотвращением воспаления. В данной работе ученые повторно проанализировали данные одиночноклеточного секвенирования РНК (single-cell RNA-seq) из биопсий толстой кишки 17 детей: у некоторых кишечник был здоров, у других — колит или воспалительное заболевание кишечника, включая язвенный колит и болезнь Крона. Этот метод позволил им увидеть, какие гены активны в тысячах отдельных клеток, и точно определить, где включен ACE2.
Колоноциты: первичные цели и первые ответчики
Анализ показал, что ACE2 сосредоточен почти исключительно в колоноцитах — основном типе эпителиальных клеток, выстилающих внутреннюю поверхность толстой кишки и обращенных к её содержимому. По сравнению с другими эпителиальными клетками колоноциты также проявляли более высокую активность генов, которые помогают вирусам проникать в клетки, отщепляться и выходить наружу. Вместе с тем эти клетки экспрессировали множество генов, участвующих в распознавании вирусной генетической информации и запуске интерферонных ответов типов I и III — ключевых ранних сигналов тревоги иммунной защиты. Они также продуцировали провоспалительные сигналы и молекулы, представляющие фрагменты вируса Т‑клеткам, что говорит о том, что колоноциты одновременно являются потенциальными мишенями для вируса и важными ранними часами, оповещающими иммунную систему.
Связанные сети иммунитета и использования энергии
Далее исследователи выясняли, какие еще гены склонны включаться или выключаться синхронно с ACE2 в колоноцитах. Они выявили более 3 400 генов, уровни которых повышались вместе с ACE2, и более 2 100 генов, уровни которых снижались при возрастании ACE2. Гены, положительно коррелирующие с ACE2, были обогащены процессами, связанными с входом и выходом вирусов, сигналингом врожденного иммунитета, клеточной убивающей активностью натуральных киллеров и Т‑клеток, а также несколькими путями клеточного производства энергии, включая функцию митохондрий и обработку жиров и сахаров. В противоположность этому, гены, изменявшиеся в обратном направлении — высокие при низком ACE2 — были связаны с антителозависимым (гуморальным) иммунитетом, системой синтеза белка в клетке, процессами захвата и переработки частиц (фагocytозом) и системой комплемента, другой ветвью иммунной защиты. Эта картина указывает на то, что ACE2 отмечает состояние, при котором колоноциты настроены на быстрое противовирусное распознавание и производство энергии, тогда как другие, более медленные иммунные программы приглушены.
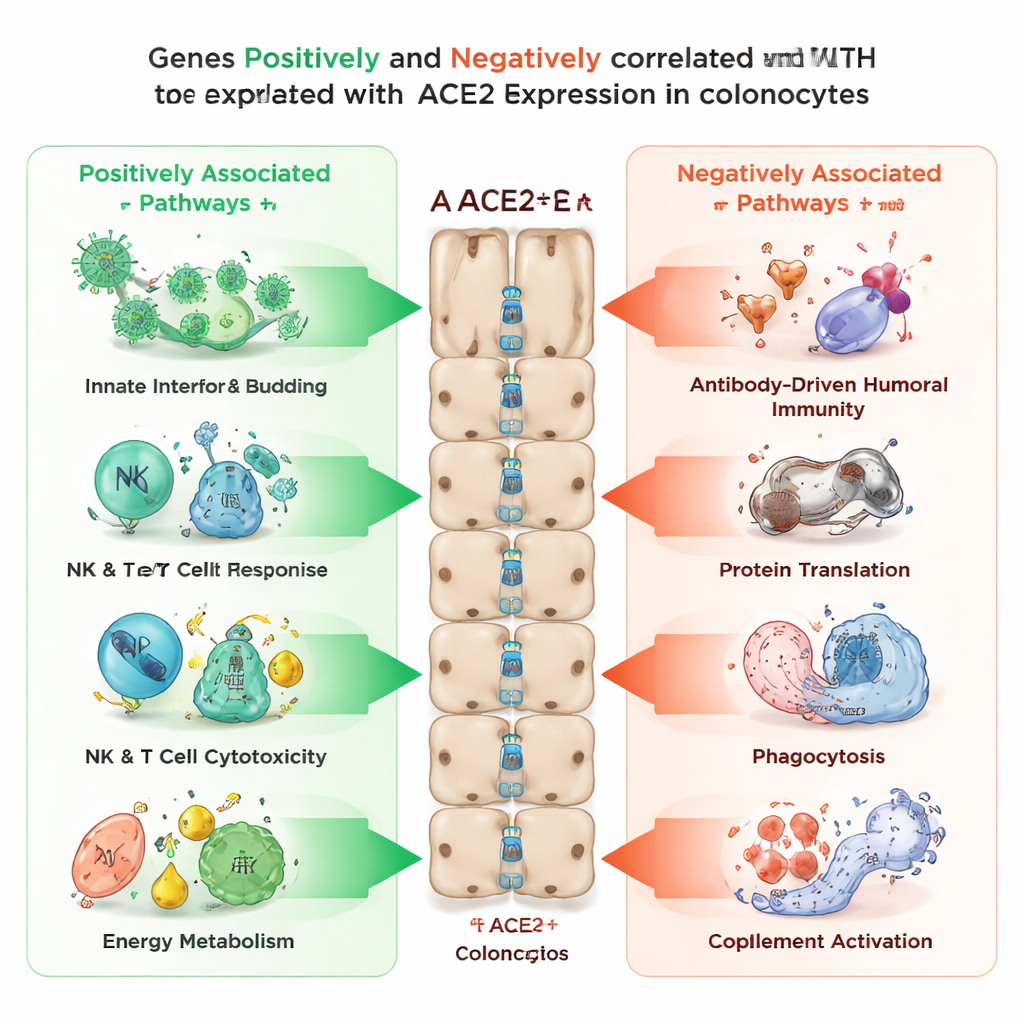
Данные из воспаленных участков кишечника
Чтобы проверить, проявляются ли эти закономерности в реальной ткани, команда использовала мультиплексную иммунофлуоресценцию — метод, который подсвечивает специфические белки разными цветами — на образцах толстой кишки детей с язвенным колитом, болезнью Крона и у контрольной группы. Они подтвердили, что белок ACE2 локализуется преимущественно на эпителиальных клетках, помеченных EPCAM. У пациентов с воспалительными заболеваниями кишечника ACE2‑положительные клетки демонстрировали более высокие уровни IFNA4 и RSAD2, двух белков, тесно связанных с интерферонным сигнальингом и противовирусной активностью. Это указывает на то, что в воспаленном кишечнике колоноциты с ACE2 — не просто возможные ворота для вируса; они также являются очагами противовирусного ответа.
Что это значит для пациентов и будущих терапий
Для непрофессионалов основной вывод таков: толстая кишка далеко не пассивный наблюдатель при COVID‑19. Тот же белок, который позволяет вирусу проникать в клетки, также помогает координировать кишечный иммунитет и энергетический обмен, особенно у детей с предшествующим воспалением кишечника. Эта двойная роль может помочь объяснить, почему у некоторых пациентов развиваются гастроинтестинальные симптомы и почему у людей с воспалительными заболеваниями кишечника исходы при COVID‑19 бывают сложными, но не обязательно однозначно худшими. Работа также вписывается в более широкий контекст обсуждений о препаратах, действующих на свертывание крови и пути регуляции кровяного давления, некоторые из которых могут смягчать повреждение легких и сосудов при тяжелой инфекции. Поскольку исследование опирается на корреляции и не доказывает причинно‑следственные связи, оно тем не менее выделяет клетки толстой кишки, богатые ACE2, как важные узлы на перекрестке вирусного проникновения, иммунной защиты и метаболизма — указывая на кишечник как ключевую и потенциально поддающуюся лечению область при коронавирусной инфекции.
Цитирование: Qi, Y., Huang, Y., Chen, H. et al. ACE2 expression by colonic epithelial cells is associated with viral infection, immunity, and energy metabolism. Sci Rep 16, 5738 (2026). https://doi.org/10.1038/s41598-026-36052-w
Ключевые слова: ACE2, колоноциты, COVID-19 кишечник, воспалительное заболевание кишечника, противовирусный иммунитет