Clear Sky Science · ru
Протеомный анализ секретома эндотелиальных прогениторных клеток выявляет Serpine 1 как мощный регулятор остеогенеза
Исцеление сломанной кости без донорских трансплантатов
Когда кость сильно повреждена или отсутствует кусок, хирургам часто трудно восстановить одновременно и прочность, и форму. Существующие варианты — пересадка кости с другой части тела или использование синтетических трансплантатов — могут быть болезненными, рискованными и не всегда успешными. В этом исследовании рассматривается другая идея: вместо пересадки клеток можно ли доставить лишь правильные природные белки, чтобы включить собственную программу строительства кости организма?
Почему некоторые переломы не заживают
Большинство переломов срастаются самостоятельно, но большие дефекты кости — например, вызванные травмой, опухолями или значительной атрофией челюстной кости — часто этого не делают. В таких случаях организму просто не хватает местных сосудистых клеток и костеобразующих стволовых клеток, чтобы восстановить отсутствующий сегмент. Исследователи в области тканевой инженерии пытаются решить эту проблему, сочетая три составляющих: живые клетки, способные формировать новую кость, каркас, на котором они могут расти, и сигналы, указывающие им, что делать. Трансплантация клеток может работать, но она дорога, строго регулируется и не всегда практична в рутинной клинической практике. Это подтолкнуло учёных к поиску «безклеточных» решений, основанных на умных биоматериалах и тщательно подобранных белках.
Тайные сигналы от сосудообразующих клеток
Эндотелиальные прогениторные клетки — редкие клетки крови, которые помогают формировать новые кровеносные сосуды. Ранее было показано, что при имплантации рядом с костью эти клетки стимулируют заживление — в основном посылая растворимые сигналы, а не превращаясь сами в кость. В новом исследовании авторы собрали жидкую культуру, в которой росли эти клетки, и с помощью современных методов протеомного анализа зарегистрировали сотни секретируемых молекул. Они сосредоточились на восьми белках, тесно связанных с ангиогенезом и остеогенезом. Используя в лаборатории человеческие стволовые клетки костного мозга и человеческие микрососудистые эндотелиальные клетки, они систематически проверяли, какие из этих белков лучше всего стимулируют пролиферацию, направляют миграцию и запускают отложение костеподобного минерала.
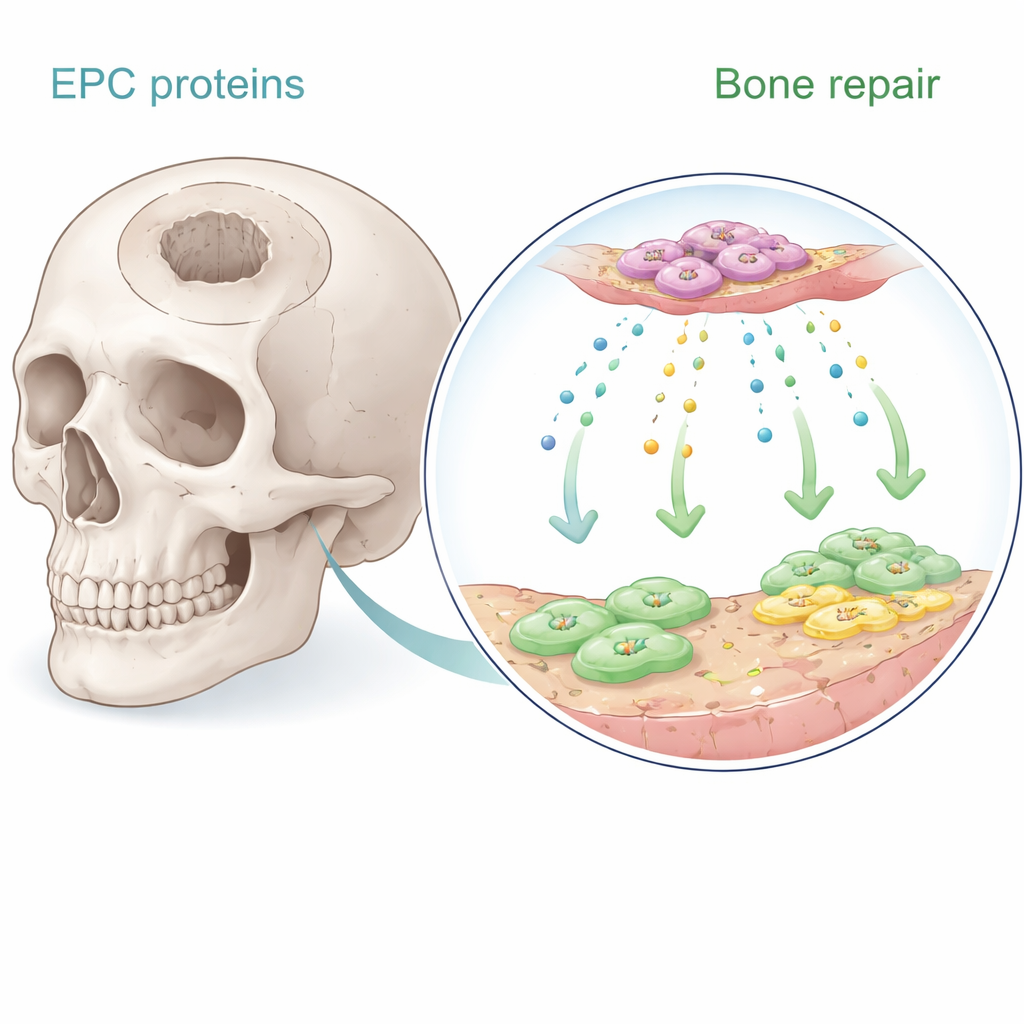
Неожиданный белок выходит на первое место
Среди кандидатов выделился один белок: Serpine-1, более известный по своей роли в регуляции свертывания крови и заживлении ран. В культурах Serpine-1 существенно увеличивал пролиферацию как стволовых клеток костного мозга, так и эндотелиальных клеток в дозозависимой манере, превосходя по этому показателю такие известные факторы роста, как BMP-2 и SDF-1. Он также способствовал созреванию стволовых клеток в остеобласты, что показали классические методы окрашивания, выявляющие активность щелочной фосфатазы и отложения кальцийсодержащего минерала. Другие белки, например фактор роста, производный от тромбоцитов, и BMP-2, были более эффективны в поощрении клеточной миграции в «раневой» зоне в тестах на движение, но Serpine-1 предлагал редкое сочетание стимулирования как численности клеток, так и их костеобразующей активности.
Превращение белка в практический имплантат
Найти перспективный белок — лишь половина задачи; его также нужно доставить в зону повреждения контролируемым способом. Команда инкапсулировала Serpine-1 в крошечные биодеградируемые шарики из медицинского полимера PLGA, затем смешала эти микрошарики с мягким коллагеновым гелем. Получился каркас, который медленно выпускает белок со временем. Они проверили его на мышах, просверлив круглый дефект диаметром 4 мм в черепе — размер дефекта, который сам по себе не заживает. Некоторые дефекты заполняли только коллагеном, некоторые — коллагеном с пустыми микрошариками, а некоторые — каркасом с Serpine-1. Через восемь недель сканы микро-КТ высокой разрешающей способности показали, что в группе с Serpine-1 объем кости, плотность и толщина внутри дефекта были значительно выше. Примечательно, что только у этих животных формировалась новая кость в центре зазора, а не лишь по краям.
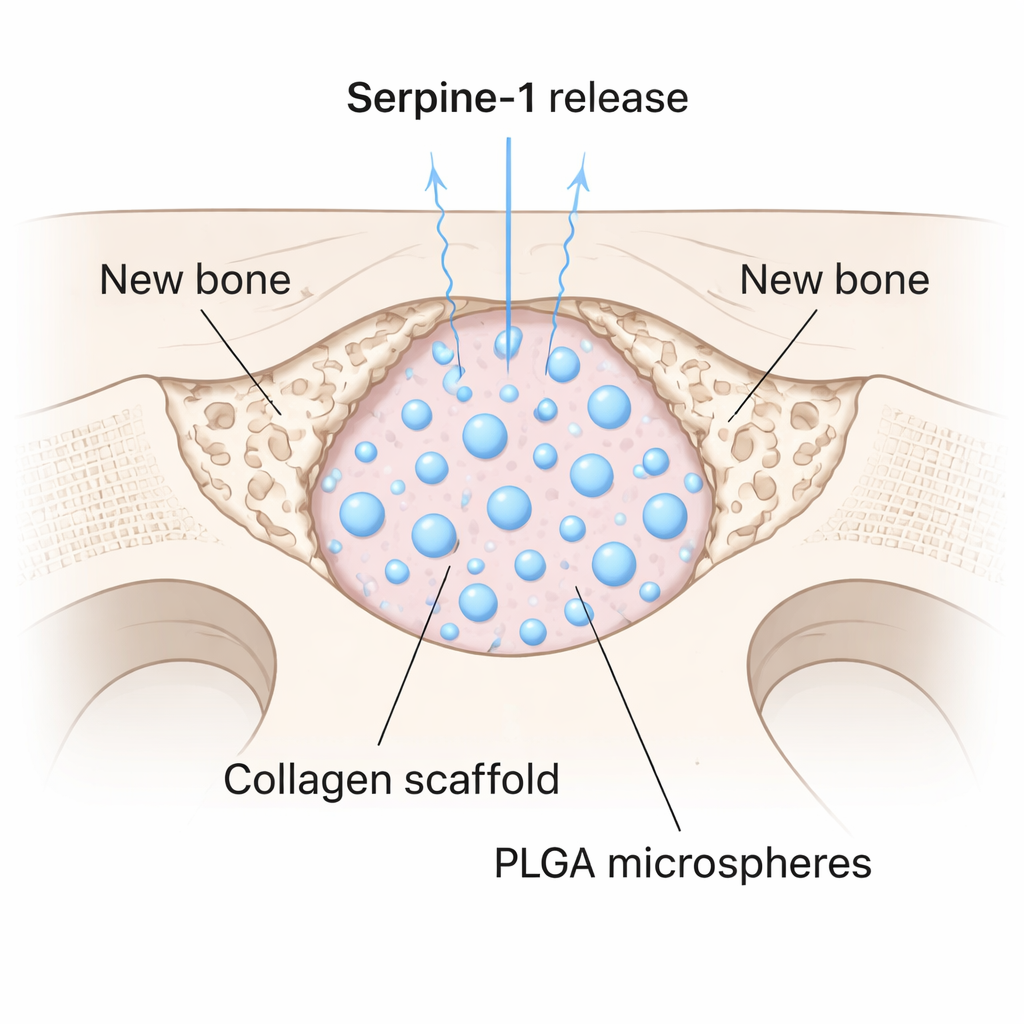
Что это может значить для будущего лечения костей
Исследование вводит Serpine-1 как мощный и ранее недооценённый сигнал для формирования кости. Сочетая этот белок с системой медленного высвобождения, исследователи добились значимого возобновления кости в дефекте, который обычно остаётся пустым. Хотя Serpine-1 не привлекал клетки в дефект так сильно, как некоторые другие факторы, его способность способствовать пролиферации и созреванию существующих клеток предполагает, что его можно комбинировать с белками, стимулирующими миграцию, для ещё лучшего эффекта. Для пациентов такие безклеточные материалы на основе белков в перспективе могут сократить необходимость в заборе собственной кости или опоре на сложные клеточные терапии, предложив более простой способ заставить упрямые костные повреждения наконец зажить.
Цитирование: Asbi, T., Tamari, T., Doppelt-Flikshtain, O. et al. Proteomic analysis of endothelial progenitor cells secretome identifies Serpine 1 as a potent regulator of osteogenesis. Sci Rep 16, 5165 (2026). https://doi.org/10.1038/s41598-026-36048-6
Ключевые слова: регенерация костной ткани, Serpine-1, тканевая инженерия, эндотелиальные прогениторные клетки, коллагеновый каркас