Clear Sky Science · ru
Самообучение на графах предсказывает ассоциации некодирующих РНК и заболеваний
Почему скрытые РНК важны для нашего здоровья
Большинство из нас изучало, что главная роль РНК — помогать в сборке белков. Но за последнее десятилетие учёные обнаружили огромное количество «некодирующих» РНК, которые не превращаются в белки, но при этом регулируют работу клеток. Многие из этих молекул уже признаны факторами, способными стимулировать или подавлять развитие рака и других сложных заболеваний. Выяснение того, какие некодирующие РНК связаны с какими болезнями, может открыть новые пути для ранней диагностики и точечной терапии — но проверять каждую гипотезу в лаборатории было бы слишком медленно. В этом исследовании предложён мощный вычислительный метод, который умеет просеивать огромные биологические сети и надёжно предлагать наиболее перспективные связи между РНК и заболеваниями для дальнейшей проверки в экспериментах.
От «мусора» к ключевым игрокам клетки
В течение многих лет некодирующие РНК считались бессмысленными остатками генетической активности. Сейчас известно, что семейства, такие как микроРНК, длинные некодирующие РНК и циркулярные РНК, участвуют в координации жизненно важных процессов — от упаковки ДНК до включения и выключения генов и передачи сигналов внутри клеток. Поскольку они занимают множество контрольных точек, даже небольшие изменения в этих РНК могут сдвинуть равновесие в сторону рака или других заболеваний. Клиницисты уже рассматривают их как потенциальные биомаркеры и таргеты для лекарств. Главная проблема — масштаб: тысячи различных РНК и сотни заболеваний, а традиционные эксперименты для проверки каждой возможной связи дороги и трудоёмки. Здесь на помощь приходит вычислительное предсказание, которое сужает пространство поиска.
Как «читать» биологическую сеть
Ранние компьютерные методы пытались предсказывать связи РНК и заболеваний, разбивая большие таблицы данных на более простые части или обучая модели машинного обучения на известных примерах. Эти подходы помогали, но часто игнорировали то, как РНК и заболевания переплетены в сети. Современные «графовые нейронные сети» рассматривают РНК и заболевания как узлы, соединённые линиями, аналогично социальной сети. Они умеют распознавать шаблоны того, кто с кем связан. Однако большинство таких методов требуют много надёжных обучающих примеров и тщательно подобранных входных признаков. Это делает их уязвимыми к пропущенным данным, шумным измерениям и переобучению — они хорошо работают на известных данных, но не справляются с предсказаниями новых ассоциаций.
Обучение на самих данных
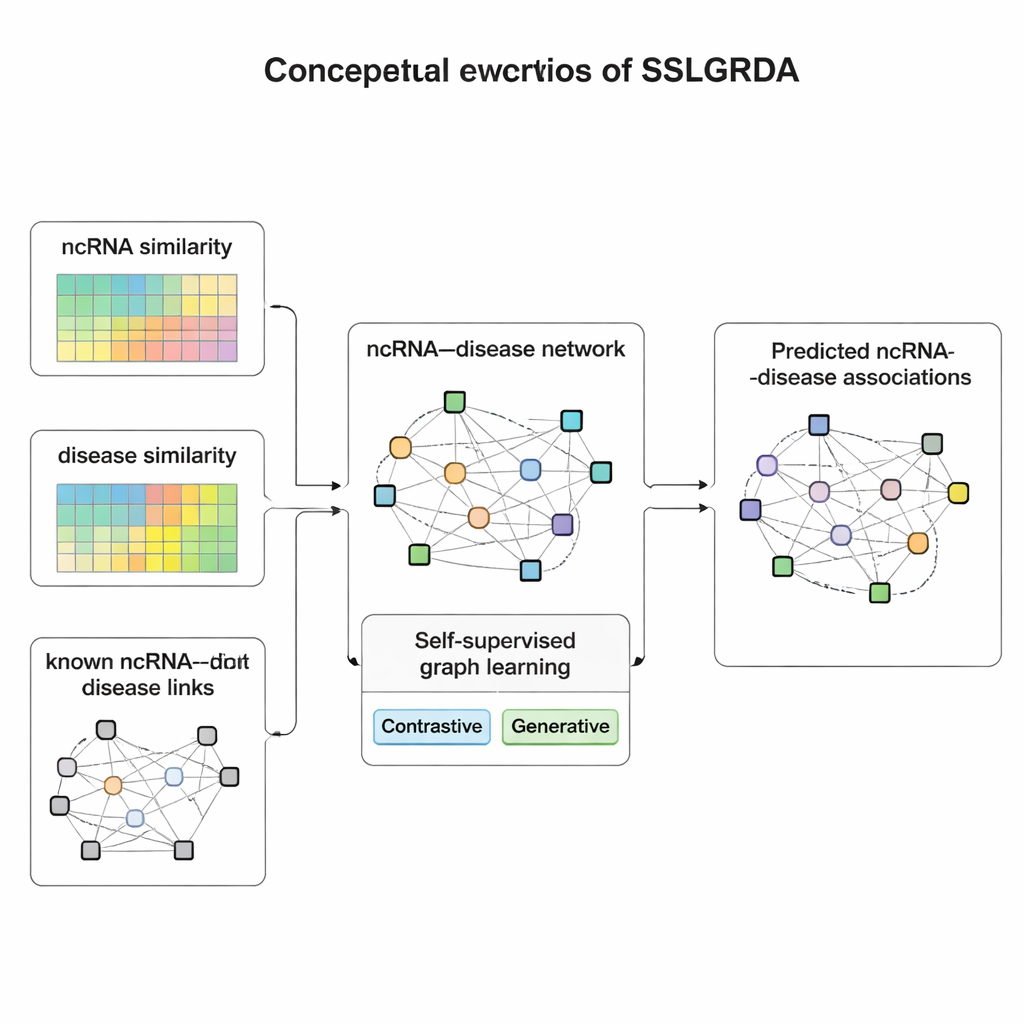
Авторы предлагают SSLGRDA — новую систему, которая учит графовую модель находить полезные закономерности, не полагаясь в большой степени на размеченные данные. Ключевая идея — «самообучение»: вместо того чтобы сообщать модели, какая РНК связана с каким заболеванием, модель сама формулирует тренировочные задачи, опираясь только на структуру и атрибуты сети. Исследователи строят два типа графов. Один сохраняет РНК и заболевания как разные типы узлов, соединённых известными связями. Другой объединяет их в единый большой граф и добавляет информацию о сходстве — насколько похожи две РНК или два заболевания — так что даже слабо связанные элементы получают поддержку соседей. На этих графах SSLGRDA использует два стиля самообучения. Контрастивные стратегии требуют, чтобы модель признала: разные «виды» представления одного и того же узла (например, его связи и его атрибуты) должны приводить к похожим внутренним представлениям, в то время как нерелевантные узлы должны быть явно различны. Генеративные стратегии намеренно скрывают части входных признаков и ставят задачу восстановить их, побуждая модель улавливать более глубокую структуру, а не запоминать шум.
Тестирование метода
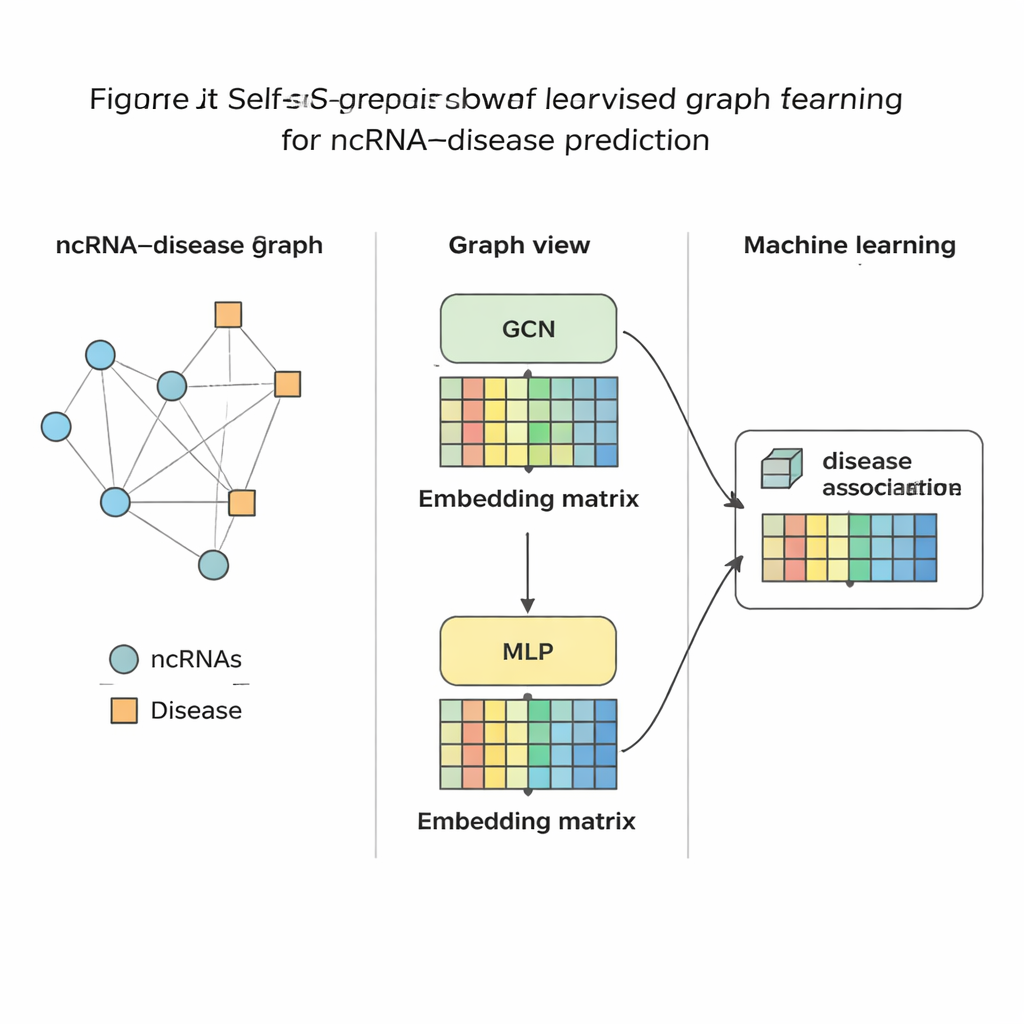
После того как SSLGRDA сводит каждую РНК и заболевание к компактному числовому «отпечатку», стандартный классификатор машинного обучения обучают оценивать, вероятна ли связь между ними. Авторы проверили подход на девяти различных наборах данных, охватывающих три основных типа РНК и сотни заболеваний. Во всех испытаниях контрастивные самообучающие варианты на объединённом (однородном) графе показали лучшие результаты, превосходя ряд существующих инструментов, включая сильные графовые базовые методы. Метод не только демонстрировал более высокую точность в глобальных тестах, но и ранжировал правильных партнёров близко к вершине при фокусировке на одной РНК или одном заболевании — что важно для реального применения, когда биолог начинает с конкретного рака и спрашивает, какие РНК исследовать. Авторы также показали, что те же идеи хорошо переносятся на другие биомедицинские сети, например связывающие микробы с заболеваниями или лекарствами.
От предсказаний к потенциальным терапиям
Чтобы продемонстрировать практическую ценность, команда применила SSLGRDA для поиска новых некодирующих РНК, вовлечённых в рак молочной железы, колоректальный рак и несколько других состояний. Многие из высоко ранжированных предложений впоследствии подтвердились в независимых базах данных или научных публикациях, что подтверждает способность модели находить биологически значимые паттерны. Для неспециалистов главное — это умный способ добывать подсказки о болезнях в постоянно растущем клубке биологических данных. Автоматически изучая, как РНК и заболевания группируются и взаимодействуют, методы самообучения на графах, такие как SSLGRDA, могут направлять лабораторных исследователей к наиболее перспективным мишеням, потенциально ускоряя путь от сырых данных к лучшей диагностике и лечению.
Цитирование: Wu, Q., Tang, S. Self-supervised learning on graphs predicts non-coding RNA and disease associations. Sci Rep 16, 5231 (2026). https://doi.org/10.1038/s41598-026-36030-2
Ключевые слова: некодирующая РНК, ассоциация с заболеванием, графовые нейронные сети, самообучение, вычислительная биология