Clear Sky Science · ru
Влияние молекулярной скученности на стабильность белков в бактериальном протеоме
Почему важна «переполненная» жизнь белков
Внутри каждой живой клетки белки выполняют свои функции в пространстве, настолько заполненном другими молекулами, что почти половина объёма может быть занята ими. Тем не менее большинство лабораторных экспериментов изучают белки в разбавленных, почти пустых растворах. В этой статье ставится простой, но важный вопрос: как эта переполненная реальность меняет стабильность и поведение белков и что это означает для молекулярной организации жизни?
Заглядывая в плотный клеточный мир
Чтобы исследовать это, учёные работали с бактерией Cupriavidus necator — микроорганизмом, представляющим интерес для зелёных технологий, таких как улавливание углерода и производство биопластиков. Они аккуратно разрушили клетки, сохранив сотни различных белков близкими к их природным состояниям. Затем добавили высокие концентрации крупных гидрофильных полимеров — распространённых «агентов скученности» PEG, декстрана и Фиколла — которые часто используют, чтобы имитировать плотную внутреннюю среду клетки.
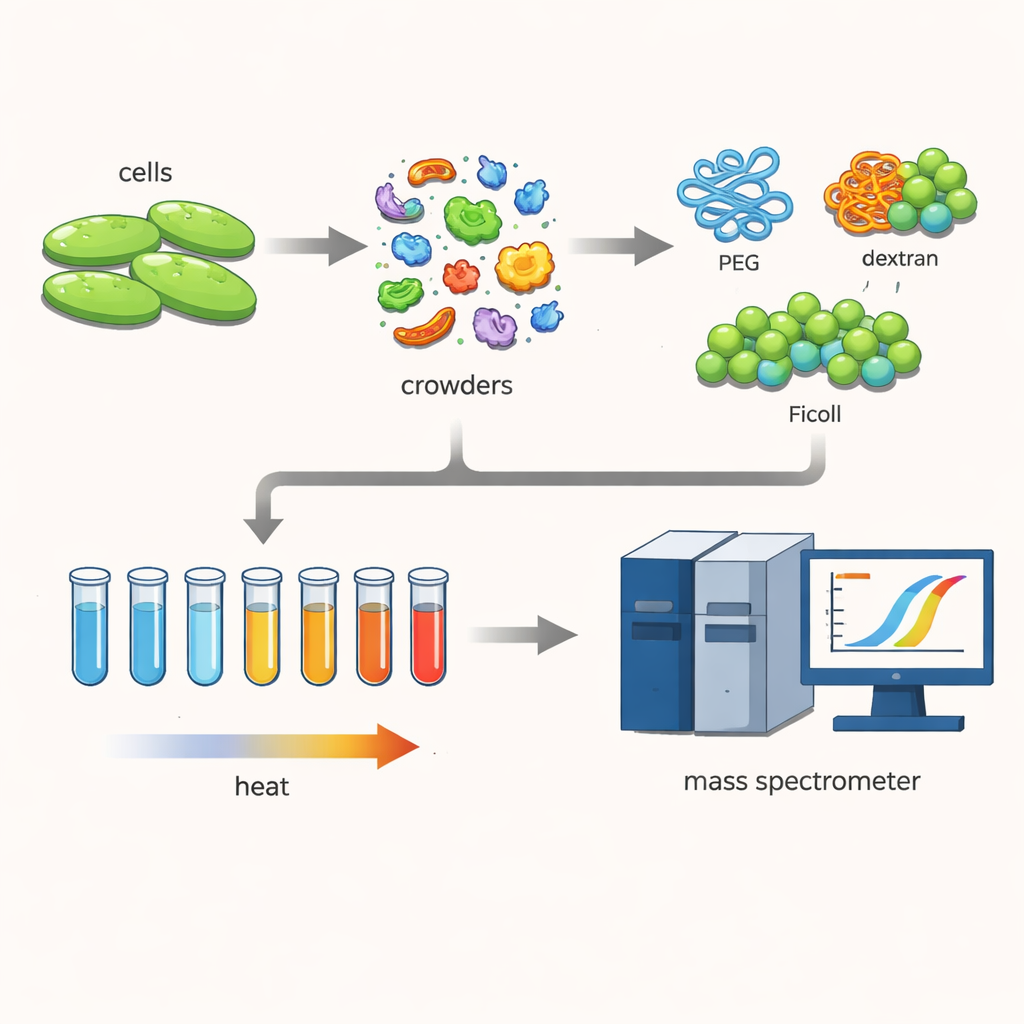
Наблюдая, как белки «плавятся»
Команда применила метод, известный как тепловое профилирование протеома. Они поэтапно нагревали множество небольших образцов белковой смеси от 30 до 70 градусов Цельсия. По мере повышения температуры менее стабильные белки разворачивались и образовывали агрегаты, выпадая из раствора. Отмечая остающиеся растворимые белки и измеряя их с помощью чувствительного масс-спектрометра, учёные восстанавливали кривые плавления для каждого белка и определяли температуру плавления — точку, при которой половина белка покидает растворимое, рабочее состояние. Сравнение этих температур с присутствием и без присутствия агентов скученности показало, как плотная среда смещает стабильность белков.
Смешанная картина: у одних белков устойчивость растёт, у других падает
В среднем добавление любого из шести полимерных агентов снизило температуры плавления по всему бактериальному протеому, что указывает на небольшое общее дестабилизирующее влияние. Но этот глобальный тренд скрывал куда более тонкую картину. Для десятков отдельных белков агенты скученности либо явно повышали, либо понижали стабильность, иногда на несколько градусов. Большинство белков реагировали только на один из шести реагентов, но небольшая группа реагировала на несколько, и почти все они либо последовательно стабилизировались, либо последовательно дестабилизировались, что намекает на общие свойства, определяющие их взаимодействие с агентами скученности.
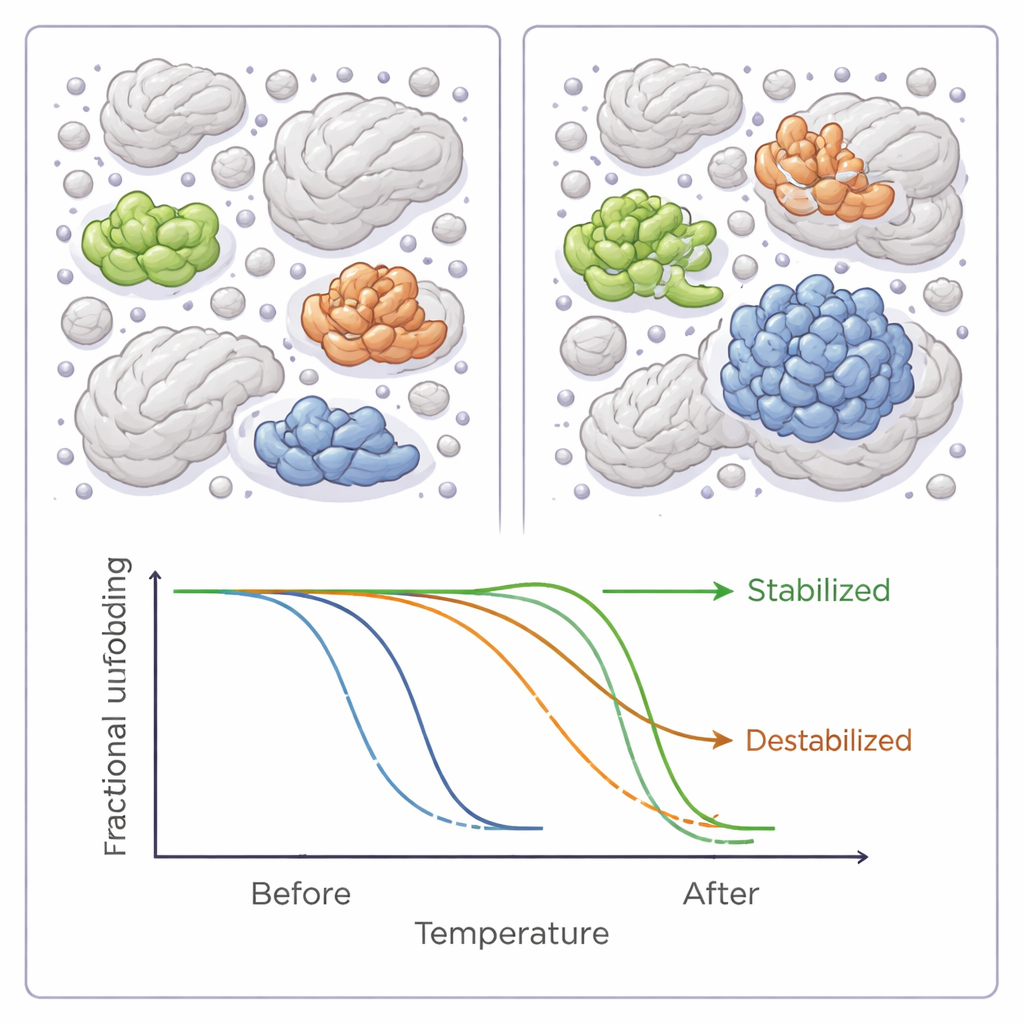
Что делает белок «выигравшим» или «проигравшим» в толпе
При детальном рассмотрении свойств этих чувствительных белков выявились закономерности. Белки, которые становились более стабильными в условиях скученности, как правило, были более гидрофобными — то есть имели больше водоотталкивающих поверхностей — и чаще оказывались классическими ферментами с чётко выраженными активными центрами. Они также чаще участвовали во взаимодействиях белок–белок или несли химические модификации, регулирующие их функцию. Напротив, дестабилизированные белки в среднем были меньше и меньше украшены такими модификациями. Эти наблюдения созвучны компьютерным моделям и другим экспериментам, предполагающим, что скученность может благоприятствовать одним белкам и делать других более уязвимыми в зависимости от размера, формы и привычных взаимодействий с партнёрами.
Не только простое сжатие: как на самом деле действуют агенты скученности
Традиционные объяснения эффекта молекулярной скученности сосредоточены на «исключённом объёме» — идее, что крупные молекулы просто занимают место, толкая белки к компактному, сложенному состоянию. Если бы это было единственным механизмом, ожидалось бы, что агенты скученности в основном стабилизируют белки и что будет сильная связь с объёмом или вязкостью полимеров. Вместо этого авторы обнаружили лишь слабые корреляции с размером и «густотой» полимеров. Их данные лучше согласуются с представлением о «преференциальном исключении»: агенты скученности и белки химически избегают друг друга, что косвенно благоприятствует некоторым сложенным состояниям, но также может нарушать тонкие взаимодействия, удерживающие другие белки стабильными. Короче говоря, это не только физическое сжатие, а тонкая химическая тяга и отталкивание формируют поведение белков.
Что это значит для понимания химии жизни
Для неспециалистов ключевая мысль в том, что белки в клетках нельзя полностью понять в изоляции, плавающими в прозрачном буфере. Плотный молекулярный джунгли вокруг них может делать одни белки прочнее, а другие — более хрупкими, изменяя работу целых сетей реакций. Это исследование, измерив изменения стабильности сотен белков одновременно, показывает, что эффекты скученности сложны и зависят от конкретного белка, и, вероятно, обусловлены прямыми взаимодействиями не меньше, чем простой упаковкой. При проектировании лекарств, промышленных ферментов или генетически модифицированных микроорганизмов признание этой переполненной реальности будет критично для предсказания того, как белки действительно ведут себя в живых системах.
Цитирование: McKeever, K., Dillon, E.T., Wynne, K. et al. Molecular crowding effects on protein stability in a bacterial proteome. Sci Rep 16, 5908 (2026). https://doi.org/10.1038/s41598-026-35990-9
Ключевые слова: молекулярная скученность, стабильность белков, тепловое профилирование протеома, бактериальный протеом, клеточная среда