Clear Sky Science · ru
Дефицит Negr1 изменяет глутаматную сигнализацию и путь кинуренина в мышиной модели психических расстройств
Почему это исследование мозга важно
Многие распространённые психические заболевания — от депрессии до шизофрении — связаны с тонкими изменениями в том, как клетки мозга общаются друг с другом. В этом исследовании изучается один из генетических факторов риска, называемый NEGR1, на мышах, чтобы понять, как его отсутствие меняет химию мозга и поведение. Отслеживая, как эти мыши двигаются после введения препарата, который кратковременно нарушает работу ключевого мозгового рецептора, и измеряя родственные нейрохимические показатели, исследователи выясняют, как генетика, пол и метаболизм мозга могут сочетаться и формировать уязвимость к психическим расстройствам.
Ген, поддерживающий равновесие сигналов в мозге
Ген NEGR1 кодирует белок на поверхности клетки, который помогает нервным клеткам формировать и стабилизировать контакты. Ранее показали, что удаление этого гена у мышей изменяет структуру мозга, снижает определённые тормозные (GABA) соединения и меняет реакции на препараты, влияющие на дофамин, такие как амфетамин. Поскольку эти изменения указывают на сдвиг в сторону усиления возбуждающих сигналов, команда сосредоточилась на другой крупной возбуждающей системе: глутамате и его NMDA‑рецепторах, которые критичны для обучения, памяти и гибкого поведения. Они также изучили «путь кинуренина» — метаболический маршрут разрушения триптофана с образованием соединений, которые могут либо усиливать, либо блокировать NMDA‑рецепторы.
Тестирование поведения с психоактивным препаратом
Чтобы проверить функцию NMDA‑рецепторов, исследователи использовали MK‑801 — известный препарат, который кратковременно блокирует эти рецепторы и может моделировать аспекты дисбаланса глутамата, наблюдаемого при психических состояниях. Самцы и самки мышей либо имели нормальный Negr1, либо полностью лишались его. Животным ежедневно вводили MK‑801, после чего тестировали в открытой арене: автоматически отслеживали общую подвижность, время, проведённое в углах, и вращательные движения. У самцов, не получавших раньше препарат, одна доза MK‑801 вызывала более сильный взрыв активности у мышей с дефицитом Negr1, чем у нормальных животных, что указывает на повышенную чувствительность их мозга к нарушению глутаматной сигнализации.
Неожиданный рисунок быстрой толерантности
При повторном введении MK‑801 картина изменилась. У самцов активность вздымалась в некоторые дни, но снижалась через день, формируя зигзагообразный паттерн, что свидетельствует о быстрой, частичной толерантности к эффектам препарата. В течение девяти дней нормальные самцы демонстрировали нарастающую реакцию, согласующуюся с сенситизацией, тогда как самцы с дефицитом Negr1 показывали приглушённое накопление активности и менее выраженные изменения из дня в день, что указывает на изменённую чувствительность NMDA‑рецепторов. Самки обоих генотипов адаптировались ещё быстрее: примерно к пятому дню MK‑801 перестал вызывать сильные поведенческие эффекты, и лечение было прекращено. Во всех показателях пол оказывал значительное влияние, а явные эффекты генотипа проявлялись главным образом у самцов.
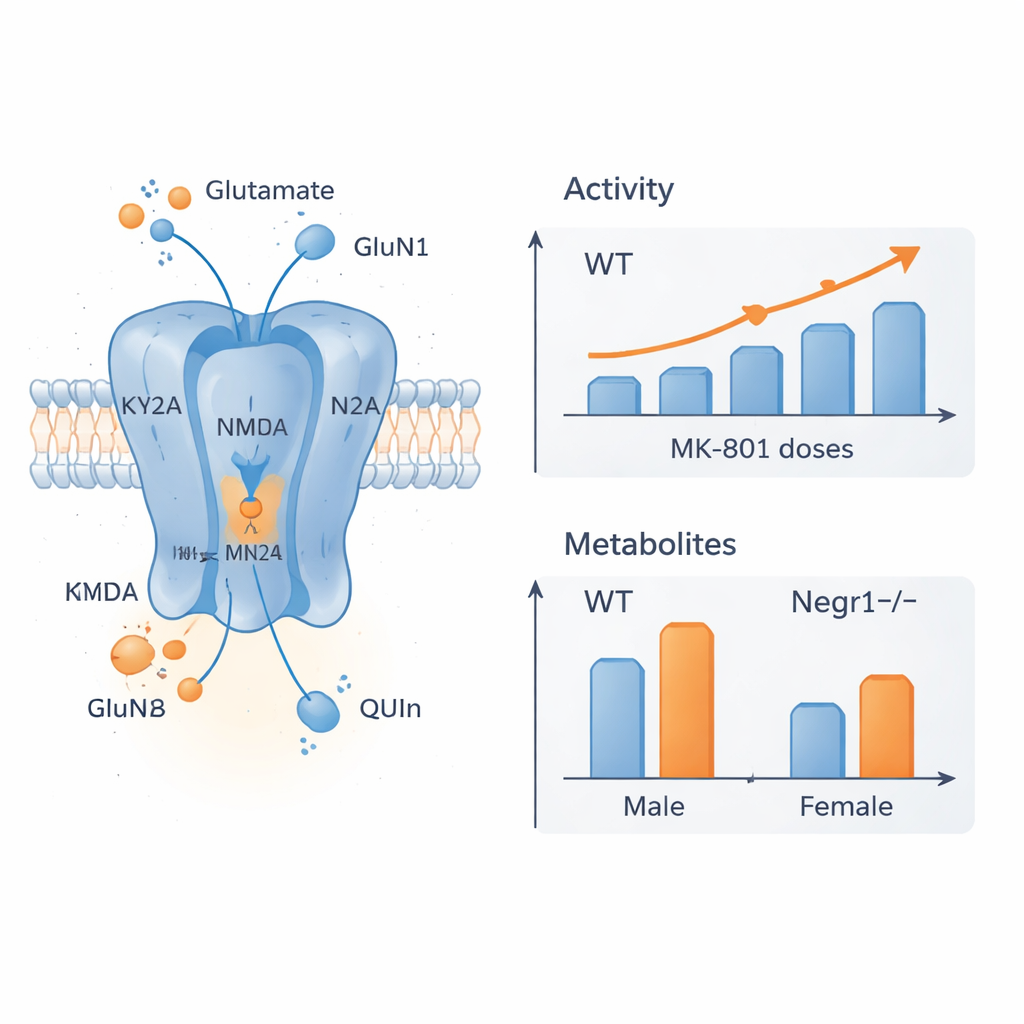
Сдвиги в рецепторах и нейрохимии
Чтобы выяснить причины поведенческих различий, команда измерила активность генов ключевых субъединиц NMDA‑рецепторов и фермента, синтезирующего D‑серин — ко‑сигнал для этих рецепторов. Они сосредоточились на областях мозга, критичных для настроения и когниции: лобной коре и гиппокампе. В лобной коре самки с дефицитом Negr1, получавшие MK‑801, продемонстрировали уменьшение экспрессии основных субъединиц рецептора, что намекает на то, что их мозг перестраивает состав рецепторов в ответ на сочетание мутации и препарата. В гиппокампе у самцов с дефицитом Negr1 наблюдалась более высокая базальная экспрессия некоторых NMDA‑субъединиц, в согласии с предыдущими данными о повышенном доступном количестве рецепторов; при лечении MK‑801 эти уровни возвращались ближе к норме. Параллельно детальный химический анализ крови и нескольких областей мозга показал, что несколько метаболитов пути кинуренина и сам глутамат изменяются в зависимости от пола и региона мозга, причём лобная кора наиболее затронута и некоторые изменения усиливаются с возрастом.
Что это означает для понимания психических заболеваний
В сумме эти результаты представляют NEGR1 как молекулярного организатора, помогающего поддерживать баланс возбуждающих и тормозных сигналов в мозге, отчасти за счёт формирования функции NMDA‑рецепторов и метаболизма триптофана. При отсутствии Negr1 мыши по‑другому реагируют на блокаду NMDA‑рецепторов, демонстрируют зависимые от пола сдвиги в нейрохимии и постепенно развивают толерантность нетипичными способами. Для неспециалиста главный вывод таков: один риск‑ген не действует сам по себе — его эффекты зависят от пола, области мозга и метаболического состояния. Эта работа укрепляет идею о том, что нацеливание на пути, связанные с NEGR1, — а не только на отдельные рецепторы — в перспективе может помочь точнее подбирать лечение психических заболеваний, связанных с нарушением глутаматного баланса.
Цитирование: Kuuskmäe, C., Mikheim, K., Mohammadrahimi, N. et al. Negr1 deficiency alters glutamate signalling and kynurenine pathway in a mouse model of psychiatric disorders. Sci Rep 16, 5317 (2026). https://doi.org/10.1038/s41598-026-35968-7
Ключевые слова: ген NEGR1, NMDA‑рецептор, глутаматная сигнализация, путь кинуренина, психические расстройства