Clear Sky Science · ru
Связанная с сепсисом утрата скелетных мышц смягчается фармакологической ингибицией сигнального пути STAT3 у мышей
Почему тяжелые инфекции крадут вашу силу
Пережить опасную для жизни инфекцию, такую как сепсис, — это лишь половина дела. Многие пациенты выходят из отделения интенсивной терапии настолько ослабленными, что ходьба, подъем по лестнице или даже поднятие рук становятся трудными. В этом исследовании задают простой, но неотложный вопрос: можно ли остановить разрушающий процесс, при котором организм поедает собственные мышцы во время сепсиса, и если да — как? Используя мышей, мышечные клетки в культуре и наблюдения за людьми в отделении интенсивной терапии, исследователи прослеживают ключевой сигнальный путь, приводящий к потере мышц, — и показывают, что целевой препарат способен частично блокировать этот вред.
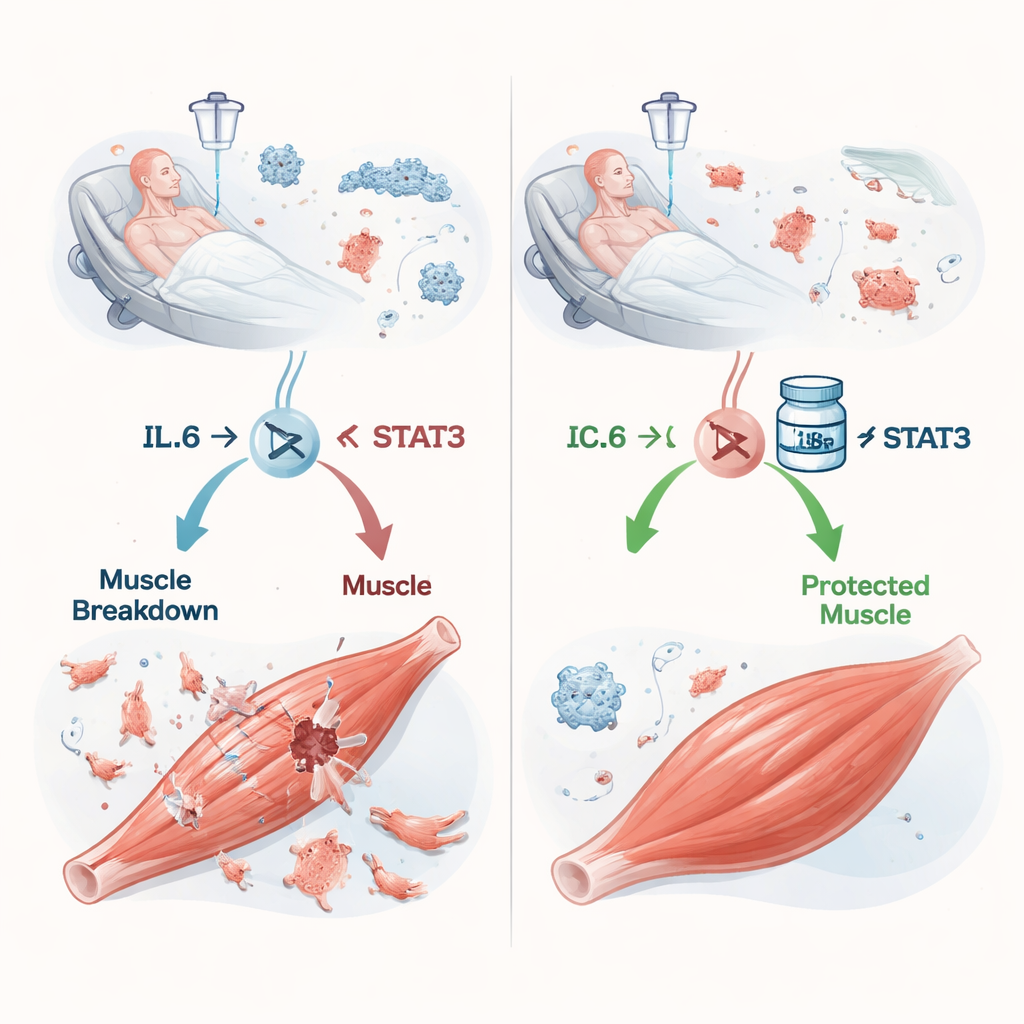
Цепная реакция от инфекции к потере мышц
Сепсис возникает, когда реакция организма на инфекцию выходит из-под контроля и в кровь выбрасывается множество провоспалительных молекул. Одной из важнейших является интерлейкин‑6 (IL‑6). Ранее были намеки, что IL‑6 может сигнализировать мышцам о необходимости разбирать собственные белки, но детали оставались неясными. Авторы сосредоточились на STAT3 — белке внутри клеток, который передаёт сигнал IL‑6 в ядро, где включаются или выключаются гены. У мышей, которым вводили слепок содержимого слепой кишки (cecal slurry) — по сути контролируемую смесь бактерий, — уровни IL‑6 в крови и в мышцах ног резко повышались по мере усугубления сепсиса. Одновременно STAT3 активировался в мышцах, а животные теряли вес, мышечную массу и силу захвата в зависимости от тяжести состояния — очень похоже на то, что наблюдается у тяжелобольных пациентов.
Как сепсис перепрограммирует мышечные клетки
Чтобы понять, что происходит внутри мышечных волокон при сепсисе, команда проанализировала активность генов в передней большеберцовой мышце (tibialis anterior), одной из главных мышц ноги. У септических мышей активность тысяч генов отличалась от контроля здоровых животных. Были включены пути, связанные с воспалением, клеточным стрессом и, в особенности, сигнальным каскадом IL‑6/STAT3. Усилились две основные системы утилизации белков: убиквитин‑протеасомная система, метящая конкретные мышечные белки для разрушения, и аутофагия, более общий процесс переработки. Ключевые «разрушительные» ферменты — MuRF1 и atrogin‑1 — резко возросли, тогда как пути, стимулирующие рост, и классические сигналы апоптоза в основном не изменились. В параллельных экспериментах культивированные мышечные клетки мыши, подвергнутые воздействию липополисахарида (LPS), компонента стенок грамотрицательных бактерий, показали ту же картину: активация IL‑6 и STAT3, всплеск MuRF1 и atrogin‑1, увеличение аутофагии и заметное истончение мышечных волокон.
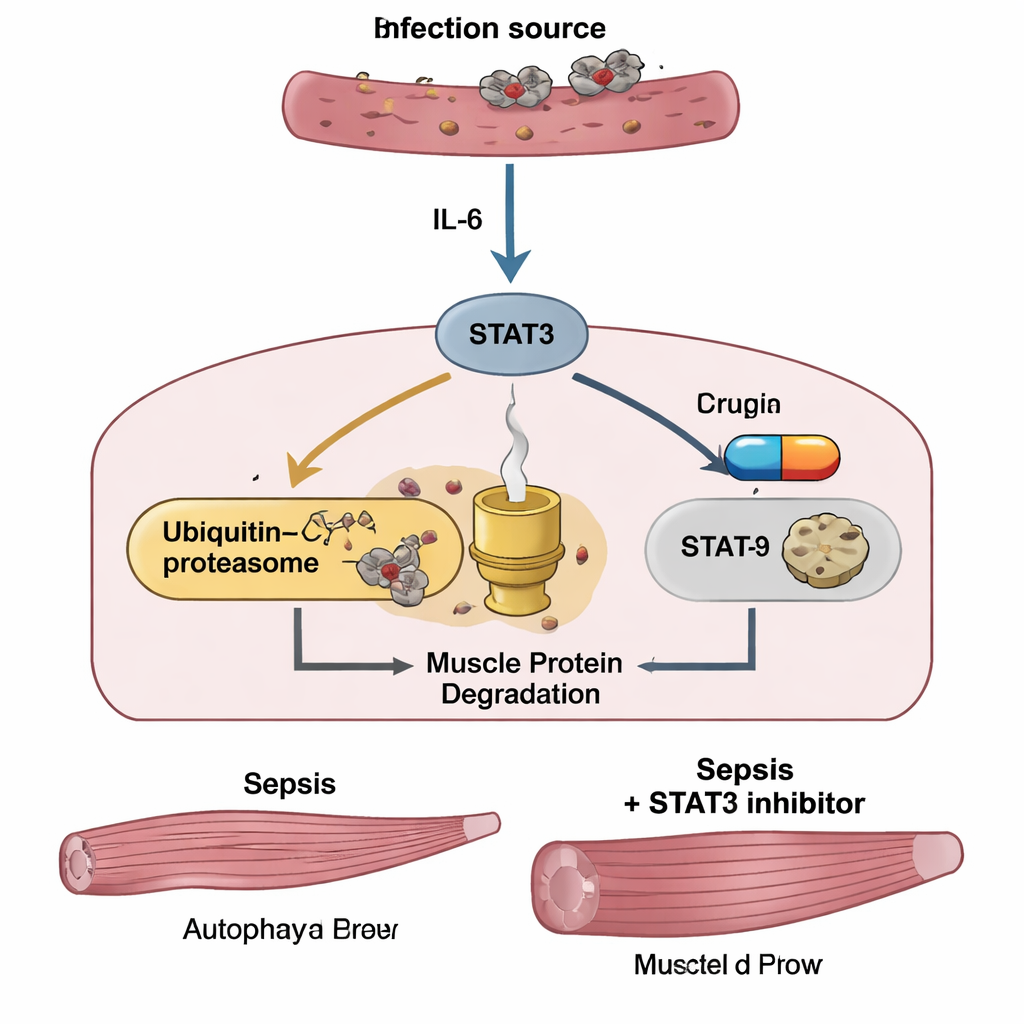
Блокировка ключевого переключателя для защиты мышц
Ключевой эксперимент проверял, может ли отключение STAT3 сохранить мышцы. Мышам с сепсисом давали малую молекулу‑ингибитор STAT3 под названием C188‑9, начиная через час после инфекции и затем ежедневно. Препарат не смягчил начальную «цитокиновую бурю» — уровни IL‑6 и другого провоспалительного фактора TNF‑α в крови оставались высокими, а вес и аппетит не восстанавливались быстро. Тем не менее C188‑9 явно защищал скелетные мышцы: у обработанных мышей сохранялась большая масса tibialis, они сильнее сжимали предмет, а под микроскопом их мышечные волокна были крупнее, чем у не получавших лечение септических животных. Внутри мышц C188‑9 резко снижал активированный STAT3 и уменьшал уровни MuRF1 и atrogin‑1, но при этом маркеры аутофагии в основном не менялись. В экспериментах в культуре предварительная обработка клеток C188‑9 аналогично сглаживала активацию STAT3 и подъём MuRF1 и atrogin‑1 и предотвращала LPS‑индуцированное усыхание волокон, опять же без подавления аутофагии.
Подсказки от пациентов в отделении интенсивной терапии
Чтобы проверить, имеют ли эти механизмы значение для людей, исследователи наблюдали 67 взрослых пациентов с сепсисом, поступивших в отделение интенсивной терапии в Японии. Анализы крови при поступлении показали, что у пациентов с септическим шоком уровни IL‑6 были особенно высоки. В общей группе IL‑6 — но не TNF‑α — тесно коррелировал с баллами тяжести сепсиса и с кровяными маркерами воспаления и повреждения мышц. В подгруппе из 45 пациентов, которым сделали два КТ‑сканирования брюшной полости, уровни IL‑6 при поступлении предсказывали, насколько сократится поясничная пояснично‑поперечная (psoas) мышца за последующие одну-три недели. Те, кто потерял больше всего мышц, имели значительно худшую двухлетнюю выживаемость по сравнению с теми, кто сохранил больше мышечной массы, что подчёркивает: связанная с сепсисом потеря мышц — это не просто косметическая проблема, она связана с долгосрочной смертностью.
Что это может значить для будущих методов лечения
В совокупности данные от мышей, клеток и людей рисуют правдоподобную картину: при сепсисе растущий уровень IL‑6 активирует STAT3 в мышцах, что в свою очередь усиливает систему разрушения белков, сдирающую с мышечных волокон их сократительные белки. Аутофагия также увеличивается, но, по-видимому, менее прямо контролируется STAT3. Фармакологически блокируя STAT3 с помощью C188‑9, исследователи смогли прервать этот путь «самоедства» у мышей и в культивированных мышечных клетках, сохранив силу, несмотря на продолжающуюся инфекцию и воспаление. Хотя это исследование пока преклиническое и не доказывает, что ингибиторы STAT3 помогут людям, оно указывает на ось IL‑6/STAT3 как перспективную мишень для препаратов, направленных на предотвращение или уменьшение глубокой мышечной слабости, преследующей многих выживших после сепсиса.
Цитирование: Ono, Y., Saito, M., Yoshihara, I. et al. Sepsis-associated skeletal muscle wasting is ameliorated by pharmacological inhibition of the STAT3 signaling pathway in mice. Sci Rep 16, 5008 (2026). https://doi.org/10.1038/s41598-026-35815-9
Ключевые слова: сепсис, потеря мышечной массы, STAT3, воспаление, восстановление после критического заболевания