Clear Sky Science · ru
Роль α7 никотинового ацетилхолинового рецептора в стимулировании поляризации макрофагов в сторону M2 в очагах воспаления
Как нервы помогают усмирять неконтролируемое воспаление
Когда мы порезали палец или боремся с инфекцией, организм запускает воспаление, чтобы защитить нас. Но если эта реакция длится слишком долго, она может повредить здоровые ткани и привести к хроническим заболеваниям. В этом исследовании изучается, как специфический «успокаивающий» рецептор на иммунных клетках, называемый α7 никотиновым ацетилхолиновым рецептором (α7nAChR), способствует смещению воспаления в сторону заживления, а не вреда, что даёт подсказки для разработки новых подходов к лечению состояний, таких как сепсис, болезни кишечника и артрит.
Две роли иммунной «уборочной» команды
Макрофаги — это иммунные клетки, которые выполняют функции уборки и восстановления. Они могут переключаться между двумя главными режимами. В режиме «атаки», часто называемом M1, они выделяют агрессивные молекулы для уничтожения микробов и удаления повреждённого материала. В режиме «исцеления», известном как M2, они выделяют успокаивающие сигналы, которые подавляют воспаление и способствуют восстановлению тканей. Здоровая реакция начинается с преобладания M1, а затем постепенно смещается в сторону M2 по мере исчезновения угрозы. Авторы поставили задачу выяснить, помогает ли α7nAChR — рецептор, изначально известный своей ролью в передаче нервных сигналов и воздействии никотина на мозг — направлять макрофаги в сторону этого восстановительного состояния M2 во время воспаления.
Нервной связью к переключателю, ведущему к исцелению
Чтобы проверить это, исследователи использовали мышей, у которых α7nAChR был либо сохранён, либо отсутствовал, и вызывали воспаление в брюшной полости двумя способами: компонентом бактерий (моделируя инфекцию) и бережной манипуляцией кишечника (моделируя стерильную хирургическую травму). Они измеряли молекулярные маркёры, различающие поведение M1 и M2, и с помощью проточной цитометрии считали доли каждого типа макрофагов. У нормальных мышей ранняя фаза воспаления была доминируема сигналами M1, но в течение следующих одного–двух дней росли маркёры M2, отражая естественный сдвиг к восстановлению. У мышей без α7nAChR, однако, уровни провоспалительных маркёров были повышены, маркёры заживления снижены, а доля M2 макрофагов в воспалённой области постоянно уменьшалась, смещая локальный баланс в сторону доминирования M1 и более разрушительного состояния.
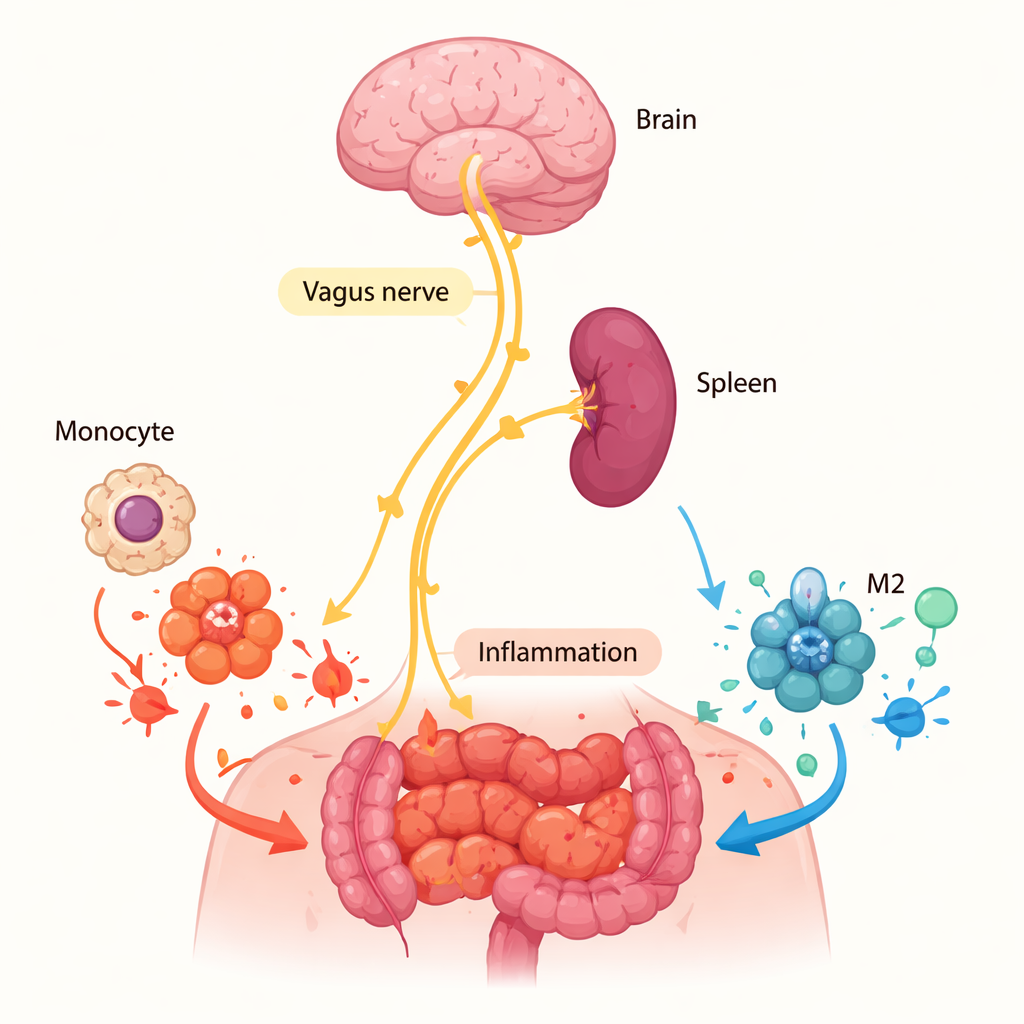
Почему селезёнка важнее, чем сама рана
Команда затем поинтересовалась, где именно действует α7nAChR. Он мог бы работать непосредственно в очаге воспаления, если бы местные клетки выделяли ацетилхолин — вещество, активирующее рецептор. Но измерения ацетилхолина в брюшной жидкости и в культурах клеток из воспалённой ткани дали по сути отрицательный результат, что говорит против сильного локального сигнала. Вместо этого внимание переключилось на селезёнку — ключевой иммунный орган, уже известный участием в «холинергическом анти-воспалительном пути», контролируемом блуждающим нервом. Когда исследователи хирургически удаляли селезёнку у нормальных мышей и затем вызывали брюшное воспаление, доля M2 макрофагов в брюшной полости падала, а общее число макрофагов снижалось. Эта картина соответствовала наблюдениям у мышей без α7nAChR, что предполагает: нервные сигналы в селезёнке подготавливают моноциты — предшественники макрофагов — становиться M2 ещё до их прибытия в воспалённую ткань.
Проверка переключателя на человеческих клетках
Чтобы выяснить, действует ли тот же рецептор на человеческие клетки, учёные обратились к лабораторно выращенным моноцитам из лейкемической клеточной линии (THP-1) и из донорской человеческой крови. Они направляли эти клетки в развитие либо в макрофаги M1, либо M2 с помощью стандартных иммунных сигналов, а затем добавляли специфический активатор α7nAChR. В обеих источниках человеческих клеток включение α7nAChR не усиливало маркёры M1, но явно повышало ключевые признаки поведения M2, включая поверхностный белок CD206 и противовоспалительный цитокин интерлейкин-10. Эти эксперименты поддерживают идею о том, что α7nAChR действует как смещающий переключатель, облегчающий развивающимся макрофагам принятие восстановительной идентичности, не подавляя при этом полностью иммунный ответ.
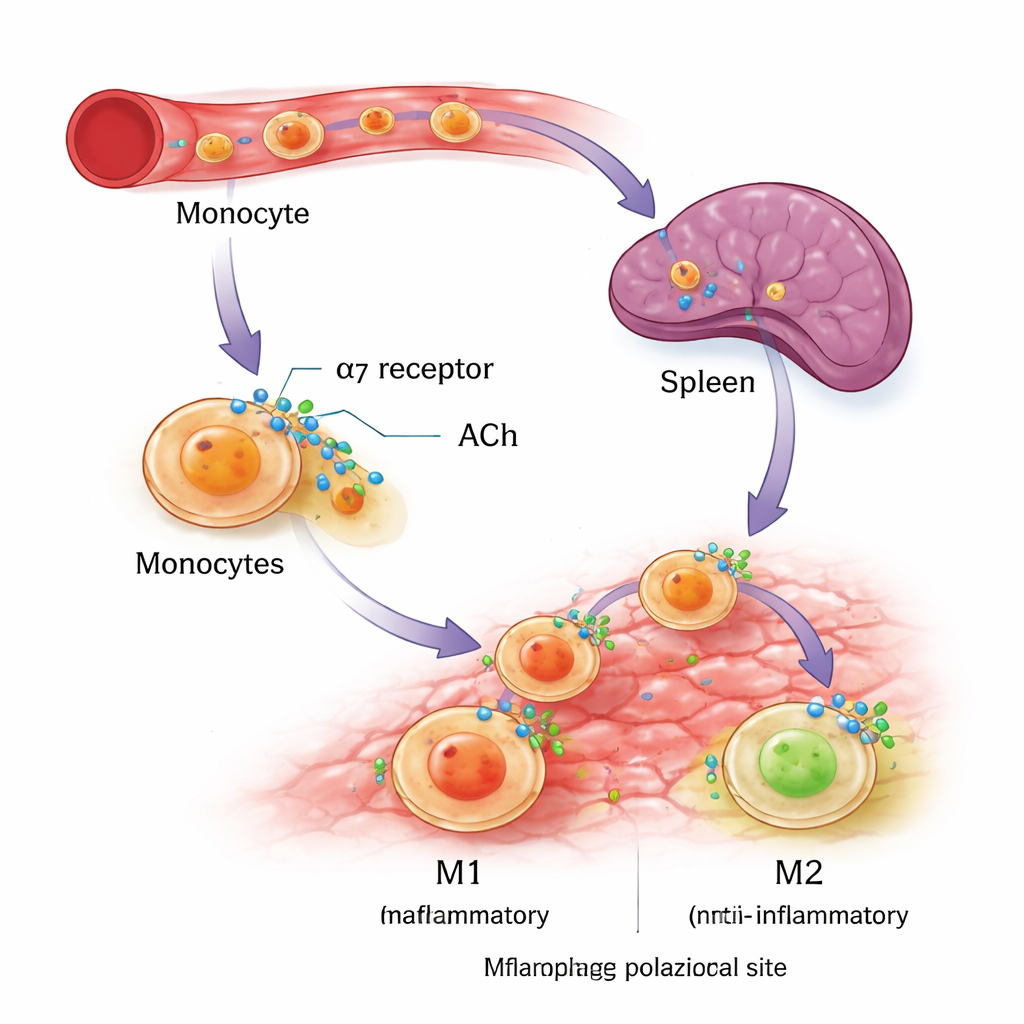
От подсказок с никотином к будущим терапиям
Полученные данные помогают объяснить несколько загадочных наблюдений: например, почему стимуляция блуждающего нерва может улучшать состояние при воспалительных заболеваниях и почему у курильщиков, несмотря на многочисленные риски для здоровья, отмечается несколько более низкий риск некоторых заболеваний кишечника — никотин может активировать α7nAChR. Вместо простого блокирования провоспалительных молекул α7nAChR, по-видимому, помогает организму переводить свои иммунные «уборочные» силы в более ориентированные на восстановление M2-клетки, особенно путём селезёчной подготовки моноцитов. Для неспециалиста это означает: наша нервная система делает больше, чем просто ощущает боль или управляет мышцами; она также тонко направляет иммунные клетки, подсказывая, когда нужно сражаться, а когда — восстанавливать. Научившись безопасно переключать этот встроенный механизм с помощью лекарств или таргетированной нервной стимуляции, можно открыть новые пути для усмирения вредного воспаления при сохранении способности организма защищаться.
Цитирование: Mihara, T., Tanabe, H., Nonoshita, Y. et al. The role of the α7 nicotinic acetylcholine receptor in promoting M2 macrophage polarization at inflammatory sites. Sci Rep 16, 5267 (2026). https://doi.org/10.1038/s41598-026-35757-2
Ключевые слова: поляризация макрофагов, воспаление, блуждающий нерв, никотиновый ацетилхолиновый рецептор, регуляция иммунитета