Clear Sky Science · ru
Физиологически релевантные формы радиотрейсеров Tc‑ и Re‑пирофосфата и основа их чувствительности к амилоиду транстиретина
Почему эта история о визуализации сердца важна
У многих людей с возрастом в сердце накапливаются бессимптомные отложения неправильно свернувшихся белков, называемые амилоидами. Некоторые из этих отложений, особенно те, что образованы белком крови транстиретином, могут делать сердце более жёстким и приводить к тяжёлым заболеваниям. Врачи всё чаще полагаются на радиотрейсер технеций‑99m пирофосфат (99mTc‑PYP), чтобы увидеть такие отложения на снимках. Тем не менее удивительно, что точная форма этого трейсерa в организме и причина его «предпочтения» определённым типам амилоида оставались неясными. В статье сочетаются теоретические и экспериментальные методы, чтобы выяснить, как трейсер действительно выглядит в условиях, близких к физиологическим, и как эта форма может позволять ему нацеливаться на вредные фибриллы транстиретина.
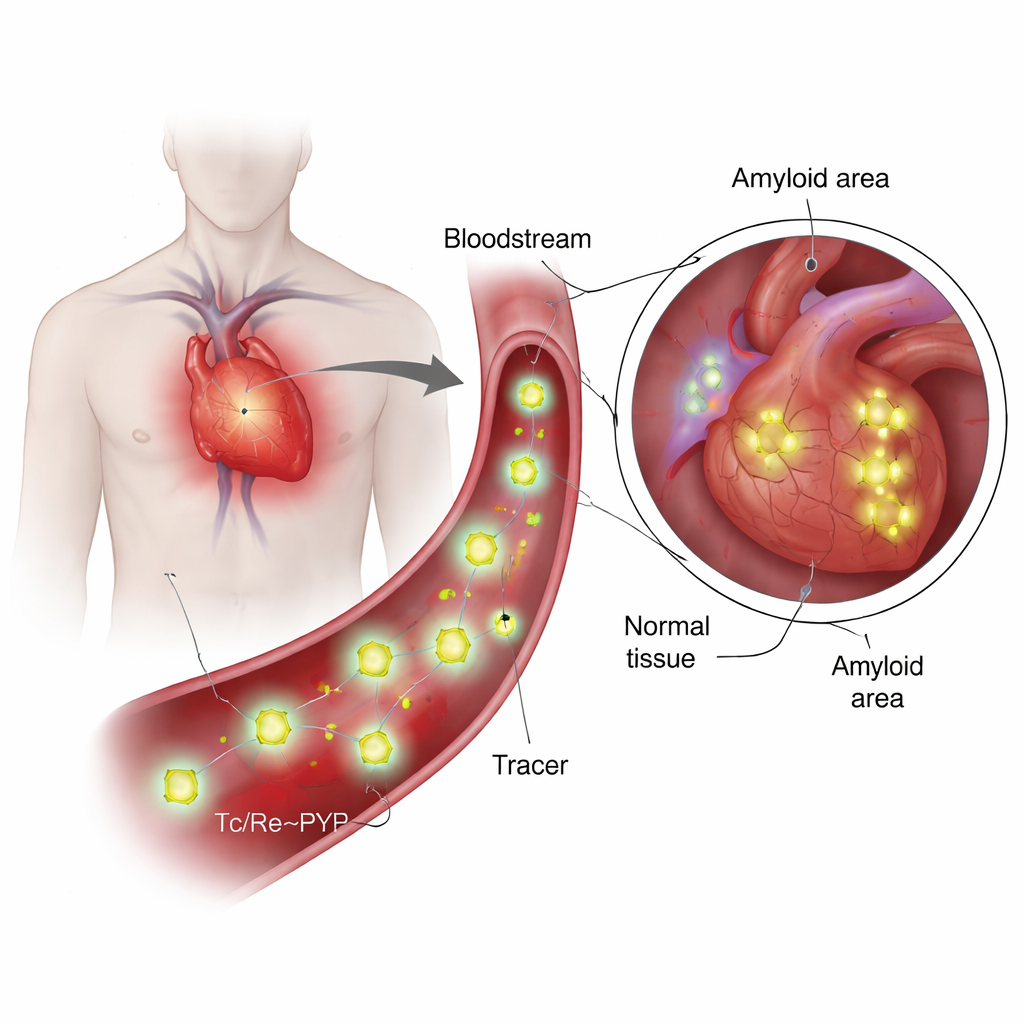
Что это за трейсеры и чем они особенные?
99mTc‑PYP используется десятилетиями для визуализации костей, поскольку он склонен накапливаться в областях с высоким обменом кальция и минералов. Более недавно врачи обнаружили, что он также способен различать два основных типа кардиального амилоидоза: один образован лёгочными цепями антител (AL), другой — транстиретином (ATTR). При ATTR сердце часто ярко светится на PYP‑сканах, тогда как при AL сигнал остаётся слабым, даже при схожем накоплении кальция. Это расхождение вызвало ключевой вопрос: прилипает ли трейсер только к кальцию или он взаимодействует непосредственно с самим амилоидным белком? Для ответа нужно знать истинную химическую структуру трейсерa в условиях, подобных крови, что ранее было описано лишь приблизительно.
Использование более безопасного аналога для изучения невидимого
Поскольку технеций радиоактивен и присутствует в медицинских препаратах в крохотных количествах, его трудно изучать напрямую многими лабораторными методами. Авторы поэтому использовали рений, близкий по размеру и предпочтениям связей элемент с более удобной химией, в качестве аналога. Они приготовили смеси рений‑пирофосфата в условиях, имитирующих клинические наборы PYP, и исследовали их с помощью набора методов: высокоуровневых квантово‑химических расчётов, УФ‑видимой спектроскопии, различных колебательных спектроскопий (ИК и Раман), ядерного магнитного резонанса, масс‑спектрометрии и спектроскопии Мёссбауэра олова. В совокупности эти методы позволили протестировать множество кандидатных структур и сузить круг видов, которые вероятно существуют при нейтральном pH, близком к значению в крови.
Гибкая, но узнаваемая молекулярная форма
Сопоставление данных указывает на общую «сердцевинную» структуру: октаэдрический комплекс, в котором атом технеция или рения в степени окисления +4 связан с двумя пирофосфатными группами и двумя молекулами воды. Проще говоря, металл находится в центре почти октаэдрической клетки из атомов кислорода; пирофосфаты действуют как многозубые анкеры, а молекулы воды занимают оставшиеся позиции. Эта базовая диаква‑дипирофосфатная единица не является жёсткой. Поскольку «руки» пирофосфата могут вращаться и образовывать внутримолекулярные водородные связи с связанными водами, молекула перебирает множество слегка разных форм в растворе. Расчёты и спектры показывают, что эти вариации смещают её поглощение света и колебательные отпечатки, что объясняет, почему экспериментальные полосы широки и почему ранним работам было трудно закрепить одну чистую структуру.
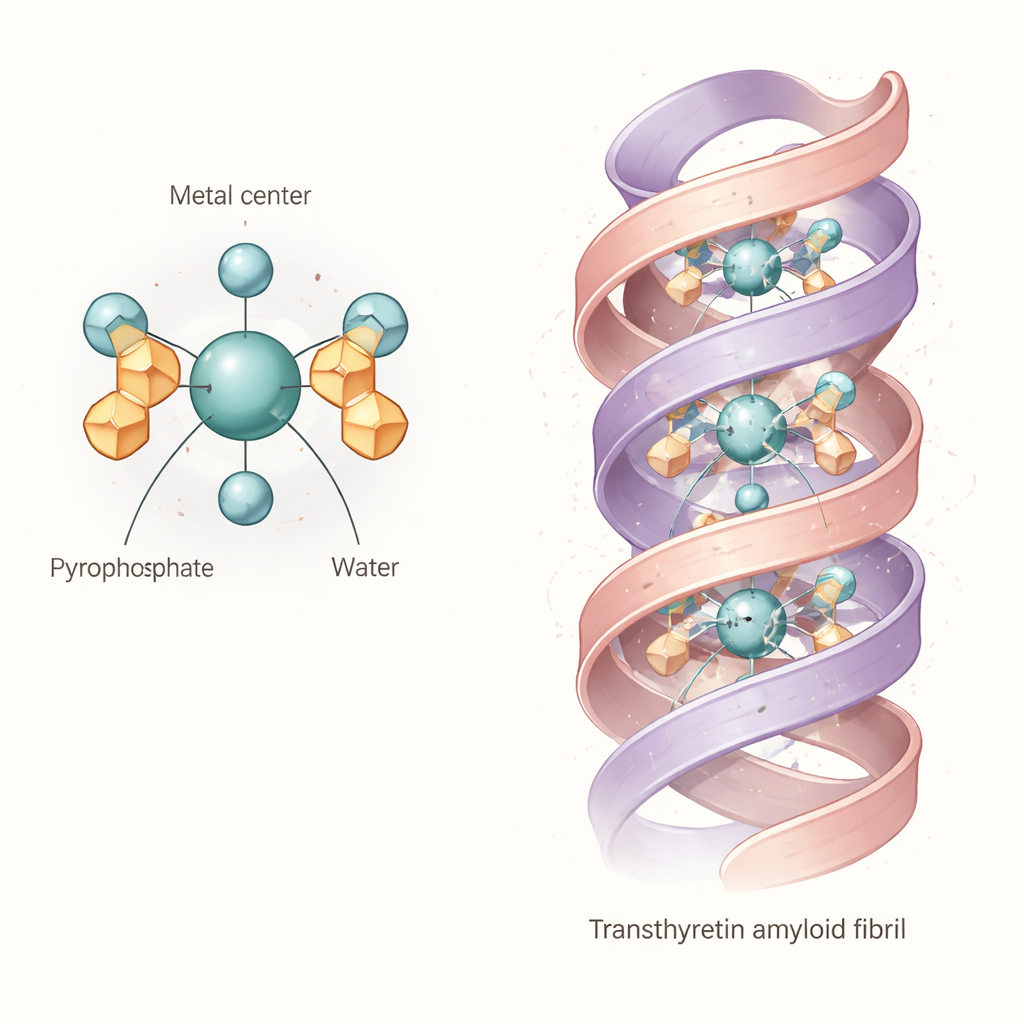
Что это значит для связывания с амилоидом сердца
Авторы затем проверили, может ли такой гибкий комплекс правдоподобно размещаться непосредственно внутри фибрилл транстиретина. Используя детальную структуру фибриллы человека, полученную методом криоэлектронной микроскопии, они провели компьютерный докинг моделированного комплекса технеций‑пирофосфата. Результаты показывают, что диаква‑дипирофосфатная единица может поместиться в центральный канал, проходящий вдоль фибриллы, образуя множественные водородные связи и ионные взаимодействия с заряженными боковыми цепями, выстилающими полость. Это указывает на то, что, по крайней мере для некоторых форм фибрилл транстиретина, трейсер не просто маркирует соседние минеральные отложения; он может захватываться непосредственно белковой каркасом. Структурная «податливость» трейсерa вероятно помогает ему адаптироваться к слегка разным карманам и распределениям зарядов в фибриллах пациентов.
Выводы для диагностики и будущих трейсеров
Для непрофессионального читателя главный вывод таков: широко используемое PYP‑сканирование сердца основано на трейсере, который более тонок и ориентирован на белок, чем считалось ранее. В физиологических условиях его лучше воспринимать как небольшую, содержащую воду металло‑пирофосфатную «клетку», способную сгибаться и образовывать множественные контакты с каналами амилоида транстиретина. Это понимание помогает объяснить, почему трейсер даёт сильные сигналы при одних амилоидных заболеваниях, но не при других, и почему незначительные изменения в белке или его окружении могут вызывать неожиданные потери чувствительности. Прояснение рабочей формы и распределения зарядов трейсерa создаёт основу для проектирования следующих поколений контрастных или терапевтических агентов, которые более селективно распознают патогенные фибриллы в сердце и за его пределами.
Цитирование: Simon, K.Z., Béres, K.A., Farkas, A. et al. Physiologically relevant forms of Tc- and Re-pyrophosphate radioactive tracers and the basis of their transthyretin amyloid sensitivity. Sci Rep 16, 6111 (2026). https://doi.org/10.1038/s41598-026-35746-5
Ключевые слова: кардиальный амилоидоз, транстиретин, технеций пирофосфат, молекулярная визуализация, химия радиотрейсеров