Clear Sky Science · ru
Синергетические анти-персистентные, ингибирующие эффлюкс и антибиопленочные свойства постбиотиков вагинального происхождения от Lactobacillus против UPEC: к новой терапии при инфекциях мочевых путей
Почему важны упорные инфекции мочевых путей
Инфекции мочевыводящих путей (ИМП) — одни из самых распространённых бактериальных инфекций, особенно у женщин, и многие люди сталкиваются с их рецидивами несмотря на приём антибиотиков. В этом исследовании рассматривается новый подход, позволяющий сократить использование антибиотиков: использование полезных вагинальных бактерий и их химических продуктов, чтобы остановить патогенные штаммы E. coli до того, как они закрепятся, спрячутся и вернутся снова.
Скрытые выжившие, стоящие за повторными инфекциями
Обычные антибиотики уничтожают большинство бактерий, но крошечная субпопуляция, известная как «персистеры», выживает, переходя в состояние спячки с низкой активностью. Эти «спящие» клетки не имеют генетической устойчивости, однако они переносят очень высокие дозы антибиотиков и могут пробудиться позже, вызывая хронические и рецидивирующие ИМП. Исследователи работали с распространённым штаммом, вызывающим ИМП — E. coli UTI89, и показали, что мощные антибиотики, такие как колистин и меропенем, легко индуцируют образование персистеров. В лабораторных тестах, моделирующих условия мочи, небольшие доли E. coli выживали при экстремальной антибиотиковой нагрузке, подтверждая, насколько легко персистеры могут появляться и почему стандартные схемы лечения часто не дают длительного облегчения.
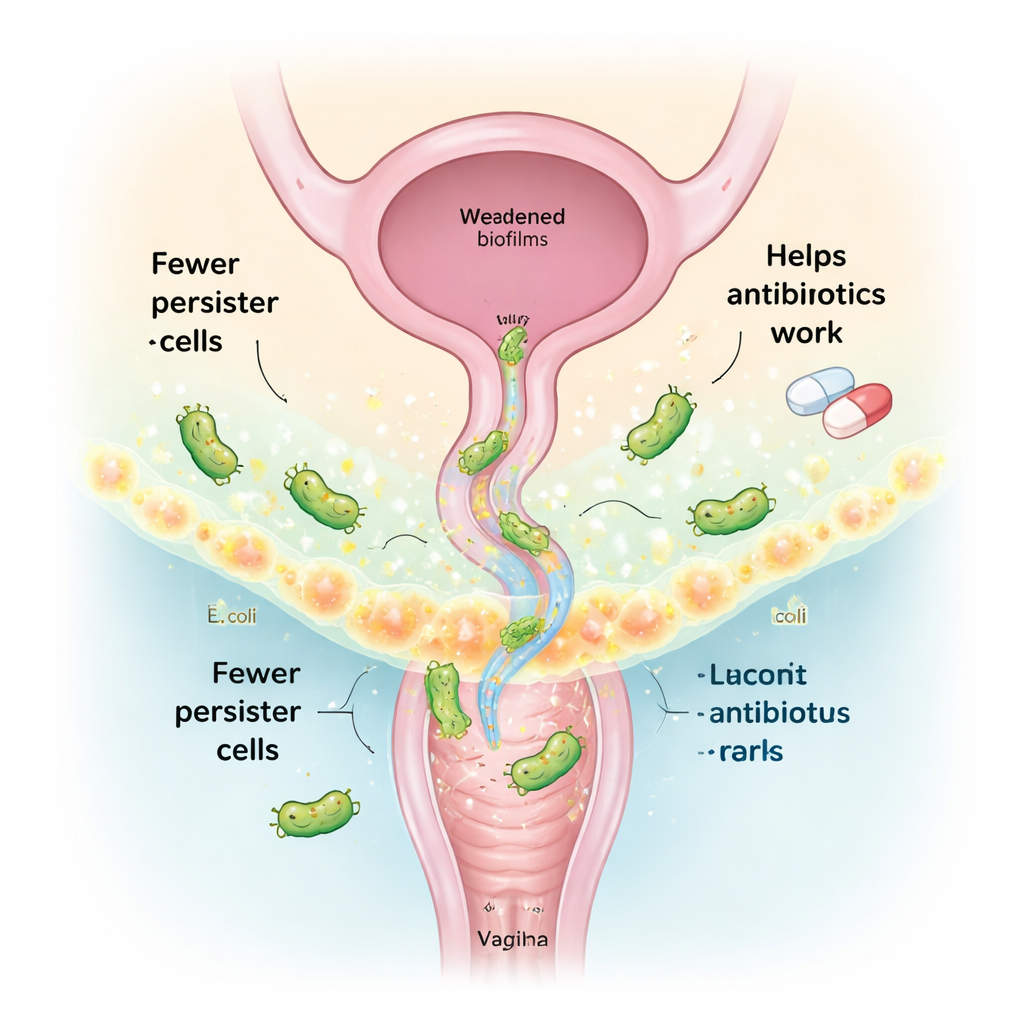
Превращение полезных вагинальных бактерий в средство лечения
Здоровая вагина обычно доминируется видами Lactobacillus, которые помогают держать вредные микробы под контролем. Вместо использования живых «пробиотиков» в этом исследовании сосредоточились на их безклеточном супернатанте — по сути на коктейле молекул, который они секретируют, называемом постбиотиками. Из штаммов вагинального Lactobacillus, выделенных у здоровых женщин, команда выделила и проанализировала эти секретированные соединения. Два ключевых метаболита — итаконовый ангидрид и (−)-терпинен-4-ол — выделялись своей способностью работать совместно и резко сокращать число персистентных клеток E. coli при сочетании с антибиотиками. Третье соединение, триптамин, ранее показавшее способность разрушать слизистую матрицу биопленки, было добавлено для усиления антибиопленочного эффекта.
Как новая смесь ослабляет трудноубиваемые бактерии
Учёные обнаружили, что молекулы, полученные от Lactobacillus, атакуют персистеров E. coli сразу по нескольким направлениям. Во-первых, они повышают образование реактивных форм кислорода — химически активных форм, повреждающих бактериальные компоненты — что делает антибиотики значительно более губительными для спящих клеток. При добавлении антиоксидантов этот эффект умирания снижался, подчёркивая роль окислительного стресса. Во-вторых, соединения делают наружную мембрану бактерий более «проницаемой», о чём свидетельствовали флуоресцентные красители, легче проникающие в клетки после обработки. В-третьих, они ингибируют клеточные «эффлюксные насосы» — крошечные молекулы-экспортёры, которые обычно выкачивают антибиотики из клетки. При блокировке насосов больше препарата остаётся внутри бактерий, и меньшее число персистеров выживает. В сумме эти изменения уменьшили уже сформированные биоплёнки E. coli в лабораторных тестах до десяти порядков величины, не повреждая при этом клетки млекопитающих иммунной системы при применённых дозах.
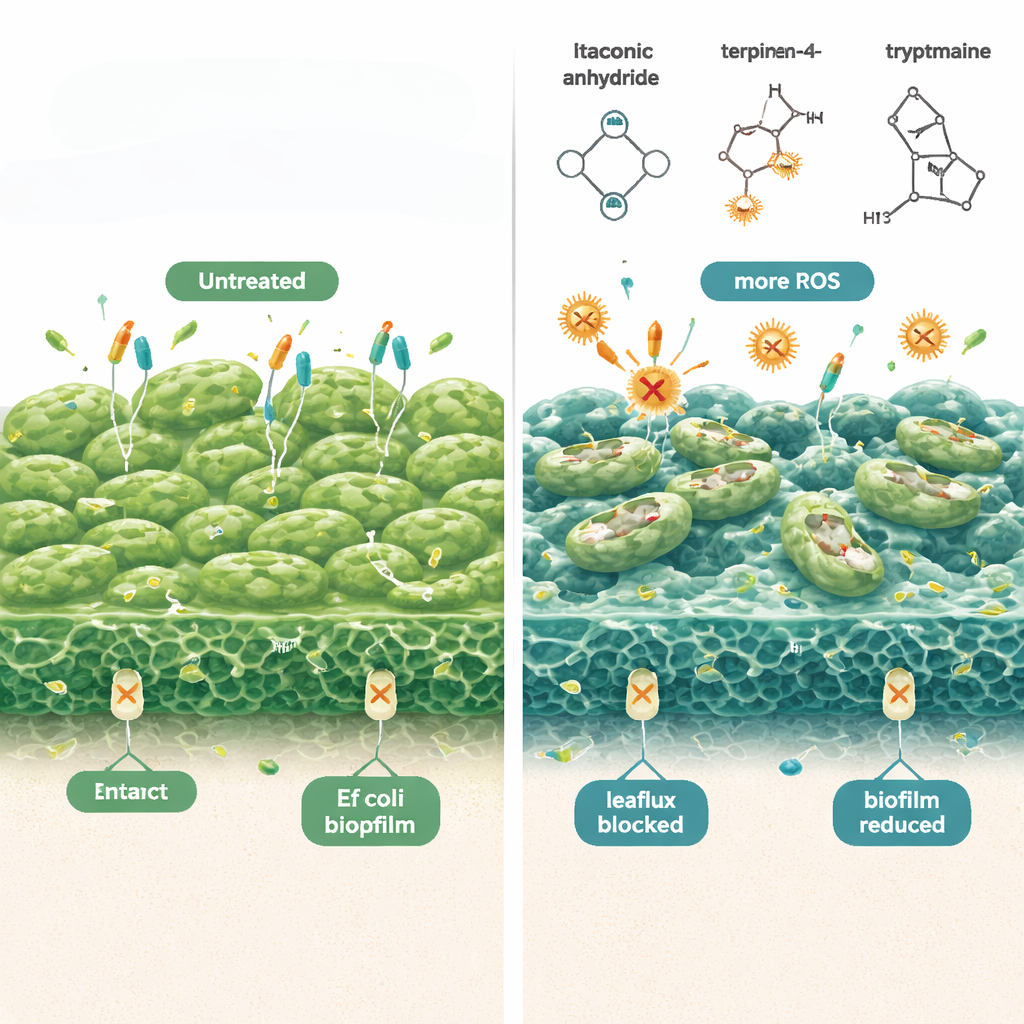
От лаборатории к практическому вагинальному лосьону
Чтобы превратить эти результаты в пригодное для повседневного использования средство, команда разработала специализированный вагинальный лосьон на термосенситивном геле на основе полоксамера 407. При комнатной температуре он ведёт себя как жидкость для удобного нанесения, затем при температуре тела мягко загустевает, улучшая контакт со стенками влагалища. Гель содержит определённую, безопасную комбинацию итаконового ангидрида, (−)-терпинен-4-ола и триптамина. В лабораторных пластинах эта формула работала в диапазоне pH, близком к вагинальным условиям, сильно подавляя формирование биоплёнок E. coli и сокращая число живых бактерий примерно на девять порядков величины. Она оставалась стабильной и биологически активной как минимум три месяца при холодном хранении и также показала широкий спектр активности против других проблемных бактерий, таких как Klebsiella, MRSA и Pseudomonas.
Оценка безопасности и защиты на мышах
Далее исследователи оценили лосьон в модели вагинальной инфекции E. coli на мышах. Мышей инфицировали светящимся (GFP-меченым) E. coli, а затем лечили либо новым метаболитным лосьоном, либо пробиотическим лосьоном с живыми Lactobacillus, либо коммерческим вагинальным лосьоном, либо плацебо-основой. Животные, получавшие специализированный метаболитный лосьон, демонстрировали заметно меньшую вагинальную воспалительную реакцию, сохраняли вес тела и имели значительно более низкие показатели бактерий в вагинальных выделениях по сравнению с другими группами. Самое впечатляющее — у обработанных мышей не выявляли E. coli в моче, мочевом пузыре, почках или вагинальной ткани, при этом функция почек оставалась нормальной, что указывает на то, что формула не только уменьшала местную инфекцию, но и предотвращала её распространение в верхние отделы мочевых путей.
Что это может значить для людей с рецидивирующими ИМП
Авторы приходят к выводу, что вагинальный лосьон, созданный из точных метаболитов, продуцируемых естественно защитными видами Lactobacillus, может ослаблять патогенные E. coli при ИМП несколькими способами: сокращая популяцию персистеров, разрушая биоплёнки и повышая эффективность стандартных антибиотиков. Поскольку подход опирается на неживые молекулы, а не на живые бактерии или длительные курсы системных препаратов, он может быть безопаснее, стабильнее и проще с точки зрения регулирования. Хотя по‑прежнему необходимы клинические исследования на людях, этот метаболитный лосьон указывает на будущее, в котором рецидивирующие ИМП предотвращают не только мощные антибиотики, но и умелое усиление собственной микробной защиты организма в её источнике.
Цитирование: Nair, V.G., Chellappan, D.R., Durai, R.D. et al. Synergistic antipersister, efflux inhibitory & antibiofilm activities of vaginal Lactobacillus-derived postbiotics against UPEC: toward a novel therapeutic for utis. Sci Rep 16, 5005 (2026). https://doi.org/10.1038/s41598-026-35736-7
Ключевые слова: инфекция мочевыводящих путей, вагинальный микробиом, постбиотики Lactobacillus, толерантность к антибиотикам, бактериальные биопленки