Clear Sky Science · ru
Прогностическое значение пространственных ниш при раке предстательной железы
Почему «районы» опухоли важны
Рак предстательной железы распространён, но не все опухоли ведут себя одинаково. Одни растут медленно, другие прогрессируют быстро и угрожают жизни пациента. Врачам сейчас помогают маркёры вроде уровня ПСА и гистологическая градация под микроскопом для оценки опасности опухоли. В этой работе поставлен новый вопрос: может ли точное место, где находятся раковые клетки внутри опухоли — оживлённый внешний край или более глубокое ядро — помочь предсказать исход для пациента?
Видеть опухоль как маленькую экосистему
Современные исследования показывают, что опухоль — это не однородный шар одинаковых клеток. Скорее, это небольшая экосистема с различными «районами» или пространственными нишами. При раке предстательной железы внутренняя часть опухоли и её наружный край, где раковые и нормальные ткани соприкасаются, могут содержать разные сочетания раковых и иммунных клеток, а также поддерживающих структур. Авторы применили технологию, называемую цифровым пространственным профилингом, которая позволяет измерять десятки белков прямо в тонких срезах ранее зафиксированной ткани, сохраняя информацию о том, из какого именно участка опухоли взята каждая проба.
Измерение белков в центре и на краю опухоли
Команда проанализировала образцы опухоли у 49 мужчин с высокорисковым раком предстательной железы, которым провели операцию. Для каждой опухоли выбирали участки в центре и на периферии и измеряли уровни 46 разных белков, связанных с иммунными клетками, апоптозом и сигнальными путями роста. В результате получились десятки тысяч точек данных. При раздельном рассмотрении центра и периферии подтвердилось, что эти зоны ведут себя по-разному: многие белки, особенно связанные с иммунной активностью, были более обильны на наружном крае опухоли, тогда как некоторые регуляторы клеточной гибели были выше в центре.
Когда раздельный взгляд не даёт ответа
Исследователи затем спросили, могут ли паттерны белков только в центре или только на периферии предсказать, как долго пациенты останутся свободны от прогрессирования болезни после операции. Применив статистические методы группировки пациентов по профилям белков в каждом из компартментов по отдельности, они нашли по два основных кластера и для центра, и для периферии. Однако ни один из наборов кластеров не соотнесся с реальным течением болезни во времени и не коррелировал явно с классическими факторами риска, такими как балл по Глисону или известные мутационные статусы (BRCA1/2, TP53). Иными словами, взгляд на любую из «микродворов» в изоляции не дал полезного нового прогностического маркера.
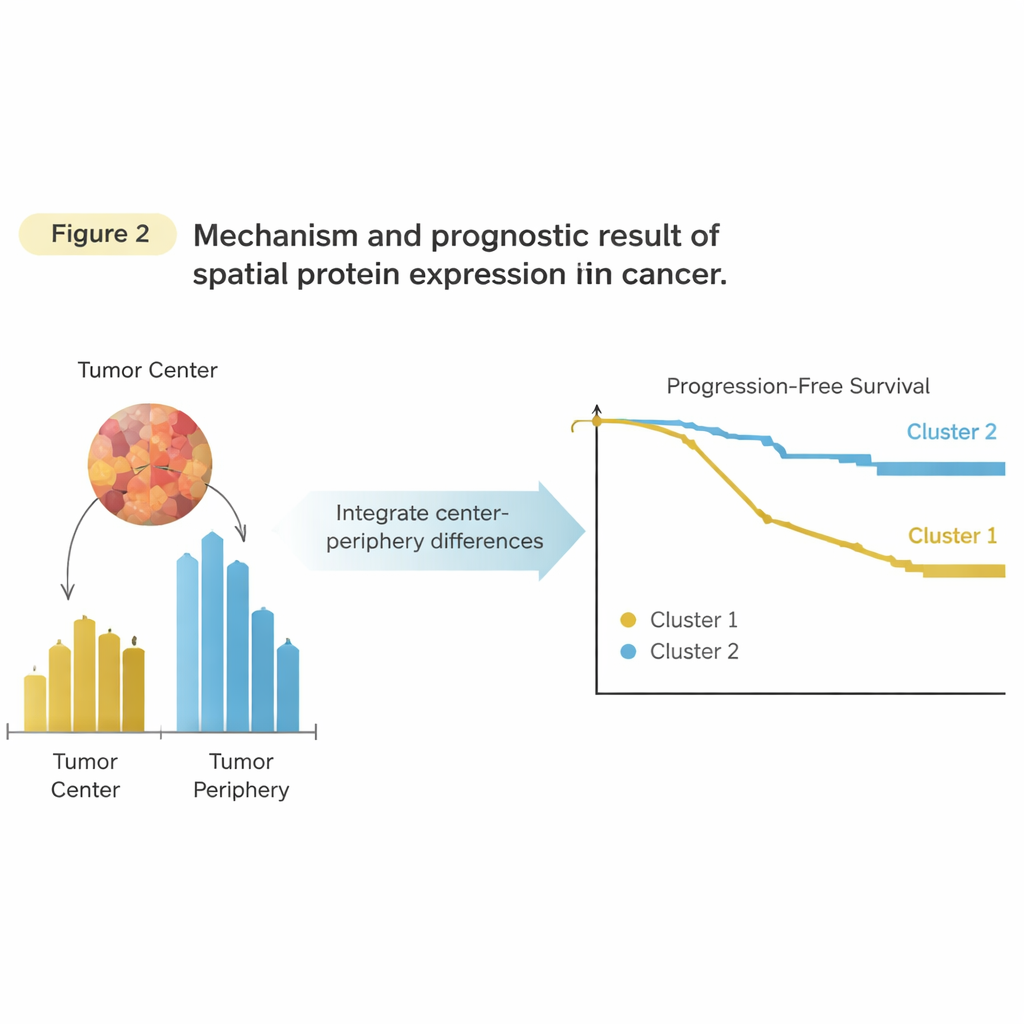
Комбинация обоих районов выявляет сигнал
Ключевой шаг заключался в объединении информации из центра и периферии, а не в рассмотрении их по отдельности. Для каждого белка и каждого пациента исследователи вычислили, насколько сильнее (или слабее) выражен этот белок на периферии по сравнению с центром. Это дало единое «значение баланса» для каждого белка, сохраняющее информацию о том, где внутри опухоли белок выше. При группировке пациентов по этим пространственным балансам появились два новых кластера. На этот раз кластеры имели значение: у одной группы время до прогрессирования заболевания было значительно короче, чем у другой. Важно, что сила подхода не зависела от какого-то единственного выдающегося белка, а возникала из общей пространственной картины по множеству белков, особенно связанных с иммунными клетками и ремоделированием ткани на краю опухоли.
Что это может означать для пациентов
Для людей с раком предстательной железы эти результаты указывают на то, что не только суммарное количество белков в опухоли, но и то, где именно они экспрессируются, может нести ценные подсказки о будущем поведении болезни. Хотя исследование небольшое и использует специализированную дорогую технологию, оно даёт доказательство концепции: пространственно учётные измерения белков могут выявить прогностическую информацию, ускользающую от стандартных тестов. При дальнейшей валидации и разработке более простых лабораторных методов такие пространственные биомаркеры в будущем могут помочь врачам точнее отличать высокорисковые опухоли, склонные к быстрому прогрессированию, от более контролируемых форм, что приведёт к более персонализированным решениям по лечению.
Цитирование: Schneider, F., Böning, S.H., Antunes, B.C. et al. Prognostic impact of spatial niches in prostate cancer. Sci Rep 16, 2598 (2026). https://doi.org/10.1038/s41598-026-35720-1
Ключевые слова: рак предстательной железы, пространственный профилинг, микроокружение опухоли, прогностический биомаркер, внутриотогенная гетерогенность