Clear Sky Science · ru
Белок Vpr ВИЧ индуцирует деметилирование промотора антисмысловой цепи SNCA, что приводит к нейрокогнитивным нарушениям
Почему ВИЧ по‑прежнему может влиять на мозг
Благодаря современным антиретровирусным препаратам люди с ВИЧ живут дольше и здоровее. Тем не менее многие по‑прежнему испытывают проблемы с памятью, вниманием и движением, даже когда вирус в крови хорошо контролируется. В этом исследовании внимание сосредоточено на небольшом вирусном белке Vpr и белке мозга альфа‑синуклеине, который также играет ключевую роль при болезни Паркинсона. Понимание того, как взаимодействуют эти две молекулы, может объяснить, почему ВИЧ способен ускорять старение мозга и подсказать новые подходы к его защите.
Белок мозга на перекрестке ВИЧ и болезни Паркинсона
Альфа‑синуклеин — это белок, который помогает нейронам общаться, особенно в областях мозга, контролирующих движение и память. Когда альфа‑синуклеина становится слишком много, он образует агрегаты, которые повреждают синапсы, перегружают митохондрии и усиливают воспаление. Такие скопления характерны для болезни Паркинсона. Авторы показывают, что уровень альфа‑синуклеина увеличивается с нормальным старением у мышей, а вирусный белок Vpr дополнительно повышает его содержание в клетках, подобных нейронам. Это ставит альфа‑синуклеин на перекрёстке между когнитивными нарушениями, связанными с ВИЧ, и классическими двигательными расстройствами.
Как вирусный белок переписывает «пунктуацию» в клетке
Каждая клетка использует химические метки на ДНК — их часто сравнивают с молекулярными знаками препинания — чтобы включать или выключать гены. В этой работе команда сосредоточилась на малоизвестном регуляторном переключателе внутри гена альфа‑синуклеина, называемом антисмысловым промотором. В здоровых клетках этот переключатель сильно метилирован, оставаясь относительно тихим. Исследователи обнаружили, что Vpr удаляет эти метки в определённых участках, процесс, известный как деметилирование. После снятия меток антисмысловой промотор активируется и стимулирует дополнительное производство альфа‑синуклеина, что создаёт условия для вредной агрегации.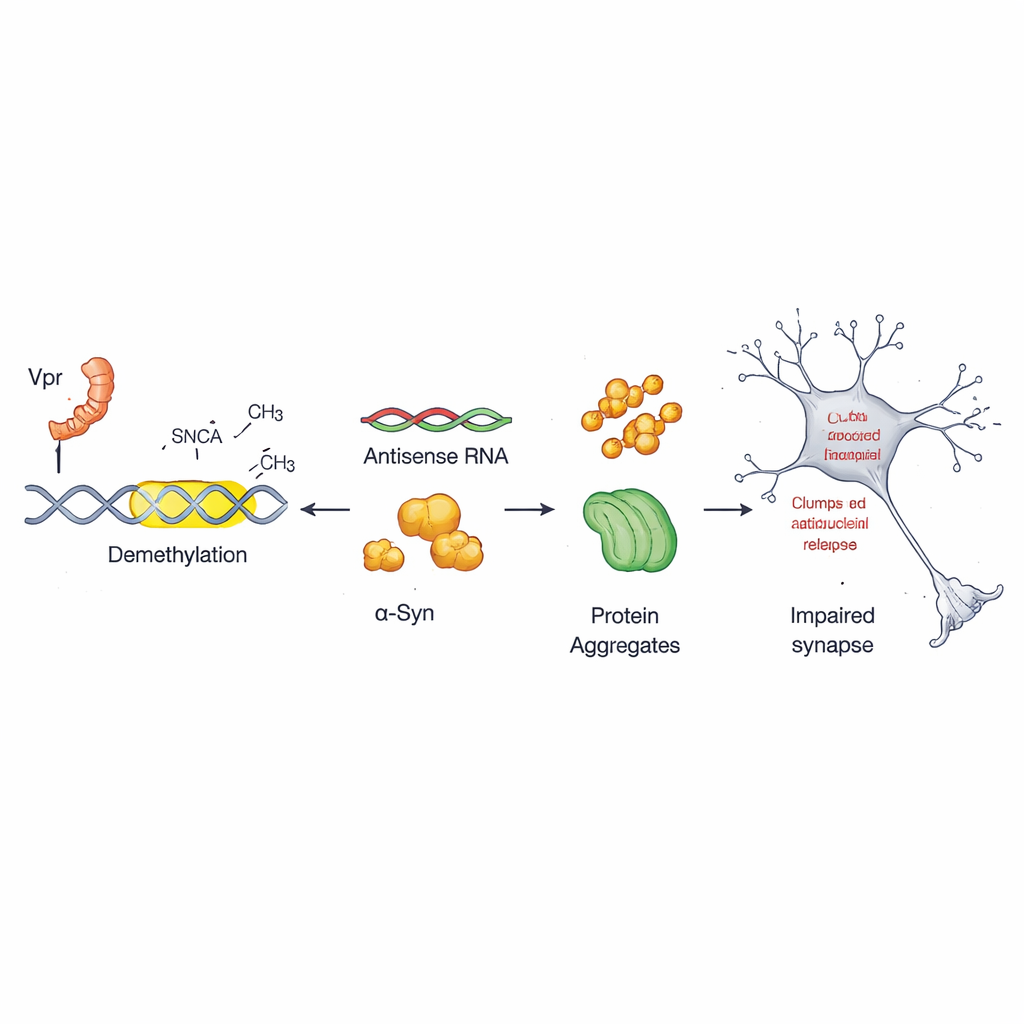
Данные из клеток, мышей и человеческих мозгов
Используя культивируемые человеческие клетки, близкие к нейронным, и первичные нейроны мышей, авторы показали, что добавление Vpr повышает уровни матричной РНК альфа‑синуклеина и самого белка с течением времени. Препарат, который в целом способствует деметилированию ДНК, отчасти имитировал эти эффекты, подчёркивая роль эпигенетического контроля. В отличие от этого, соединение DMOG, блокирующее деметилирующие ферменты, препятствовало полной активации антисмыслового промотора под действием Vpr. Далее команда проанализировала образцы человеческого мозга от доноров с ВИЧ и без. В мозгах ВИЧ‑позитивных доноров — и до, и после антиретровирусной терапии — было меньше метильных меток в том же участке ДНК и более высокие уровни альфа‑синуклеина и его антисмысловой транскрипции, особенно у доноров с ВИЧ‑ассоциированной деменцией. Это свидетельствует о том, что вирус оставляет стойкий эпигенетический след в мозге.
От молекулярных изменений до проблем с памятью
Чтобы связать эти молекулярные сдвиги с поведением, исследователи изучили влияние Vpr на мозговые цепи у мышей. При применении Vpr к слайсам гиппокампа — области, важной для памяти — базовая сила сигналов между нейронами не менялась, но способность укреплять связи (процесс, называемый долговременной потенциацией) снижалась. В живых мышах целевые инъекции Vpr в гиппокамп приводили к худшему выполнению задачи на пространственную память, где животные должны запомнить расположение объектов. В совокупности эти эксперименты показывают, что вызванные Vpr изменения альфа‑синуклеина — не просто биохимические курьёзы; они выражаются в ослаблении синапсов и измеримых дефицитах памяти.
Что это значит для людей, живущих с ВИЧ
В исследовании предлагается чёткая цепочка событий: ВИЧ выделяет Vpr, Vpr перепрограммирует ключевой ДНК‑переключатель, контролирующий альфа‑синуклеин, белок накапливается и образует сгустки, и нейроны постепенно теряют способность передавать сигналы и поддерживать память. Поскольку похожие нарушения альфа‑синуклеина лежат в основе болезни Паркинсона, работа указывает на общие механизмы между ВИЧ‑ассоциированными нарушениями и классическими нейродегенеративными болезнями. Важно, что результаты выделяют возможные новые стратегии — например, препараты, стабилизирующие метилирование ДНК в антисмысловом промоторе или ограничивающие накопление альфа‑синуклеина — чтобы замедлить или предотвратить когнитивный спад и двигательные проблемы, связанные с ВИЧ.
Цитирование: Santerre, M., Wang, Y., Kalamarides, D. et al. HIV Vpr induces demethylation of the SNCA antisense promoter, leading to neurocognitive impairment. Sci Rep 16, 6078 (2026). https://doi.org/10.1038/s41598-026-35691-3
Ключевые слова: Нейрокогнитивные расстройства, связанные с ВИЧ, альфа-синуклеин, эпигенетика, метилирование ДНК, симптомы, похожие на болезнь Паркинсона