Clear Sky Science · ru
Рациональная переработка высокоактивного ДНК-диазима G-квадруплекса через фланкирующие и петлевые нуклеобазы
Маленькие ДНК‑машины с большими возможностями
Представьте, что хрупкие белковые ферменты можно заменить крошечными нитями ДНК, которые выдерживают нагрев, химические воздействия и грубое обращение, но при этом выполняют полезную химию. Это исследование как раз изучает такую идею. Учёные модифицируют особые структуры ДНК, чтобы они вели себя как миниатюрные очистительные ферменты, способные использовать перекись водорода для генерации сильного сигнала. Эти более прочные и быстрые ДНК‑«машины» могут сделать будущие медицинские тесты, экологические сенсоры и переносную диагностику дешевле, надёжнее и проще в использовании вне лаборатории.
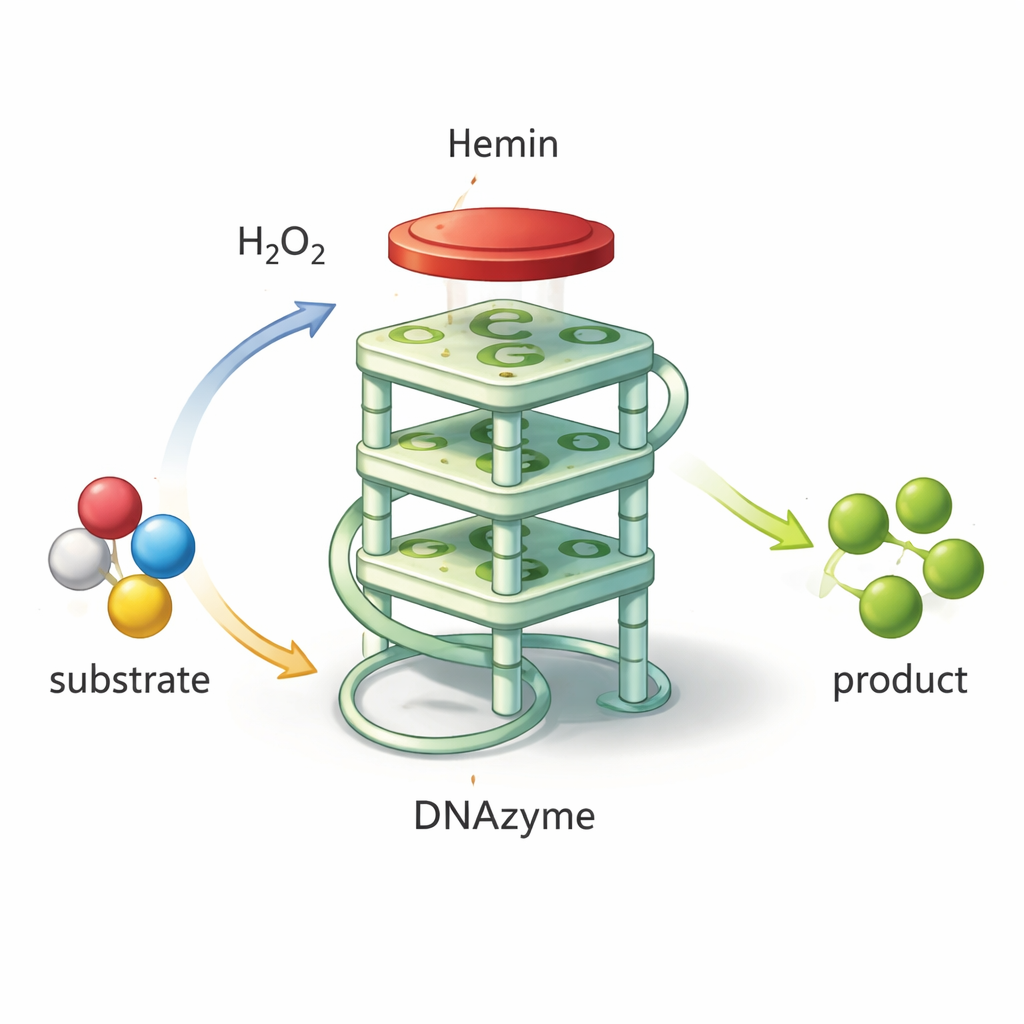
Преобразование ДНК в миниатюрный химический инструмент
Не всякая ДНК выступает лишь пассивным носителем генетической информации. Некоторые короткие последовательности сворачиваются в необычные формы, которые захватывают определённые молекулы или даже ускоряют химические реакции. Одна из таких форм — G‑квадруплекс, в котором гуанин‑богатая ДНК складывается в компактную четырёхслойную стопку. Когда небольшая молекула, содержащая железо, — гемин — располагается сверху этой стопки, пара ведёт себя как «ДНК-диазим»: ДНК‑катализатор, имитирующий природные пероксидазы. Он может использовать перекись водорода для окисления красящего реагента, давая сильный зелёный сигнал, который легко измерить. Поскольку такие ДНК‑диазимы дешёвы в производстве, стабильно ведут себя и легко перестраиваются, они являются перспективными строительными блоками для биосенсоров, обнаруживающих патогены, токсины или маркёры заболеваний.
Почему текущие ДНК‑ферменты требуют улучшения
Несмотря на обещания, большинство ДНК‑диазимов всё ещё медленнее и менее эффективны, чем белковые ферменты, встречающиеся в природе. Существующие биосенсоры часто вынуждены усиливать сигнал с помощью методов вроде ПЦР или добавлять вспомогательные химические вещества, что повышает стоимость и сложность. Ранее предпринятые попытки улучшить ДНК‑диазимы включали связывание двух ДНК‑звеньев, постоянное прикрепление гемина или окружение реактивного центра дополнительными химическими группами. Эти приёмы иногда помогают, но могут вводить громоздкость или требовать сложной химии. Ключевой открытый вопрос заключался в том, как простые изменения соседних нуклеобаз — особенно те, которые не нарушают основную форму G‑квадруплекса — могут предсказуемо и «проектируемо» регулировать активность.
Переработка высокоэффективного ДНК‑фермента
Команда сосредоточилась на особенно активном ДНК‑диазиме, известном как B730, который уже занимает место среди лучших немодифицированных катализаторов G‑квадруплекса. Они систематически изменяли ДНК прямо за пределами его ядра, добавляя или перемещая обычные основания — аденин, тимин и цитозин — в регионах петель и хвостов. Одна из переработанных версий, названная B730‑1.2, комбинировала добавленные аденины в петлях с короткой парой тимин–цитозин на одном конце нити. При умеренных концентрациях перекиси водорода этот вариант утраивал начальную скорость реакции и примерно вчетверо увеличивал общее количество окрашенного продукта по сравнению с оригинальным B730. Он также явно превосходил два других хорошо известных ДНК‑диазима — AS1411 и CatG4 — при сопоставимых тестах.
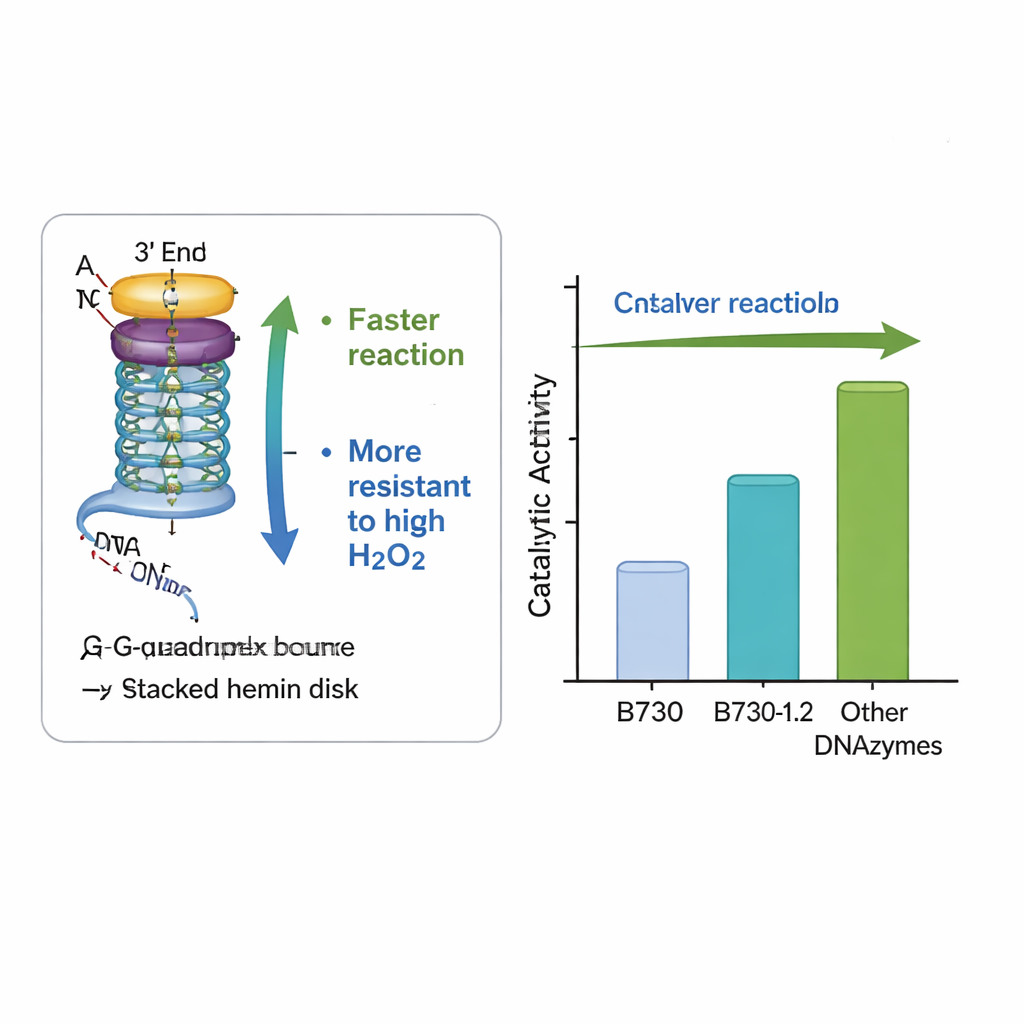
Создано, чтобы выдерживать суровые условия
Важное практическое препятствие как для природных, так и для искусственных пероксидаз состоит в том, что высокие уровни перекиси водорода — того самого ингредиента, который приводит реакцию в действие — способны разрушать фермент и останавливать процесс. Переработанный ДНК‑диазим B730‑1.2 показал выдающуюся стойкость: он сохранял и даже увеличивал свою активность при уровнях пероксида, которые обычно инактивируют похожие системы. Измерения поглощения света подтвердили, что модифицированная ДНК помогала более быстро формировать ключевой реактивный интермедиат — так называемое Соединение I — не нарушая при этом общей формы G‑квадруплекса. Иными словами, тонкие изменения во фланкирующих основаниях создали более благоприятную локальную среду для химии, ускоряя полезные стадии и помогая защитить каталитический центр от самоуничтожения.
Что это означает для будущих сенсоров
Для неспециалиста посыл прост: аккуратно подправив всего несколько «букв» по обе стороны от уже хорошего ДНК‑фермента, авторы получили версию, которая работает быстрее и продолжает действовать в более жёстких условиях. Их стратегия изменения фланкирующих и петлевых оснований предлагает простой, недорогой рецепт создания более мощных ДНК‑катализаторов без обращения к сложным химическим модификациям. Такие прочные и эффективные ДНК‑диазимы могут стать сердцем тест-полосок и переносных устройств нового поколения, которые быстро превращают невидимые биологические сигналы — следы вирусов или загрязнений — в легко читаемые цветовые изменения.
Цитирование: Adeoye, R.I., Babbudas, N., Birchenough, M. et al. Rational redesign of high-activity G-quadruplex DNAzyme through flanking and looping of nucleobases. Sci Rep 16, 5060 (2026). https://doi.org/10.1038/s41598-026-35686-0
Ключевые слова: ДНК-диазим G-квадруплекса, имитация пероксидазы, биосенсоры, инжиниринг аптамеров, катализ перекисью водорода