Clear Sky Science · ru
In silико‑дизайн мультиэпитопной вакцины, нацеленной на DENV‑1 и DENV‑3
Почему вакцины от денге по‑прежнему важны
Лихорадка денге уже не редкая тропическая болезнь; сейчас она угрожает миллиардам людей более чем в 100 странах и регулярно переполняет больницы в некоторых регионах Азии, Латинской Америки и других частях света. Несмотря на наличие двух лицензированных вакцин, защита остаётся неравномерной, особенно у людей, никогда прежде не болевших денге, и в регионах, где одновременно циркулируют несколько серотипов вируса. В этом исследовании ставится своевременный вопрос: может ли компьютерное проектирование помочь создать более безопасную и точную вакцину, нацеленную специально на опасные соинфекции двумя серотипами денге, которые часто встречаются вместе?
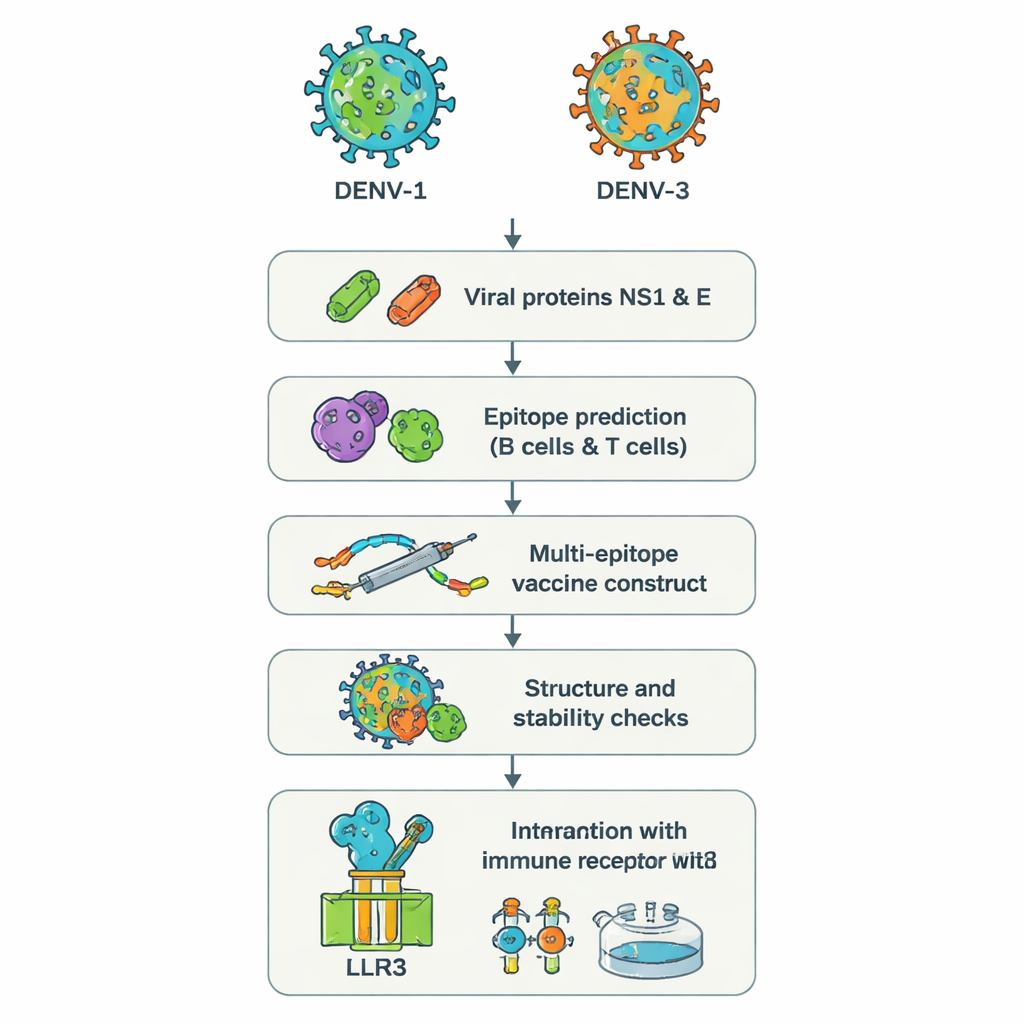
Два «хитрых» серотипа и почему они представляют проблему
Вирус денге существует в четырёх вариантах, называемых серотипами DENV‑1—DENV‑4. Инфекция любым из них может вызвать высокую температуру, сильную боль и в некоторых случаях угрожающее жизни кровотечение или шок. Тревожно, что повторное заражение другим серотипом порой ухудшает течение болезни вместо улучшения, поскольку уже присутствующие антитела могут облегчать проникновение нового вируса в клетки — этот процесс называют усилением, зависящим от антител (antibody‑dependent enhancement). В недавних вспышках врачи регистрировали пациентов с одновременной инфекцией DENV‑1 и DENV‑3 — сочетание, связанное с более тяжёлым течением и запутанными результатами тестов. Существующие вакцины не всегда надежно защищают все возрастные группы и все серотипы, особенно лиц без предыдущего контакта с вирусом, что оставляет опасную брешь в защите.
Проектирование вакцины «с молекулы вверх»
Вместо выращивания цельных вирусов в лаборатории исследователи использовали подход, иногда называемый «обратной вакцинацией». Они взяли генетические последовательности двух белков денге — NS1 и E — из DENV‑1 и DENV‑3. Эти белки важны для проникновения вируса в клетки и для того, как иммунная система распознаёт патоген. Мощные веб‑инструменты просканировали последовательности белков в поисках коротких участков — эпитопов — которые с наибольшей вероятностью будут распознаны человеческими B‑клетками (производящими антитела) и T‑клетками (уничтожающими инфицированные клетки и координирующими ответ). Из сотен кандидатов команда отобрала небольшой набор, прогнозируемо хорошо видимый иммунной системой, разделяемый между двумя серотипами и способный вызывать полезные противовирусные сигналы, такие как интерферон‑гамма.
Создание единой мультифункциональной вакцинной молекулы
Выбранные эпитопы затем цифровым образом сшили в один длинный искусственный белок — «мультиэпитопную» вакцину. Короткие аминокислотные связки действуют как гибкие распорки, чтобы каждый эпитоп сохранял свою форму и оставался доступным для иммунных клеток. Дополнительный фрагмент, основанный на природном человеческом антимикробном пептиде бета‑дефензине, добавили в качестве адьюванта для усиления общей реакции. Компьютерный анализ предсказал, что итоговая конструкция, содержащая 575 аминокислот, будет стабильной, гидрофильной (и, следовательно, легчерастворимой) и вряд ли будет выступать как аллерген. Дополнительные инструменты предсказания структуры сгенерировали трёхмерную модель и проверили, что большинство строительных блоков расположено реалистично, аналогично известным структурам белков.
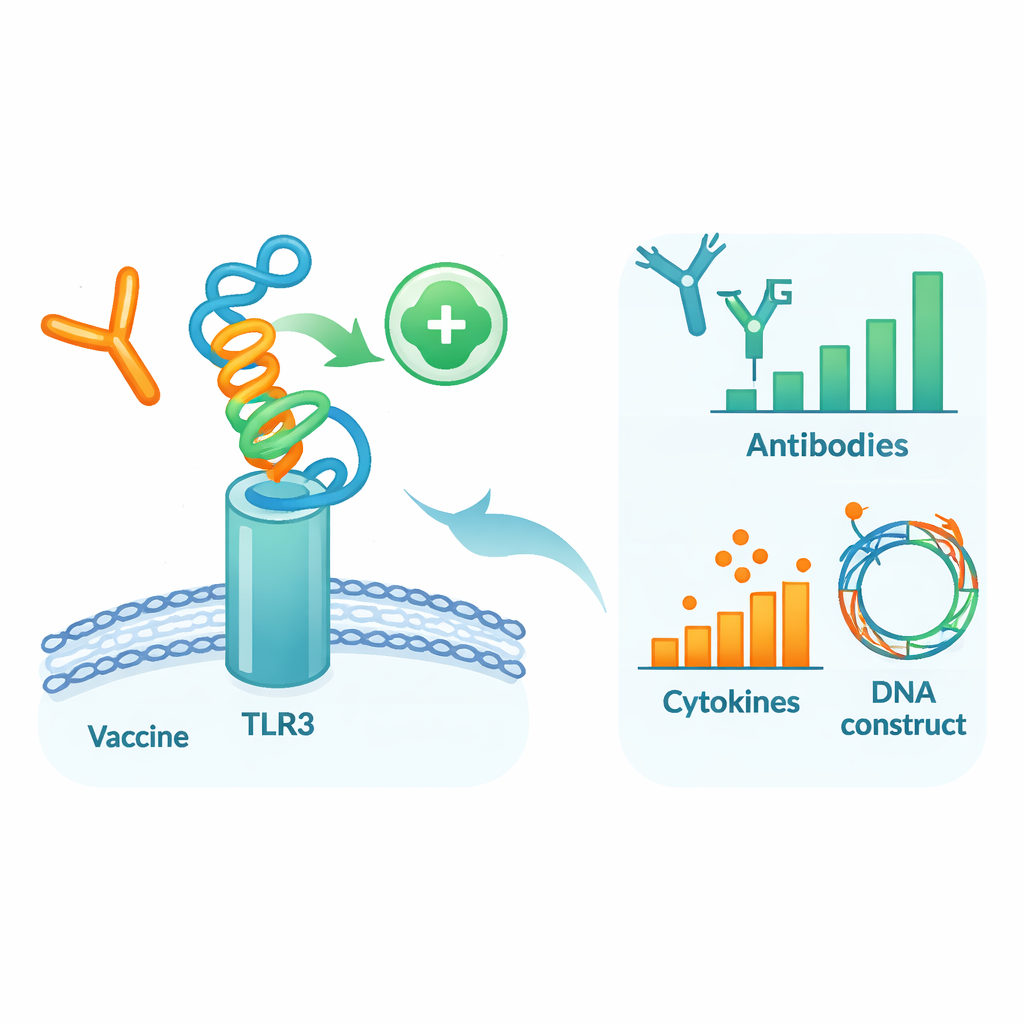
Тестирование кандидата в виртуальном организме
Чтобы понять, как этот спроектированный белок может вести себя в среде, приближённой к человеческой, авторы провели серию подробных компьютерных симуляций. Сначала они «докировали» модель вакцины к TLR3 — сенсорному белку на иммунных клетках, который обнаруживает вирусный материал и помогает запускать ранние оборонительные реакции. Молекулярно‑динамические симуляции — виртуальные «фильмы» движения атомов — показали, что вакцина и TLR3 формируют стабильный комплекс, что подтверждается благоприятной энергией связывания и множеством водородных связей. Дополнительные анализы движений и энергетики указали на конкретные области обоих молекул, выступающие в роли контактных «горячих точек». Затем симулятор иммунной системы смоделировал три прививки в течение нескольких месяцев. Виртуальная иммунная система выработала сильные волны защитных IgG‑антител, долгоживущую память B‑ и T‑клеток и сигнальные молекулы, соответствующие устойчивому противовирусному ответу.
От компьютерной модели к лабораторному чертежу
В заключение исследователи адаптировали генетический код вакцины для эффективного производства в распространённых лабораторных микроорганизмах и успешно вставили оптимизированную последовательность ДНК в стандартный экспрессионный плазмид, готовый для будущих экспериментальных испытаний. Проще говоря, их работа представляет подробный план новой вакцины от денге, ориентированной на тщательно подобранные фрагменты DENV‑1 и DENV‑3, прогнозируемо стабильной и безопасной и способной активно вовлекать обе ветви иммунной системы. Хотя эти результаты полностью вычислительные и требуют подтверждения в клетках, животных и, в конце концов, у людей, они демонстрируют, как современная биоинформатика может быстро генерировать таргетированные кандидаты на вакцину для сложных задач, таких как соинфекция денге.
Цитирование: Ishwar, D., Padavu, S., Kumar, M. et al. In silico design of a multi-epitope vaccine targeting DENV-1 and DENV-3. Sci Rep 16, 5308 (2026). https://doi.org/10.1038/s41598-026-35678-0
Ключевые слова: вакцина от денге, мультиэпитопная, DENV‑1, DENV‑3, иммуноинформатика