Clear Sky Science · ru
Интегративный анализ протеомики и метаболомики выявляет нарушение обмена аминокислот в клетках острого миелоидного лейкоза, устойчивых к адриамицину
Почему некоторые препараты против лейкоза перестают работать
Химиотерапия изменила подход к лечению острого миелоидного лейкоза (ОМЛ), быстропрогрессирующего рака крови. Тем не менее у многих пациентов болезнь возвращается, потому что раковые клетки учатся выживать несмотря на действующие на них препараты. В этом исследовании задают простой, но ключевой вопрос: что меняется внутри лейкемических клеток, когда они становятся устойчивыми к адриамицину — одному из стандартных препаратов — и могут ли эти изменения подсказать новые способы вернуть эффективности препарата?
Заглядывая внутрь лейкемических клеток
Чтобы ответить на этот вопрос, исследователи сравнили распространённую человеческую линию клеток ОМЛ под названием HL60 с её «сестринской» линией, приобретшей устойчивость к адриамицину (HL60/R). Вместо того чтобы изучать по одному гену или белку, они использовали две широкие взаимодополняющие методики. Протеомика измеряла тысячи разных белков — молекул‑исполнителей большинства клеточных функций. Метаболомика фиксировала сотни малых молекул, участвующих в метаболизме клетки, включая липиды, сахара и аминокислоты. Комбинируя эти уровни «омики», команда создала подробную картину того, чем устойчивые клетки отличаются от всё ещё чувствительных собратьев.
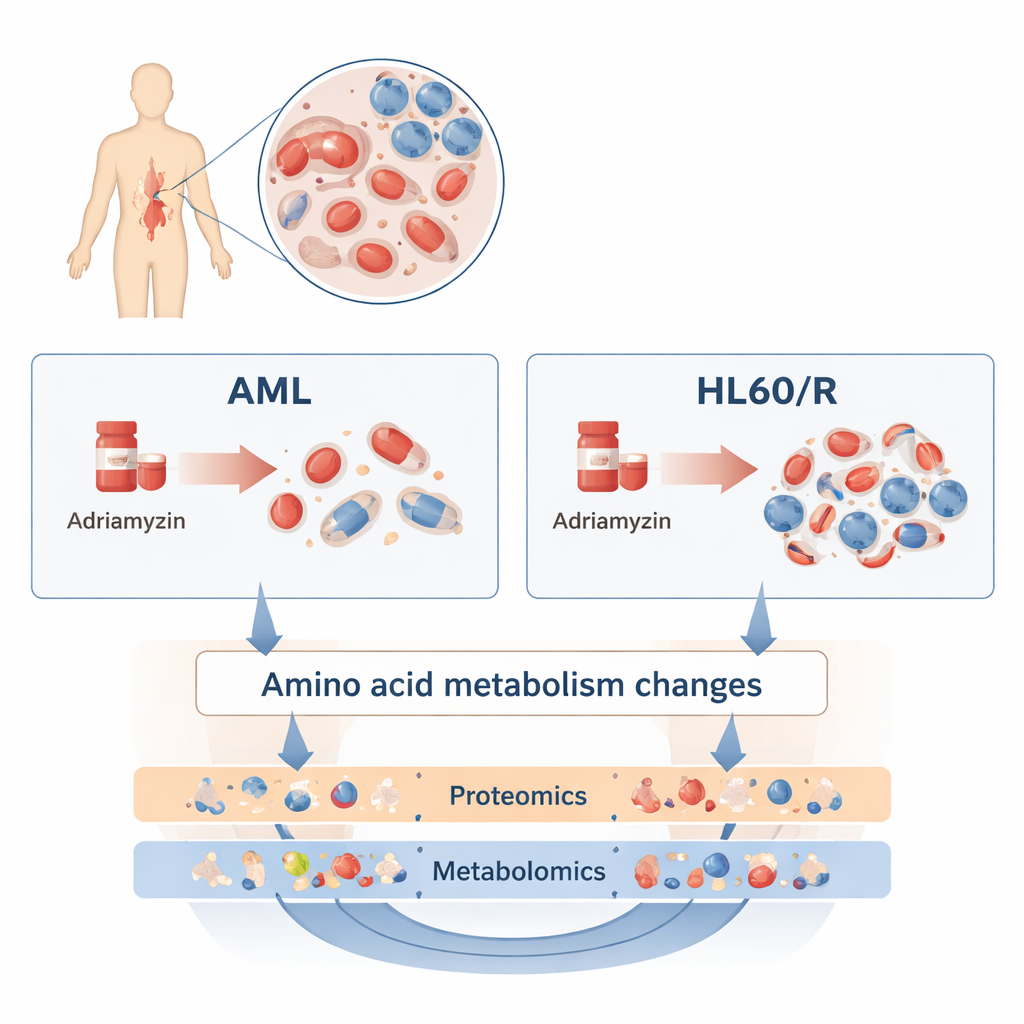
Масштабная перенастройка клеточной работы
Обзор протеома выявил масштабные изменения: более 3200 белков были представлены в изменённых количествах в клетках, устойчивых к адриамицину, по сравнению с обычными клетками HL60. Многие из этих белков сгруппировались в пути, контролирующие использование энергии и ответ на стресс. В частности, были изменены белки, связанные с cAMP‑сигнальным путём, путём HIF‑1 (помогающим клеткам адаптироваться к низкому содержанию кислорода) и окислительным фосфорилированием (основной процесс производства энергии в митохондриях). Эти сдвиги указывают на то, что устойчивые клетки лейкоза перепрограммируют способы «дыхания», роста и сигнализации, чтобы противостоять химиотерапии.
Метаболизм смещается в сторону аминокислот
Анализ метаболома дал дополнительную картину. Из примерно 1400 обнаруженных метаболитов 260 изменились значимо в устойчивых клетках. Статистические модели чётко разделили устойчивые и неустойчивые клетки, что указывает на устойчивый метаболический «отпечаток» резистентности. При отображении изменённых метаболитов на известные биохимические пути выделились несколько направлений. Многие наиболее затронутые пути были связаны с аминокислотами — строительными блоками белков, особенно с путями, включающими аланин, аспартат, глутамат, цистеин, метионин и глутатион. Были также нарушены сети пуринового и пиримидинового обмена (важные для ДНК и РНК) и обработка некоторых липидов, что подчёркивает: устойчивость связана с широкой метаболической перестройкой.
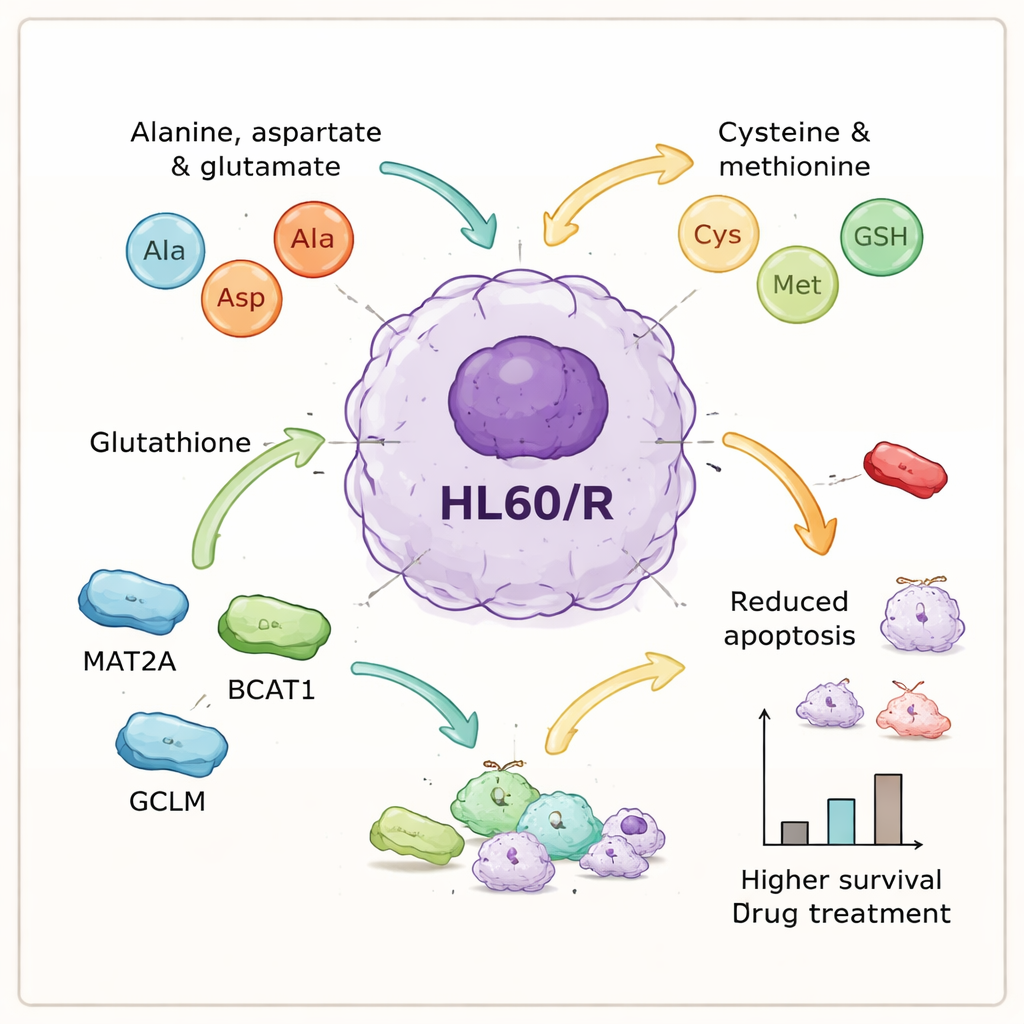
Ключевые молекулярные участники, помогающие клеткам выживать
Интегрируя данные по белкам и метаболитам, авторы выделили набор аминокислотно‑связанных процессов, которые казались центральными для резистентности. Они выбрали шесть белков, связанных с этими путями — GOT1, GPX1, AHCY, MAT2A, BCAT1 и GCLM — для более детального изучения. Лабораторные тесты подтвердили, что пять из них более многочисленны в устойчивых клетках, что согласуется с идеей усиленной переработки аминокислот, тогда как один антиоксидантный фермент, GPX1, был снижен. Чтобы проверить причинно‑следственные связи, команда использовала малые интерферирующие РНК для подавления трёх из повышенных белков — MAT2A, BCAT1 и GCLM — в устойчивых клетках. При их угнетении клетки значительно чаще вступали в программируемую гибель после лечения, то есть теряли большую часть приобретённой защиты от адриамицина.
Что это значит для будущих терапий
В совокупности результаты указывают на то, что клетки ОМЛ, устойчивые к адриамицину, выживают не только из‑за отдельных мутаций, но и потому, что они перестраивают свою внутреннюю химию, где обмен аминокислот становится центральным узлом. Перенаправляя больше ресурсов в определённые аминокислотные и глутатионовые пути, клетки, по‑видимому, лучше справляются со стрессом, ремонтируют повреждения и избегают гибели при воздействии химиопрепаратов. Для неспециалистов главный вывод таков: резистентность не случайна — она следует обнаружимым схемам, которые можно измерить и, возможно, целенаправленно блокировать. В перспективе препараты, мешающие специфическим белкам обработки аминокислот, таким как MAT2A, BCAT1 или GCLM, могли бы комбинироваться с адриамицином или подобными агентами, предоставляя клиницистам новые инструменты для предотвращения или преодоления резистентности у пациентов с острым миелоидным лейкозом.
Цитирование: Li, C., Liang, X., Gong, S. et al. Integrative analysis of proteomics and metabolomics reveals amino acid metabolism disorder in adriamycin-resistant acute myeloid leukemia cells. Sci Rep 16, 4902 (2026). https://doi.org/10.1038/s41598-026-35675-3
Ключевые слова: острый миелоидный лейкоз, лекарственная устойчивость, адриамицин, обмен аминокислот, мультиомика