Clear Sky Science · ru
Синтез, характеристика, DFT-анализ, молекулярное докирование и противораковое исследование при колоректальной карциноме нового комплекса цинка(II) с пиразол-гидразоном
Почему лекарство на основе металла может мягче бороться с раком толстой кишки
Многие сильнодействующие противораковые препараты основаны на тяжёлых металлах, таких как платина. Они могут быть эффективны, но зачастую сопровождаются жёсткими побочными эффектами и развитием резистентности со временем. В этом исследовании рассматривается иной подход: новый кандидат в лекарства, построенный вокруг цинка — жизненно важного микроэлемента, уже присутствующего в организме, — в сочетании с органическим остовом, называемым пиразол–гидразоном. Учёные спросили, может ли присоединение цинка к этому остову дать соединение, которое эффективно поражает клетки колоректального рака, при этом щадя здоровые клетки.
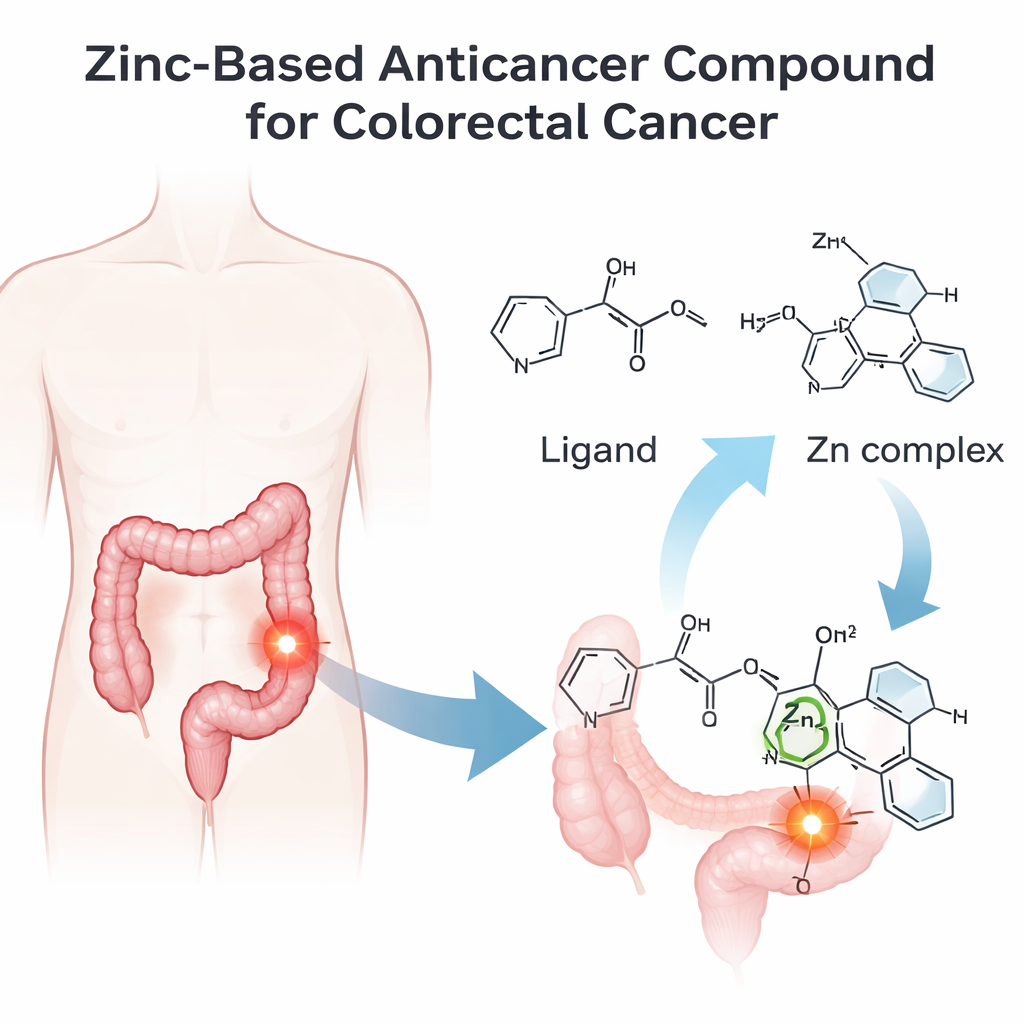
Создание более «умолекулы» на основе цинка
Команда сначала разработала и синтезировала новую органическую молекулу, обозначенную как IMP, а затем связала её с ионом цинка, чтобы получить цинковый комплекс IMP-Zn. Точная структура обоих веществ была подтверждена с помощью набора методов, которые фактически «снимали отпечаток» молекул: инфракрасной спектроскопии для определения химических связей, ядерного магнитного резонанса для картирования положения атомов, масс-спектрометрии для проверки молекулярной массы и УФ–видимой спектроскопии для изучения взаимодействия соединений со светом. Эти эксперименты вместе с тестами электропроводности показали, что цинк прочно координирован с тремя ключевыми атомами в IMP и двумя хлорид-ионами, образуя единственный, чётко определённый центрированный на цинке комплекс.
Заглядывая в молекулу с помощью виртуальной химии
В дополнение к лабораторным измерениям исследователи провели подробные компьютерные симуляции с использованием теории функционала плотности (DFT). Эти расчёты позволили предсказать распределение электронов в IMP и IMP-Zn, стабильность каждой формы и склонность молекул к участию в химических реакциях. Результаты показали, что после присоединения цинка энергетический разрыв между «фронтальными» орбиталями уменьшается, то есть электроны могут двигаться внутри структуры легче. Это обычно означает повышенную химическую реактивность. Цинковый комплекс также продемонстрировал более высокий так называемый индекс электрофильности, что указывает на его большую готовность взаимодействовать с биологическими мишенями по сравнению со свободным лигандом IMP.
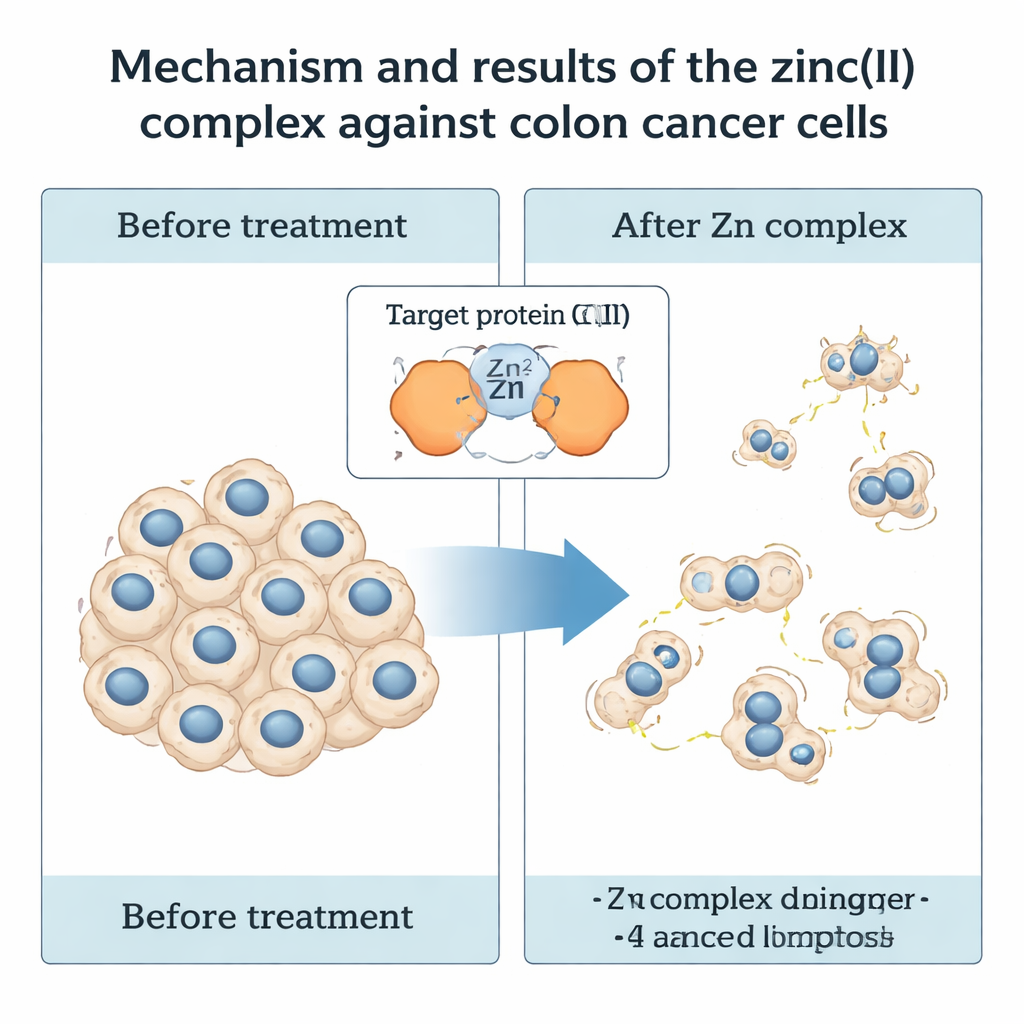
Как цинковый комплекс воздействует на клетки колоректального рака
Реальным испытанием стала биология. Исследователи обработали клетки человеческого колоректального рака (HCT116) препаратами IMP и IMP-Zn при различных дозах и времени воздействия и затем измерили выживаемость клеток. Оба соединения замедляли рост раковых клеток, но цинковый комплекс оказался явно сильнее: через 48 часов IMP-Zn снижал жизнеспособность клеток наполовину при концентрации около 25 микромоляр, тогда как лиганду в одиночку требовалась гораздо более высокая доза. Не менее важно, что те же концентрации IMP-Zn не вызывали обнаруживаемой токсичности в нормальной линии человеческих почечных клеток (HEK293), что указывает на некоторую селективность по отношению к раковым клеткам. При наблюдении обработанных клеток в течение двух недель команда обнаружила, что IMP-Zn значительно уменьшает как число, так и размер колоний, которые могут образовывать клетки, что свидетельствует о нарушении их способности к долгосрочному пролиферативному росту.
Улики, что клетки направляют к запрограммированной гибели
Чтобы понять, как цинковый комплекс повреждает раковые клетки, учёные изучили клеточный цикл — последовательность стадий, через которые проходят клетки при росте и делении. После воздействия IMP-Zn существенно большая доля HCT116 клеток смещалась в фазу «SubG0», характерную для клеток с фрагментированной ДНК. Такая картина обычно ассоциируется с апоптозом — контролируемой формой клеточной гибели, нацеленой многими противораковыми препаратами. Молекулярное докирование дало ещё одно подтверждение: виртуальные модели показали, что IMP-Zn связывается сильнее, чем IMP, с несколькими белками, связанными с раком, включая киназу рецептора фактора роста, киназу, регулирующую клеточный цикл, и фермент метаболизма лекарств. Эти более прочные взаимодействия поддерживают идею о том, что координация с цинком помогает соединению «зафиксироваться» на критических клеточных механизмах и нарушать выживание раковых клеток.
Что это может значить для будущих лечебных подходов
В целом исследование показывает, что «украшение» каркаса пиразол–гидразона цинком делает больше, чем просто изменяет его химию: оно превращает IMP в более реактивное, более мощное и, по-видимому, более селективное средство против клеток колоректального рака. Хотя IMP-Zn пока далёк от готового лекарства — ему ещё предстоит пройти испытания на животных и людях — его способность значительно замедлять рост клеток рака толстой кишки, направлять клетки к апоптозу и щадить нормальные клетки делает его многообещающим представителем растущего класса цинксодержащих металлорганических препаратов. Эта работа указывает на то, что тщательно спроектированные цинковые комплексы могли бы в будущем стать более мягкими, целенаправленными альтернативами или дополнениями к традиционной химиотерапии на основе металлов.
Цитирование: Mermer, A., Bayrak, A.M., Bolat, Z.B. et al. Synthesis, characterization, DFT analysis, molecular docking and anticancer investigations in colorectal carcinoma of a novel pyrazole-hydrazone zinc(II) complex. Sci Rep 16, 6391 (2026). https://doi.org/10.1038/s41598-026-35664-6
Ключевые слова: антираковые препараты на основе цинка, колоректальный рак, комплекс пиразол-гидразона, молекулярное докирование, апоптоз