Clear Sky Science · ru
Хлорированные бис-4-гидроксикумарины подавляют репликацию флавивирусов, ингибируя трансляцию и репликацию вируса денге типа 2
Новые надежды в борьбе с вирусами, переносимыми комарами
Вирусы денге и Зика инфицируют сотни миллионов человек ежегодно, зачастую в регионах с ограниченными медицинскими ресурсами. Вакцины дают лишь частичную защиту, и по‑прежнему нет широко применяемого противовирусного препарата, который врачи могли бы назначать на ранней стадии болезни. В этом исследовании рассматривается семейство синтетических соединений, созданных по образцу растительных молекул, с простым, но срочным вопросом: способны ли какие‑нибудь из них надежно замедлять эти вирусы внутри человеческих клеток, не вредя при этом самим клеткам?
Молекулы, вдохновлённые растениями, как блокаторы вирусов
Исследователи сосредоточились на кумаринах — классе природных соединений, обнаруживаемых во многих растениях и давно известных своими антимикробными и антивирусными свойствами. Они протестировали двенадцать производных «бискумарина» — состоящих из двух связанных друг с другом кумариновых звеньев — против вируса денге типа 2 и вируса Зика в культуре клеток. Измеряя, сколько инфекционных частиц вируса образуется, и насколько хорошо сохраняется жизнеспособность клеток, они обнаружили, что две хлорированные варианты, обозначенные как соединения 3 и 4, особенно многообещающи. При низких микромолярных концентрациях эти хлорированные бис-4-гидроксикумарины снижали образование вируса более чем на 90% при сохранении работоспособности большинства клеток.
Точная настройка химии для усиления защиты
Не все химические модификации работали одинаково эффективно. Систематически меняя атомы вокруг кольцевой части молекул, команда установила, что присоединение хлора в определённых позициях обеспечивает наилучшую антивирусную активность. Замена хлора на другие галогены, такие как фтор или бром, или добавление различных функциональных групп обычно ослабляли эффект против денге и Зика. С помощью компьютерного моделирования авторы связали силу антивирусного действия с простыми молекулярными характеристиками, такими как распределение заряда по молекуле и площадь её поверхности. Методы машинного обучения уловили эти зависимости гораздо лучше, чем традиционные статистические инструменты, что указывает на то, что искусственный интеллект может помочь направлять дизайн улучшенных кандидатов в противоденге препараты.
Как соединения нарушают жизненный цикл вируса
Попадая в клетку, вирус денге использует свою РНК как шаблон для синтеза длинного полипротеина, который затем расщепляют на рабочие компоненты, и копирует свою РНК для порождения новых вирусов. Исследование показывает, что соединения 3 и 4 в основном мешают этим этапам трансляции и репликации. В инфицированных клетках уровни ключевого белка оболочки вируса резко снижались при наличии соединений, а репортерная система, отслеживающая репликацию вирусной РНК, также подавлялась в дозозависимой манере. Биохимические тесты и компьютерный докинг указали на один вирусный фермент, NS5 метилтрансферазу, как на прямую, но относительно слабую мишень: соединения могли ингибировать функцию «капирования» РНК, хотя и значительно слабее, чем известный эталонный ингибитор. Они также умеренно замедляли работу вирусной протеазы — другого фермента, участвующего в расщеплении полипротеина.
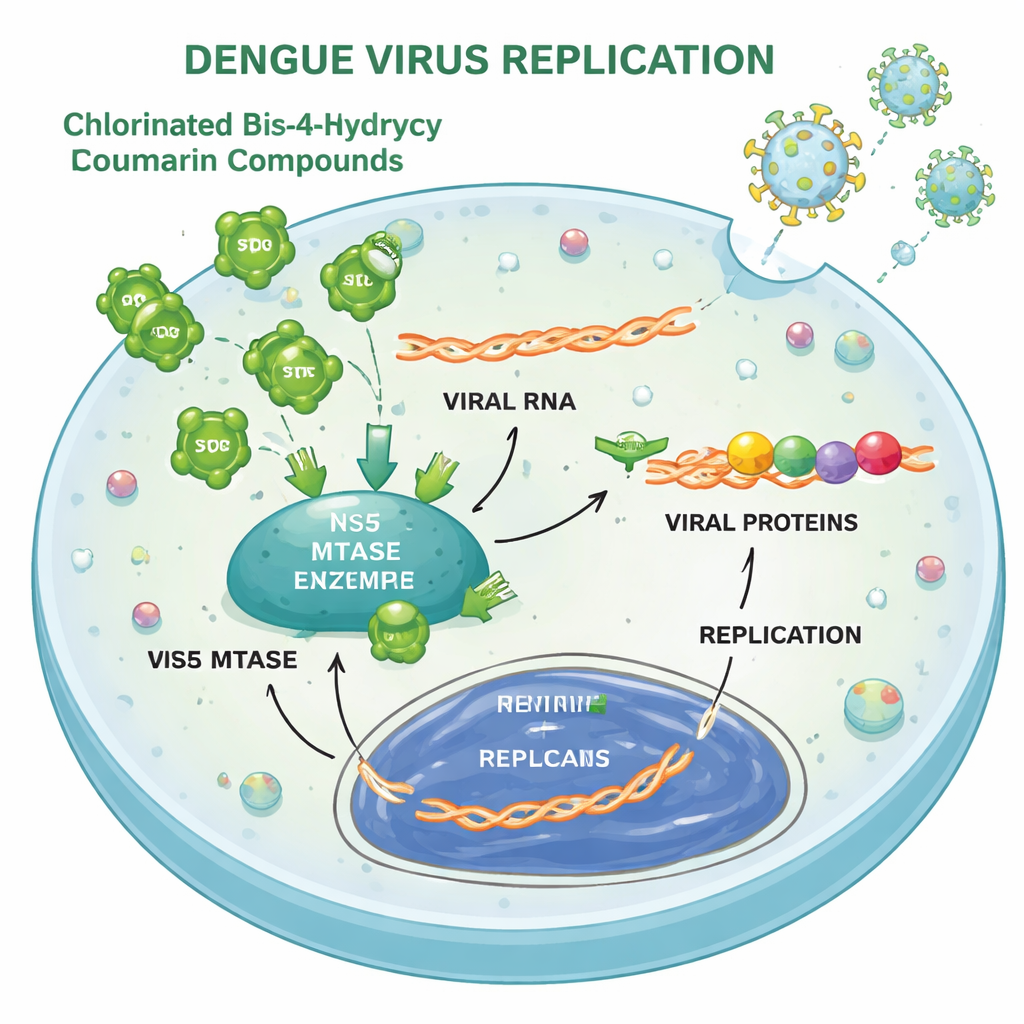
Вирусам трудно адаптироваться к атаке
Вирусы часто избегают действия лекарств путём мутаций. Чтобы проверить, может ли это произойти в данном случае, команда многократно выращивала вирус денге в клетках, окружённых новыми соединениями, в течение многих циклов инфекции. Появились несколько изменений в другом вирусном белке, NS4B, который помогает изгибать мембраны клетки в небольшие карманы, где происходит репликация. Удивительно, но мутировавшие вирусы не стали менее чувствительны к соединениям по сравнению с исходным штаммом. Компьютерно предсказанные структуры показали, что общая форма NS4B осталась в основном прежней. Эта картина указывает на то, что мутации были общими адаптациями к стрессу, а не на настоящую резистентность. Это также поддерживает идею о том, что соединения действуют на несколько частей репликационного аппарата или на факторы хозяина, которые вирусу трудно перестроить.
Почему эти результаты важны для будущих терапий
Для неспециалистов главный вывод таков: исследователи выявили новую химическую «скелетную структуру», которая способна замедлять вирусы денге и Зика на нескольких этапах их жизненного цикла, особенно при попытке вирусов транслировать свои гены и копировать РНК внутри клеток. Наиболее перспективная молекула, соединение 3, действует при низких дозах, относительно мало повреждает клетки, эффективна против всех четырёх основных типов вируса денге, а также против Зика, и в лабораторных условиях не вызывает быстрой эволюции резистентности у вируса. Хотя эти хлорированные бис-4-гидроксикумарины ещё далеко до статуса лекарств, они дают прочную отправную точку для химиков и вирусологов, чтобы дорабатывать соединения, тестировать их на животных и в конечном счёте комбинировать с другими препаратами — шаги, которые могут приблизить нас к столь необходимой противовирусной таблетке против инфекций, переносимых комарами.
Цитирование: Loeanurit, N., Phan, THT., Hengphasatporn, K. et al. Chlorinated bis-4-hydroxycoumarins suppress flavivirus replication by inhibiting dengue virus type 2 translation and replication. Sci Rep 16, 5300 (2026). https://doi.org/10.1038/s41598-026-35654-8
Ключевые слова: вирус денге, вирус Зика, антивирусные соединения, производные кумарина, вирусная репликация