Clear Sky Science · ru
Хемосенсорный ответ на химиотерапевтические препараты на основе платины через рецепторы горького вкуса in vitro выявляет новый механизм нарушений вкуса
Почему противораковые препараты внезапно делают всё на вкус отвратительным
Пациенты с раком часто сообщают, что еда начинает казаться странно горькой или металлической вскоре после начала химиотерапии. Это не просто портит приёмы пищи: такое изменение вкуса может уменьшать аппетит, вызывать потерю веса и снижать качество жизни именно в тот момент, когда пациентам нужна сила. В этом исследовании поставлен внешне простой, но важный практический вопрос: как именно распространённые препараты на основе платины нарушают нашу способность ощущать вкус и можно ли ослабить этот эффект, не снижая эффективности лечения?
Скрытая роль «датчиков горечи» во рту и кишечнике
Наш язык и пищеварительный тракт усеяны рецепторами горького вкуса, созданными для предупреждения о потенциально вредных веществах. Эти датчики, известные как TAS2R, расположены не только на вкусовых почках; они также присутствуют в клетках желудка. Исследователи использовали линию человеческих желудочных клеток (HGT-1), которая функционирует как in vitro-детектор горечи: при активации горьких рецепторов клетки выбрасывают больше протонов (кислоты), что измеряют по показателю, называемому индексом внутриклеточных протонов. Воздействуя на эти клетки двумя широко применяемыми препаратами на основе платины — карбоплатином и цисплатином — команда могла безопасно оценить, насколько «горькими» эти препараты выглядят для человеческих клеток, не прибегая к тому, чтобы человек пробовал токсичное вещество. 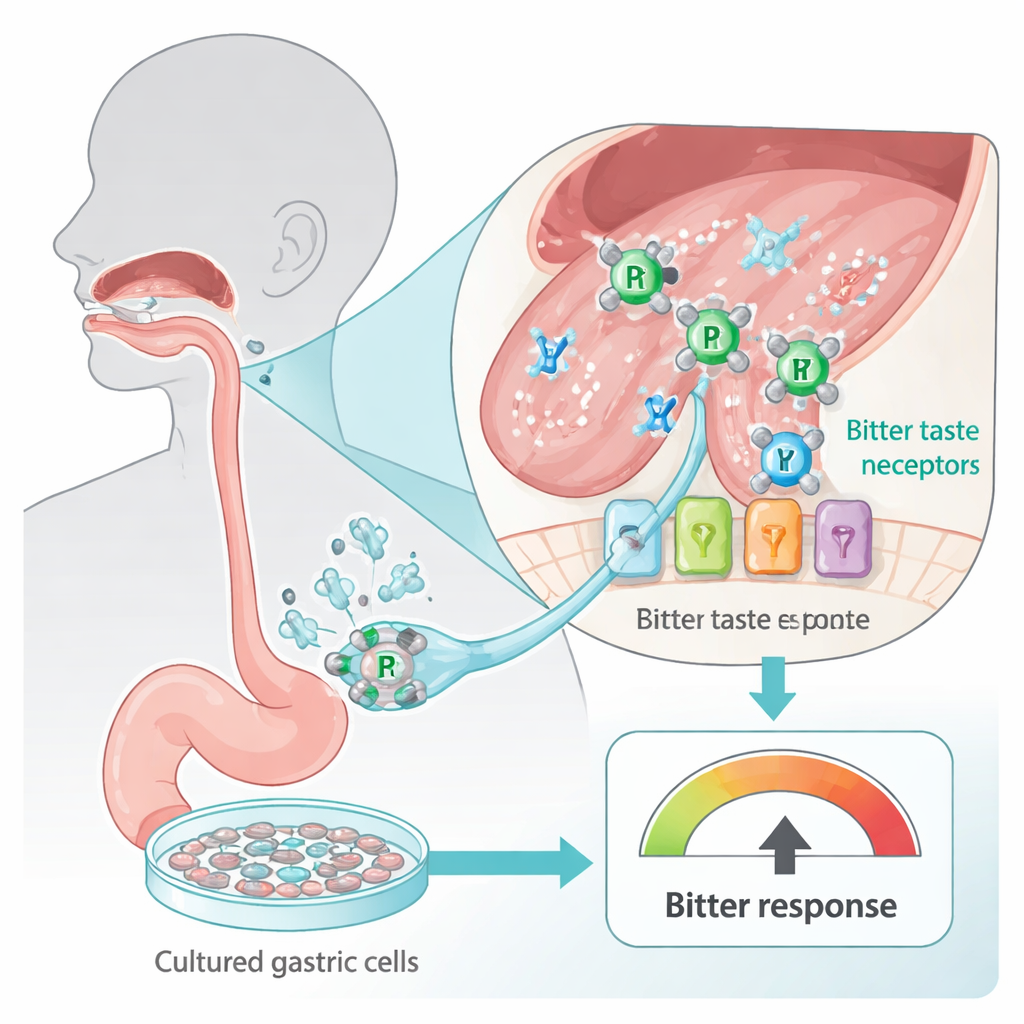
Химиопрепараты, которые для клеток кажутся горькими
Когда желудочные клетки обрабатывали клинически релевантными концентрациями карбоплатина и цисплатина, оба препарата вызвали чёткий, зависимый от дозы ответ, похожий на горечь: чем выше доза, тем сильнее реакция клеток. Однако цисплатин давал более интенсивный ответ, чем карбоплатин, если учитывать их обычное терапевтическое соотношение доз (примерно 1:4), что говорит о том, что он может сильнее способствовать проблемам с горьким вкусом у пациентов. На генетическом уровне воздействие этих препаратов изменяло активность множества генов рецепторов горечи в клетках, указывая на то, что платиновые препараты не действуют через один «переключатель горечи», а широко перестраивают систему распознавания горечи. Среди этих рецепторов выделялись TAS2R4 и TAS2R5 как особенно активные и сильно затронутые лечением.
Выключение сигналов горечи и испытание природного блокатора горечи
Чтобы уточнить, какие рецепторы имеют наибольшее значение, команда выборочно деактивировала отдельные рецепторы горечи. Удаление TAS2R4 или снижение экспрессии TAS2R5 по отдельности уменьшало ответ, похожий на горечь, на карбоплатин и цисплатин, что подтвердило роль этих рецепторов в распознавании препаратов. Затем учёные протестировали перспективное контрмеры: натриевую соль гомоэриодиктиола (Na-HED), флаванона, впервые выделенного из североамериканского растения Herba Santa и уже известного способностью маскировать горечь других соединений. Когда Na-HED добавляли вместе с платиновыми препаратами, он заметно подавлял клеточный горький ответ — примерно на три четверти для обоих препаратов — не оказывая при этом вредного воздействия на клетки сам по себе. Это показывает, что Na-HED может действовать непосредственно на рецепторы горечи, ослабляя сигнал, вызываемый химиопрепаратами.
Когда распознавание горечи и поглощение препарата пересекаются
Помимо объяснения того, почему платиновая химиотерапия может казаться горькой, исследование выявляет неожиданный поворот: те же рецепторы горечи, по-видимому, влияют и на количество препарата, попадающего в клетки. С помощью очень чувствительной масс-спектрометрии исследователи измеряли содержание платины внутри клеток после обработки. Клетки, лишённые определённых рецепторов, таких как TAS2R4 или TAS2R43, накапливали больше платины, чем нормальные клетки, что предполагает, что интактные рецепторы помогают ограничивать клеточное поглощение или удержание этих токсичных агентов. Na-HED не изменял поглощение карбоплатина, но уменьшал, сколько цисплатина проникало в клетки, и демонстрировал прямое молекулярное взаимодействие с цисплатином в растворе. Это наводит на мысль, что соединение, маскирующее горечь, в некоторых случаях может также модулировать силу воздействия препарата на локальные ткани, такие как вкусовые клетки или слюнные железы. 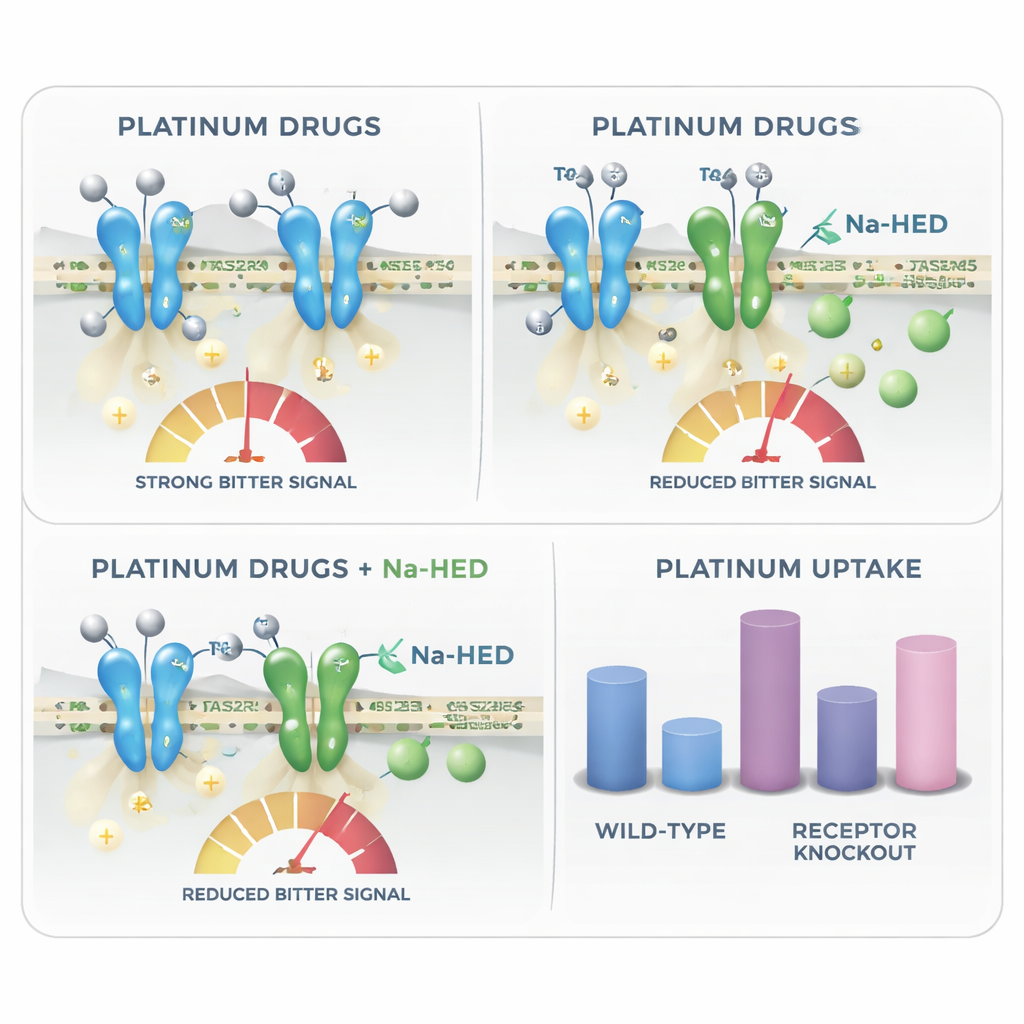
К более мягким вкусовым ощущениям во время химиотерапии
Для пациентов главный вывод даёт надежду: платиновая химиотерапия, по-видимому, вызывает проблемы с горьким вкусом путём прямой активации рецепторов горечи, которые присутствуют не только на языке, но и в клетках, похожих на клетки кишечника. Цисплатин в этом отношении выглядит особенно мощным. Исследование показывает, что Na-HED способен значительно приглушать этот горький сигнал в контролируемой клеточной системе и может также ограничивать локальное поглощение цисплатина. Хотя эти результаты необходимо подтвердить на людях, они указывают на перспективу будущих полосканий или ополаскивателей для рта с Na-HED, которые могли бы смягчить резкие горькие и металлические ощущения, не вмешиваясь в противораковое действие препаратов по всему организму.
Цитирование: Zehentner, S., Mistlberger-Reiner, A., Pirkwieser, P. et al. Chemosensory response to Pt-based chemotherapeutics via bitter taste receptors in vitro reveals a new mechanism for bitter taste disorders. Sci Rep 16, 2634 (2026). https://doi.org/10.1038/s41598-026-35636-w
Ключевые слова: изменения вкуса при химиотерапии, рецепторы горького вкуса, цисплатин и карбоплатин, средства маскировки горечи, питание пациентов с раком