Clear Sky Science · ru
Вычисления DFT комплексообразования Ac3+ и Bi3+ с гибридным хелатором 3p-C-DEPA для таргетной альфа-терапии
Почему это исследование важно для лечения рака
Современная онкология все чаще опирается на радиоактивные препараты, которые способны находить опухолевые клетки буквально поодиночке. Мощный подход, называемый таргетной альфа-терапией, использует высокоэнергичные частицы, способные с высокой точностью уничтожать отдельные раковые клетки. Но чтобы доставить такие частицы безопасно, радиоактивный металл нужно надежно заключить в крошечную молекулярную «клетку», чтобы он не попал в здоровые ткани. В этой работе исследуется новая молекула-клетка, 3p‑C‑DEPA, разработанная для удержания особенно сложных металлов, таких как актиний‑225 и висмут‑213, и поставлен вопрос: может ли она связывать их прочнее, чем нынешний стандартный хелатор DOTA?
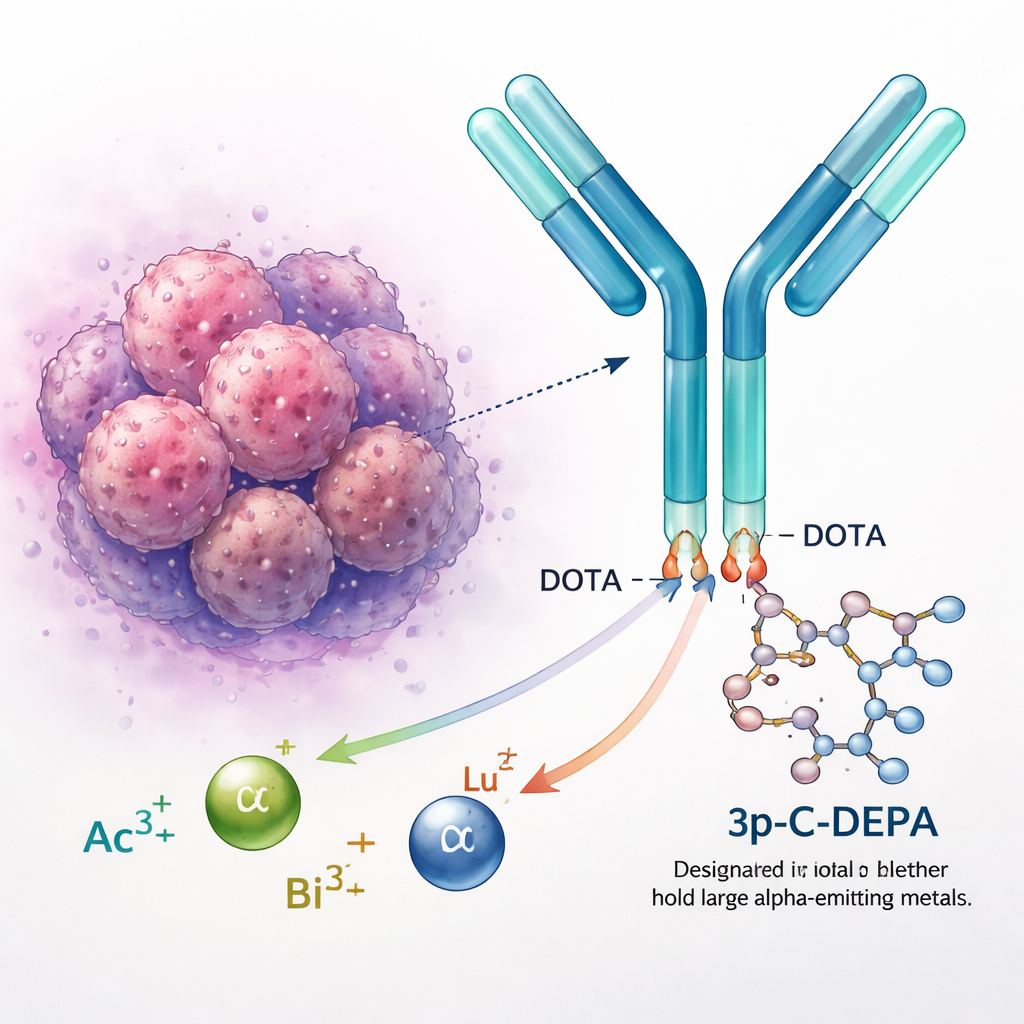
Надежное закрепление радиоактивных металлов
Радиоактивные металлы, такие как актиний, висмут и лютеций, используются для диагностики и лечения рака. Однако в свободном виде эти положительно заряженные ионы металлов могут взаимодействовать с организмом и потенциально повреждать здоровые органы. Поэтому химики привязывают их к «хелаторам» — кольцевым молекулам, которые обвивают металл и удерживают его на месте. Эталонный хелатор DOTA применяется во многих одобренных препаратах, но испытывает трудности с более крупными и рассеянными ионами, такими как актиний‑225. Такие металлы со временем могут выскользнуть, что вызывает опасения по поводу долгосрочной безопасности и ограничивает распространение таргетной альфа-терапии.
Гибридная «клетка», рассчитанная на крупные атомы
Новый хелатор 3p‑C‑DEPA объединяет черты двух известных конструкций: жесткую, кольцеобразную систему DOTA и более гибкую, открытую структуру другого хелатора, DTPA. Такая гибридная архитектура дает 3p‑C‑DEPA десять сильных «рук» для связывания (атомов азота и кислорода) по сравнению с восьмью у DOTA, а также более просторную полость, которая лучше вмещает крупные ионы металлов. Предыдущие лабораторные работы показали, что 3p‑C‑DEPA может быстро мечетить антитела при мягких условиях и надежно удерживать радионуклиды на основе висмута в сыворотке крови. Текущее исследование делает следующий шаг: с помощью квантово‑уровневых расчетов систематически сравниваются способности 3p‑C‑DEPA и DOTA связывать лютеций‑177, висмут‑213 и актиний‑225.
Заглядывая в молекулярное рукопожатие
Поскольку работа с короткоживущими альфа-излучателями затруднена, исследователи обратились к теории функционала плотности (DFT) — мощному вычислительному методу, который оценивает распределение электронов в молекулах и силу взаимного притяжения атомов. Они смоделировали каждый ион металла в водной среде, затем его комплекс с DOTA или 3p‑C‑DEPA и рассчитали изменение свободной энергии при переходе металла из воды в «клетку» хелатора. Это изменение энергии переводится в «константу стабильности»: чем выше значение, тем крепче хелатор удерживает металл. Для проверки надежности выводов использовались два разных подхода DFT и две модели сольватации, имитирующие реалистичные условия раствора и исключающие артефакты одной вычислительной схемы.
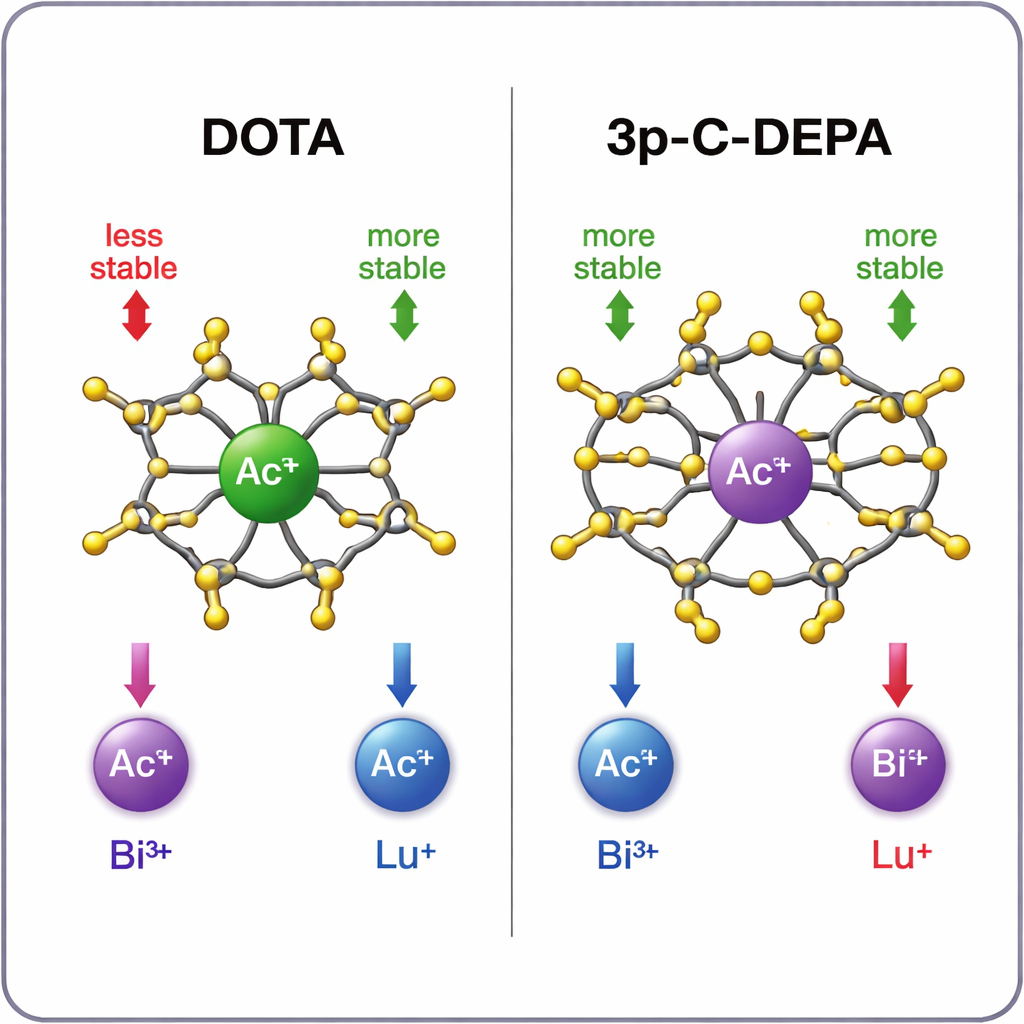
Какая «клетка» лучше держит какой металл?
Симуляции показывают четкую картину. Для большого иона актиния 3p‑C‑DEPA формирует заметно более стабильный комплекс, чем DOTA, благодаря своей большей полости и большему числу кислородных доноров, которые могут крепко охватить металл. Висмут‑213 также хорошо устраивается в 3p‑C‑DEPA, выигрывая и за счет размера, и за счет своей электроноакцепторной природы, хорошо сочетающейся с электроноотдающими группами хелатора. Напротив, более маленький лютеций‑177 удобнее размещается в тесной, восьмирукой среде DOTA. В 3p‑C‑DEPA избыточные донорные группы оказываются слишком близко к небольшому иону, создавая отталкивающие взаимодействия, которые, по-видимому, замедляют мечение и несколько ослабляют итоговый комплекс. Рассчитанные тренды стабильности хорошо согласуются с доступными экспериментальными данными и выходами радиомечения, что придает доверия теоретическим предсказаниям.
Что это означает для будущих методов лечения рака
Проще говоря, исследование указывает на то, что DOTA не является универсальной «клеткой»: она отлично работает для более мелких металлов, таких как лютеций, но не оптимальна для громоздких альфа‑излучателей вроде актиния‑225. 3p‑C‑DEPA, напротив, ведет себя как специально сконструированный держатель для этих больших ионов, крепко удерживая их и при более мягких условиях, подходящих для чувствительных молекул‑мишеней, таких как антитела. Хотя необходимы дальнейшие экспериментальные и клинические исследования, вычисления выделяют 3p‑C‑DEPA как перспективную основу для более безопасной и эффективной таргетной альфа‑терапии — что потенциально расширит доступ к очень мощным методам лечения рака, способным уничтожать опухоли при минимальном вреде окружающим тканям.
Цитирование: Ramdhani, D., Watabe, H., Ahenkorah, S. et al. DFT calculation of Ac3+ and Bi3+ complexation with hybrid chelator 3p-C-DEPA for targeted alpha therapy. Sci Rep 16, 6587 (2026). https://doi.org/10.1038/s41598-026-35633-z
Ключевые слова: таргетная альфа-терапия, радиофармацевтика, проектирование хелаторов, актиний-225, теория функционала плотности