Clear Sky Science · ru
Протеомика и редокс-протеомика в изучении гетерогенности ОРДС
Почему это важно для пациентов в отделении интенсивной терапии
Острый респираторный дистресс-синдром (ОРДС) — угрожающее жизни нарушение функции лёгких, которое может развиться у людей с тяжёлыми инфекциями, травмами или другими критическими заболеваниями. Многие пациенты с ОРДС на вид похожи у кровати, но одни выздоравливают, а другие — нет, и ни одно лекарство до сих пор не доказало способность специально обратить синдром вспять. В этом исследовании поставлен простой, но важный вопрос: если всесторонне изучить белки и химические реакции в лёгких и крови пациентов с ОРДС, можно ли выявить скрытые биологические «типы» болезни, которые объясняют, почему исходы у пациентов так сильно различаются?
Смотреть в сами лёгкие, а не только в кровь
Чтобы ответить на этот вопрос, исследователи наблюдали 16 взрослых пациентов в отделении интенсивной терапии с ОРДС, получавших аппаратную вентиляцию лёгких. В течение первых трёх дней после постановки диагноза они брали кровь и специальный образец — жидкость бронхоальвеолярного лаважа (БАЛ), представляющую собой мягкое промывание альвеол лёгких. По возможности эти заборы повторяли в последующие дни. С помощью высокоточного масс-спектрометра они измеряли сотни белков в каждом образце (протеомика) и, что особенно важно, исследовали степень окисления некоторых из этих белков (редокс-протеомика), что отражает, насколько они повреждены или регулируются реактивными формами кислорода — химически активными продуктами воспаления.
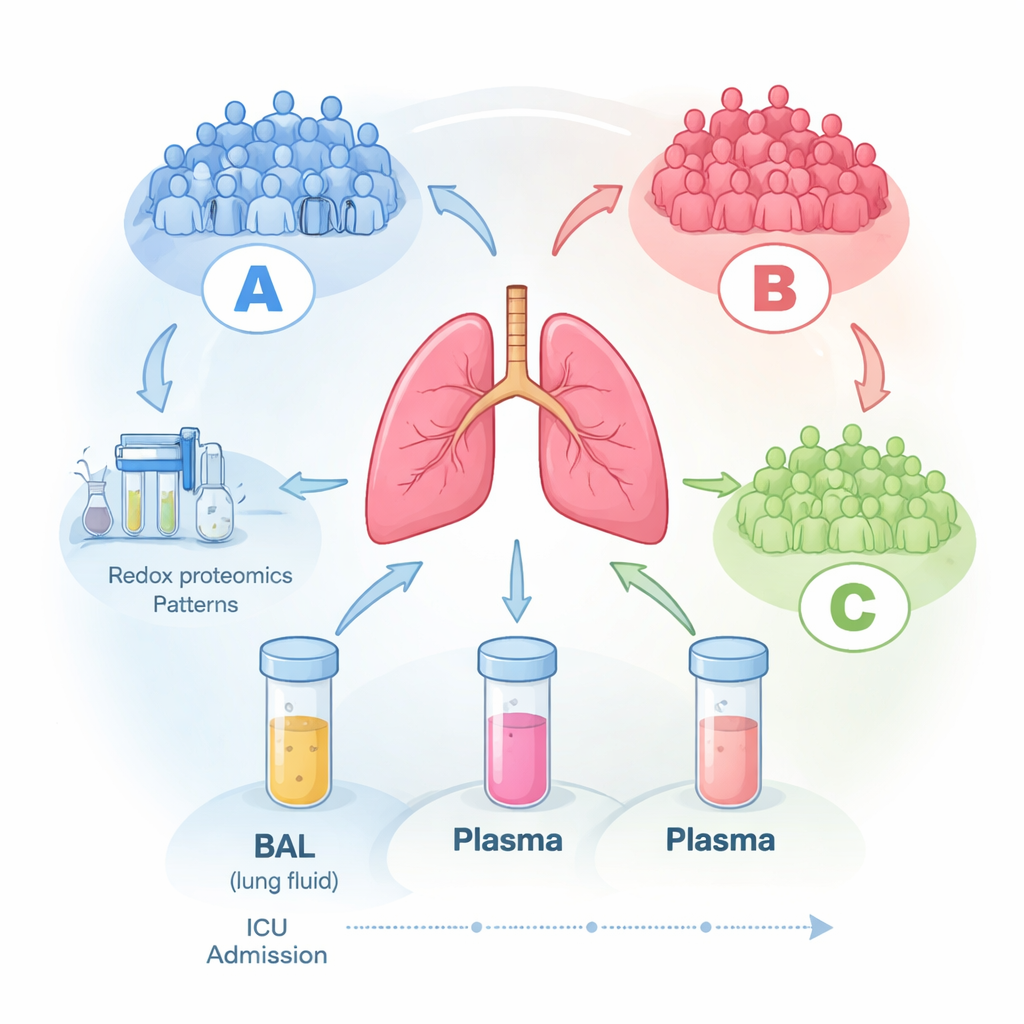
Выявлены три скрытые группы пациентов
Когда команда позволила данным самой формировать группы без какого-либо предварительного указания о пациентах, в образцах жидкости лёгких проявилась чёткая картина: три отчётливые молекулярные кластеры, обозначенные A, B и C. Пациенты из группы A при поступлении, как правило, были тяжелее, тогда как в группах B и C заболевание протекало мягче. Поразительно, что эти молекулярные подписи оставались в основном стабильными в течение до шести дней в реанимации, что говорит о том, что у каждого пациента наблюдается относительно постоянный биологический профиль, а не случайные дневные колебания. Стандартные клинические показатели — такие как уровень кислорода, продолжительность пребывания или общие шкалы тяжести — плохо коррелировали с этими молекулярными группами, что намекает на то, что обычные инструменты пропускают ключевую биологию, происходящую в лёгких.
Оксидативный стресс и защитные механизмы организма
Главной темой в данных была равновесие между повреждающими реактивными формами кислорода и антиоксидантной защитой организма. В группе A, самой тяжёлой, многие лёгочные белки, участвующие в энергообеспечении и клеточной «уборке», были представлены в меньших количествах. Ещё важнее: ключевые антиоксидантные ферменты, такие как пероксиоредоксины, белки, связанные с глутатионом, тиоредоксин и каталаза, были значительно снижены. В отличие от этого, в группах B и особенно C уровни этих защитных белков были выше, что говорит о том, что у их лёгких был лучший потенциал детоксикации вредных окислителей и ограничения сопутствующего воспалению повреждения. Состояние окисления белков добавляло ещё один уровень информации — разные наборы окисленных белков были обогащены в самых тяжёлых и самых лёгких группах.
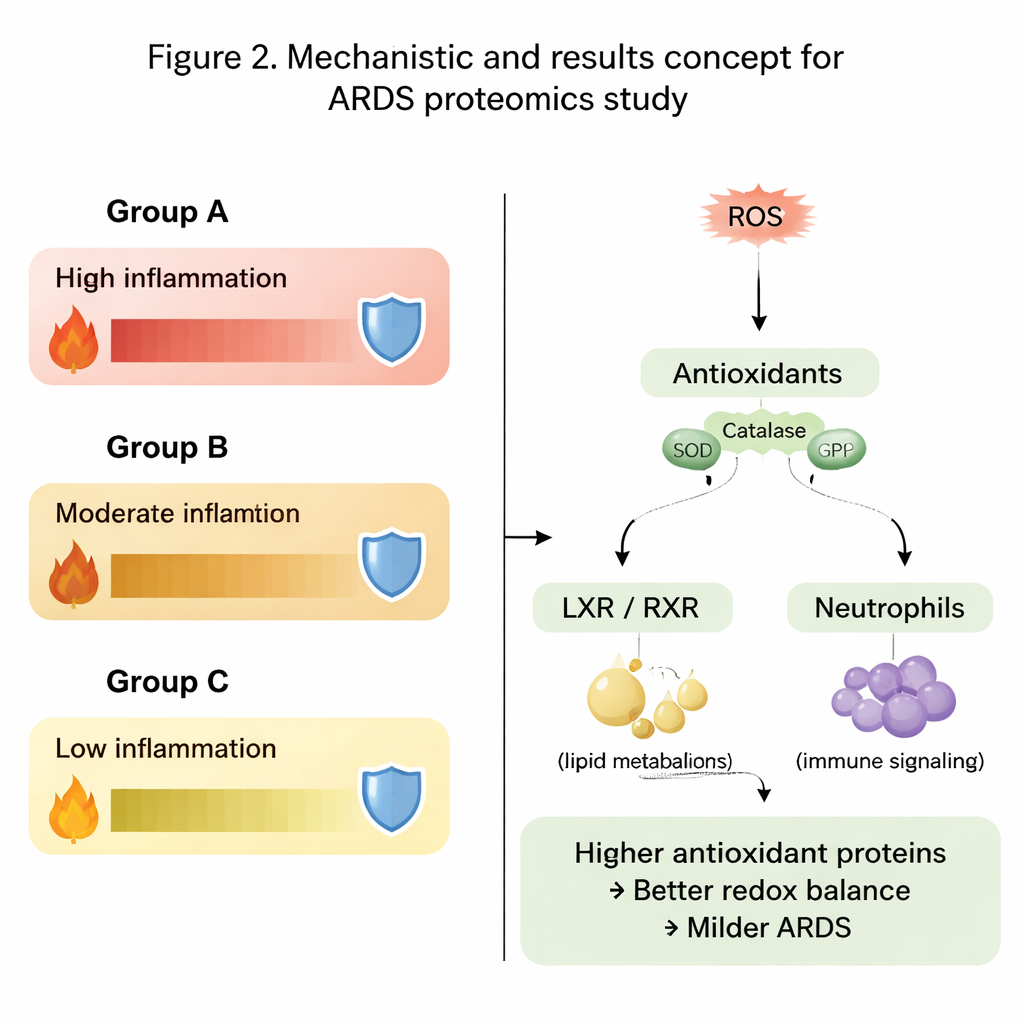
Сигнальные пути, формирующие воспаление
Помимо отдельных белков авторы изучили целые биологические пути. Они обнаружили, что пути, связанные с воспалением, обращением холестерина и липидов, а также активностью иммунных клеток, ведут себя по-разному в трёх группах. Особое внимание привлекли сигналы, связанные с рецептором печёночного X-рецептора–ретиноидным X-рецептором (LXR/RXR) и ферментом DHCR24, которые совместно регулируют как обмен липидов, так и иммунные ответы. В самой тяжёлой группе эти пути, по прогнозам, были более активны, при этом сигналы иммунного медиатора интерлейкина‑12 были понижены. Одновременно пути, связанные с реактивными формами кислорода, их детоксикацией и активностью нейтрофилов (лейкоцитов), показали противоположные закономерности в жидкости лёгких и в крови, подчёркивая, что локальные процессы в лёгких могут отличаться от того, что видно в системном кровообращении.
Что это может означать для будущей помощи
Это небольшое, первичное исследование не меняет текущую терапию и требует подтверждения в значительно больших когортах пациентов. Тем не менее оно демонстрирует, что при тщательном профилировании белков и их редокс‑состояния непосредственно в жидкости лёгких — а не только по анализам крови или оценкам у койки больного — можно выделить биологически значимые подтипы ОРДС. Эти подтипы различаются по уровню оксидативного стресса, антиоксидантной ёмкости, метаболизму и иммунной сигнализации и остаются относительно стабильными в первые критические дни болезни. В будущем такие молекулярные отпечатки могут помочь врачам точнее классифицировать пациентов с ОРДС, подбирать таргетную терапию под конкретный профиль и проектировать более умные клинические испытания с лучшими шансами найти действительно эффективные лечения.
Цитирование: Forshaw, T.E., Shukla, K., Wu, H. et al. A proteomics and redox proteomics approach to understanding ARDS heterogeneity. Sci Rep 16, 6034 (2026). https://doi.org/10.1038/s41598-026-35606-2
Ключевые слова: острый респираторный дистресс-синдром, протеомика, оксидативный стресс, бронхоальвеолярный лаваж, реанимация