Clear Sky Science · ru
Эффективность и безопасность криоаблации при моделях рака мочевого пузыря на мышах
Замораживание опухолей вместо удаления мочевого пузыря
Для многих пациентов с распространённым раком мочевого пузыря стандартное лечение подразумевает полное удаление органа — операция, полностью меняющая привычный образ мочеиспускания. В этом исследовании рассматривается принципиально иная идея: применение экстремального холода для уничтожения опухолей при сохранении самого пузыря. Испытания этой методики на мышах позволили авторам задать важный для пациентов и их семей вопрос: может ли более простая, сохраняющая орган процедура контролировать рак, поддерживать относительно нормальное мочеиспускание и даже помочь собственной иммунной системе бороться с заболеванием?
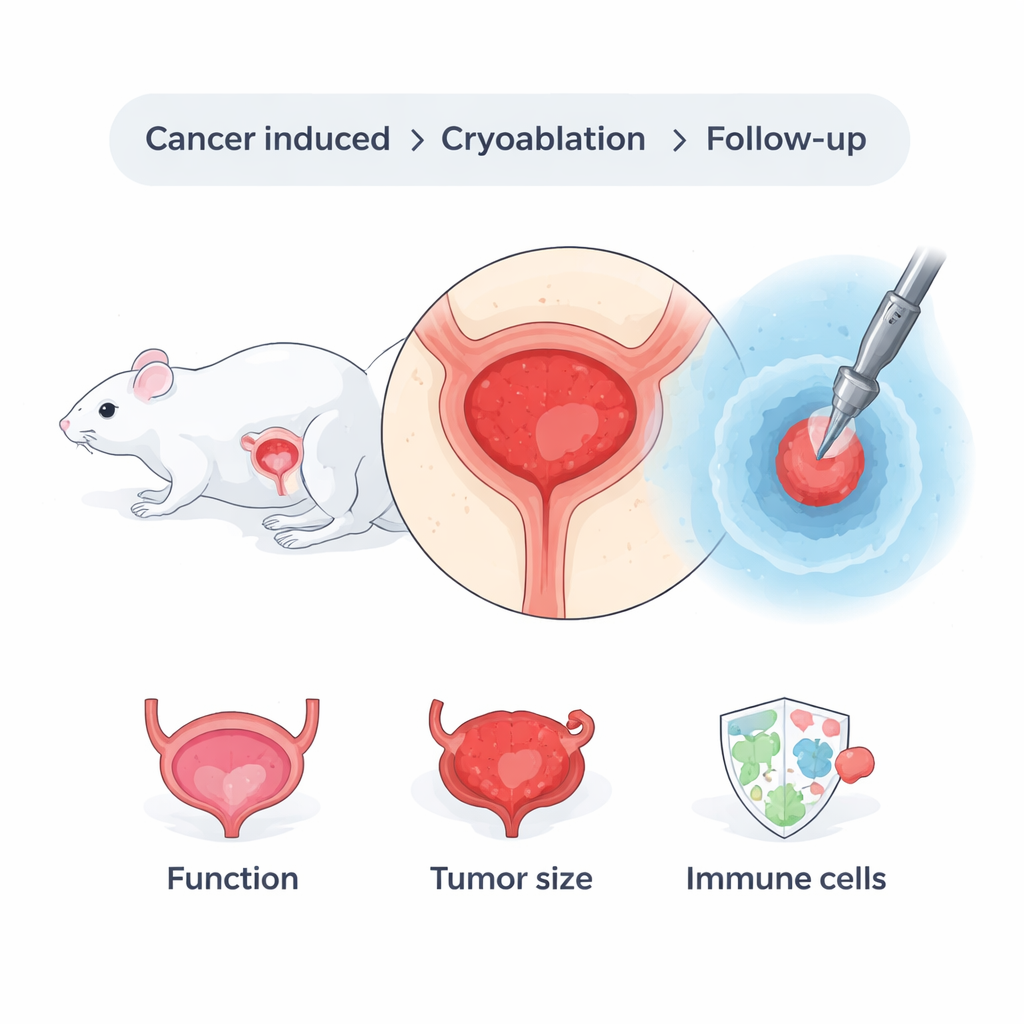
Почему удаление пузыря так тяжело даётся пациентам
Рак мочевого пузыря часто делят на два основных типа: опухоли, остающиеся на поверхности, и те, которые прорастают в мышечную стенку. Когда опухоль захватывает мышцу, обычное лечение — радикальная цистэктомия, то есть удаление всего мочевого пузыря. Хотя операция спасает жизни многих пациентов, она крайне инвазивна и требует от хирургов перенаправить отток мочи в резервуар на коже или в хирургически сформированный мешок. Такие изменения серьёзно снижают качество жизни, особенно у пожилых или ослабленных пациентов, которым порой даже противопоказана крупная операция. Поскольку у процедуры не идеальные показатели выживаемости, врачи и пациенты давно ищут альтернативы, которые были бы одновременно эффективны и менее тяжёлы для организма.
Как проверяли методику замораживания
Для изучения одной из таких альтернатив исследователи использовали хорошо известный метод индукции рака мочевого пузыря у мышей — добавление химического вещества BBN в питьевую воду. В течение нескольких месяцев у большинства животных развивались опухоли с прорастанием в мышечный слой, что моделировало опасную форму болезни у людей. После появления опухолей учёные хирургически обнажали пузырь через небольшое брюшное разрез и прижимали металлический стержень, предварительно охладённый в жидком азоте, к наружной поверхности поражённого пузыря. Это формировало строго контролируемый «ледяной шар», который замораживал ткань в двух коротких циклах замораживания–оттаивания. Другие мыши подвергались анестезии и вскрытию брюшной полости без замораживания и служили контрольной группой, показывая, что происходит без процедуры.
Действительно ли замораживание убивает рак и сохраняет функцию?
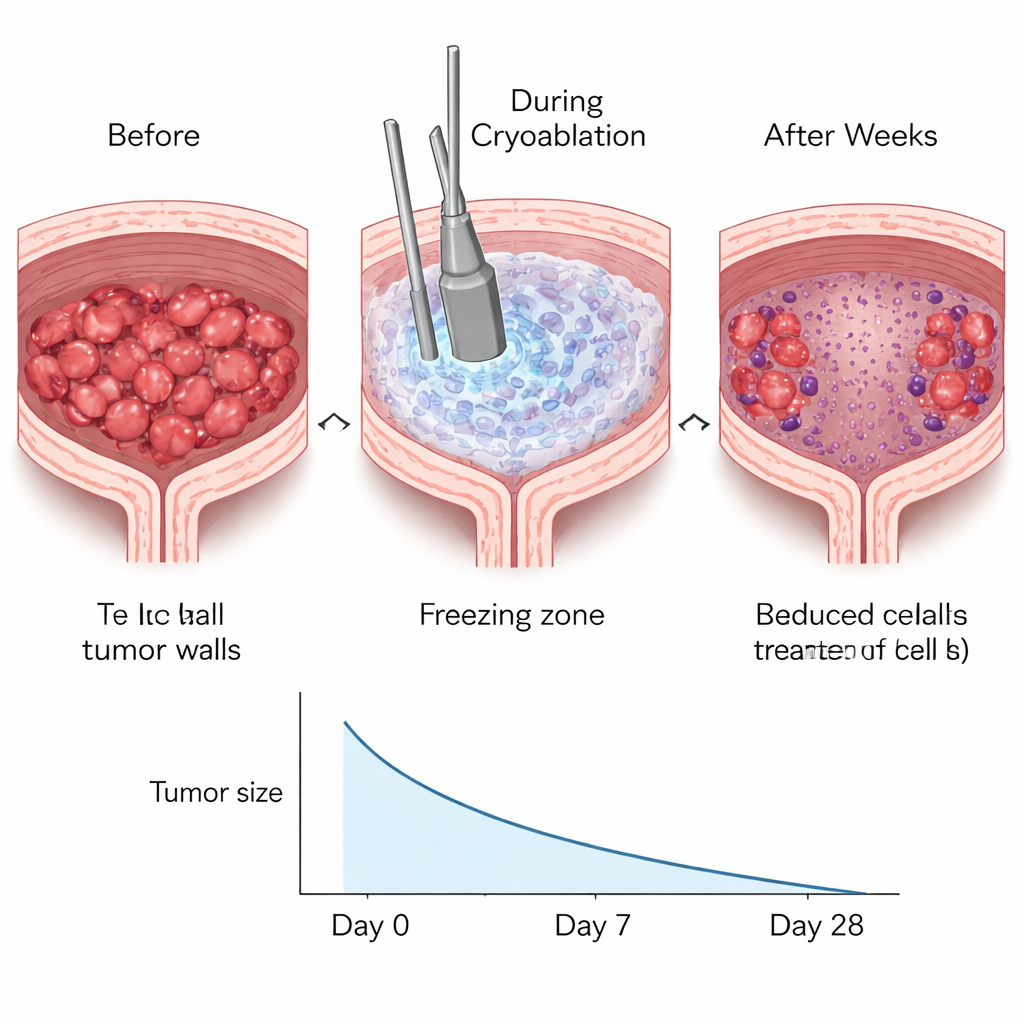
Тщательное микроскопическое исследование тканей мочевого пузыря показало, что процедура замораживания эффективно уничтожала раковые клетки в обработанных областях. В течение нескольких часов замороженные зоны выглядели повреждёнными: исчезали ядра гладкомышечных клеток и образовывались пустоты там, где клетки погибли. В последующие дни эти повреждённые участки уменьшались в размерах и примерно через две недели во многом заменялись соседней тканью. Размер опухолей заметно снижался в течение недель после процедуры. При этом мыши продолжали пить, мочиться и сохранять массу тела на уровне, сопоставимом с не оперированными животными. Простой тест с подсчётом пометок мочи на бумаге показал, что частота мочеиспускания не ухудшалась, что указывает на сохранение базовой функции пузыря несмотря на локальное повреждение, вызванное заморозкой.
Пробуждение собственных защитных сил организма
Исследователей также интересовало, не активизирует ли замораживание опухоли иммунную систему. При гибели клеток от экстремального холода может происходить выделение раково‑связанных белков в форме, которую иммунная система способна распознать. В этом исследовании образцы тканей из обработанных пузырей показали заметное повышение через несколько недель после криоаблации двух ключевых типов Т‑лимфоцитов: CD4 и CD8. Эти иммунные клетки помогают координировать и выполнять прицельные атаки на атипичные клетки. Прирост был особенно выражен у мышей с реальной опухолью мочевого пузыря, что указывает на то, что иммунный ответ был направлен не только на неспецифическое повреждение, но и на опухоле‑специфические сигналы в зоне обработки. Любопытно, что сходных изменений не наблюдали в селезёнке, важном иммунном органе, что говорит о локализованном ответе в самом пузыре, а не о системной активации.
Что это может значить для будущей онкологии
В совокупности результаты указывают, что тщательно контролируемое замораживание может уменьшать инвазивные опухоли мочевого пузыря у мышей, не увеличивать число пероперационных смертей, сохранять базовое мочеиспускание и привлекать полезные иммунные клетки в обрабатываемую область. Хотя работа выполнена с наружным зондом в мелких животных, те же принципы могут послужить основой для разработки устройств, замораживающих опухоль изнутри у людей. Если такие подходы подтвердят безопасность и эффективность в дальнейших исследованиях, они могли бы однажды предложить пациентам промежуточный путь между крупной органосберегающей операцией и менее эффективными методами — использовать холод не только для уничтожения видимого рака, но и для помощи организму в отслеживании его возврата.
Цитирование: Inui, S., Ito, S., Ueda, T. et al. Efficacy and safety of cryoablation procedures using mouse models of bladder cancer. Sci Rep 16, 5157 (2026). https://doi.org/10.1038/s41598-026-35571-w
Ключевые слова: рак мочевого пузыря, криоаблация, сохранение органа, онкоиммунология, мышиная модель