Clear Sky Science · ru
Сравнительная геномика множественно устойчивого к антибиотику колистину Pseudomonas aeruginosa выявляет новые линии в Таиланде
Почему этот внутрибольничный микроб важен для всех
Pseudomonas aeruginosa — внутрибольничный патоген, который атакует людей в самые уязвимые моменты — после операций, при подключении к аппарату искусственной вентиляции лёгких либо при тяжёлых ожогах или заболеваниях лёгких. В течение многих лет врачи полагались на мощный «антимикробный препарат последней инстанции» — колистин, когда другие антибиотики не действовали. В этом исследовании проанализированы штаммы Pseudomonas из больниц по всей территории Таиланда, которые больше не реагируют на колистин и на многие другие антибиотики. Прочитав полные геномы этих бактерий, исследователи показали, как распространяются новые высокоустойчивые линии, и почему это должно вызывать беспокойство у пациентов, клиницистов и систем здравоохранения во всём мире.
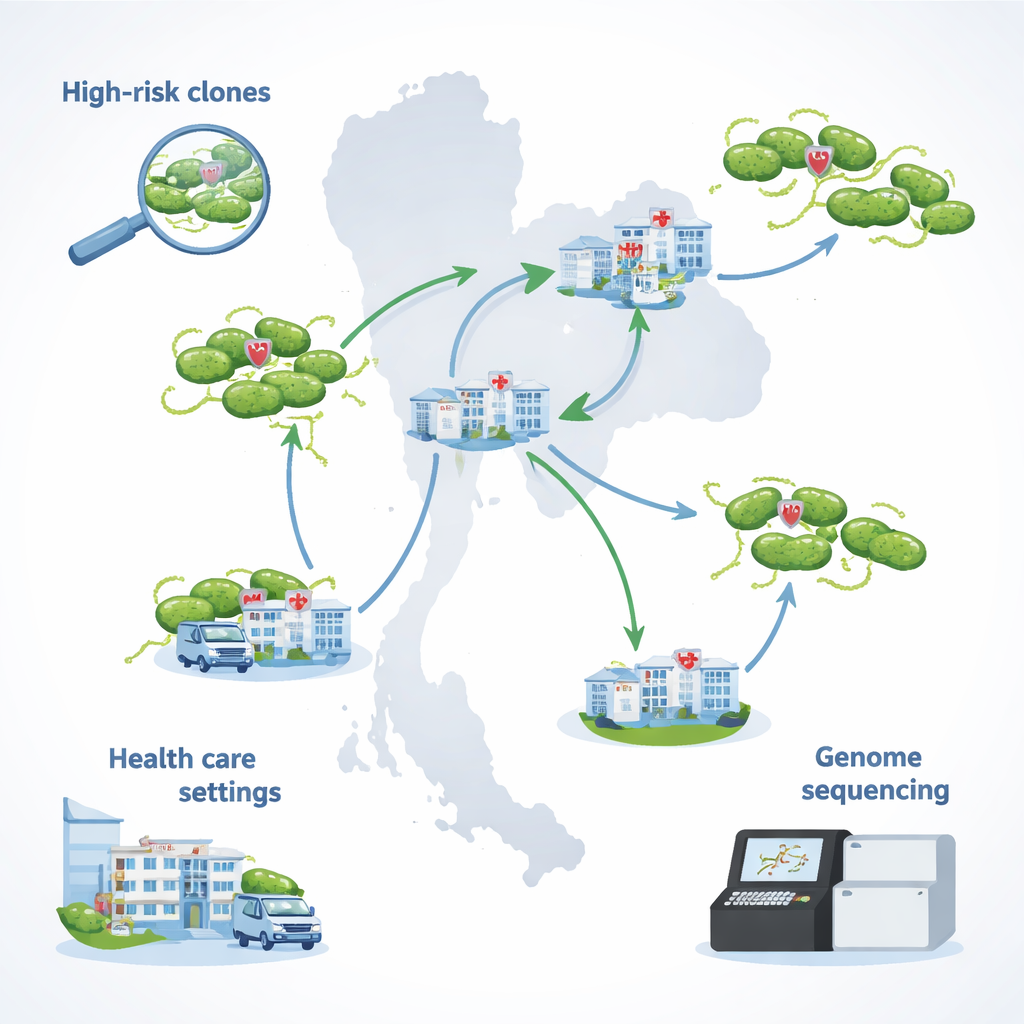
Отслеживание трудноизлечимой инфекции по всей территории Таиланда
Команда сосредоточилась на 29 штаммах Pseudomonas aeruginosa, собранных в 2021–2022 годах в больницах, участвующих в национальной программе надзора за устойчивостью к антибиотикам в Таиланде. Все эти штаммы были множественно устойчивыми: они выдерживали воздействие нескольких основных классов антибиотиков, включая препараты, обычно применяемые при тяжёлых инфекциях. Существенно, что они также не были полностью чувствительны к колистину — препарату, который часто оставляют в резерве для угрожающих жизни случаев. Большинство образцов взято из мочи, но другие — из крови, мокроты, гноя и хирургических дренажных жидкостей, что отражает разнообразие инфекций, которые этот микроорганизм вызывает у госпитализированных пациентов.
Чтение «отпечатков» генома бактерий
Используя сочетание краткочтения и длинночтения ДНК‑секвенирования, исследователи собрали высококачественные геномы для каждого штамма. Затем они сравнили эти геномы, чтобы классифицировать бактерии по генетическим семьям, известным как последовательностные типы. Были обнаружены девять различных последовательностных типов, что указывает на значительное разнообразие. Один из них, обозначенный как ST5340, ранее не описывался. Оказалось, что он тесно связан с известным международным клоном высокого риска ST357, отличаясь только в одном из семи стандартных «гомеостатических» генов. Несмотря на это родство, ST5340 выделялся тем, что все его изоляты сопротивлялись всем протестированным антибиотикам, что делает эту линию особенно тревожной.
Появляющиеся линии высокого риска и их распространение
Сопоставив мелкие различия в ДНК — однонуклеотидные полиморфизмы — в 108 тайских геномах Pseudomonas (29 новых и 79 из публичных баз данных), команда построила филогенетическое древо штаммов, циркулирующих в стране. Этот анализ выделил несколько доминирующих кластеров, сосредоточенных вокруг ST5340, ST357, ST654 и ST235 — линий, уже известных или появляющихся как «высокого риска», поскольку они часто устойчивы к множеству препаратов и вызывают внутрибольничные вспышки. В особенности ST5340 был обнаружен в нескольких провинциях и регионах, что указывает на широкое распространение, а не на ограниченность одной больницей. Также присутствовали другие глобальные клоны высокого риска, такие как ST654 и ST235, тогда как некоторые важные в мировом масштабе линии, например ST244, оказались отсутствующими — вероятно потому, что в исследование вошли только штаммы, несусцептивные к колистину.
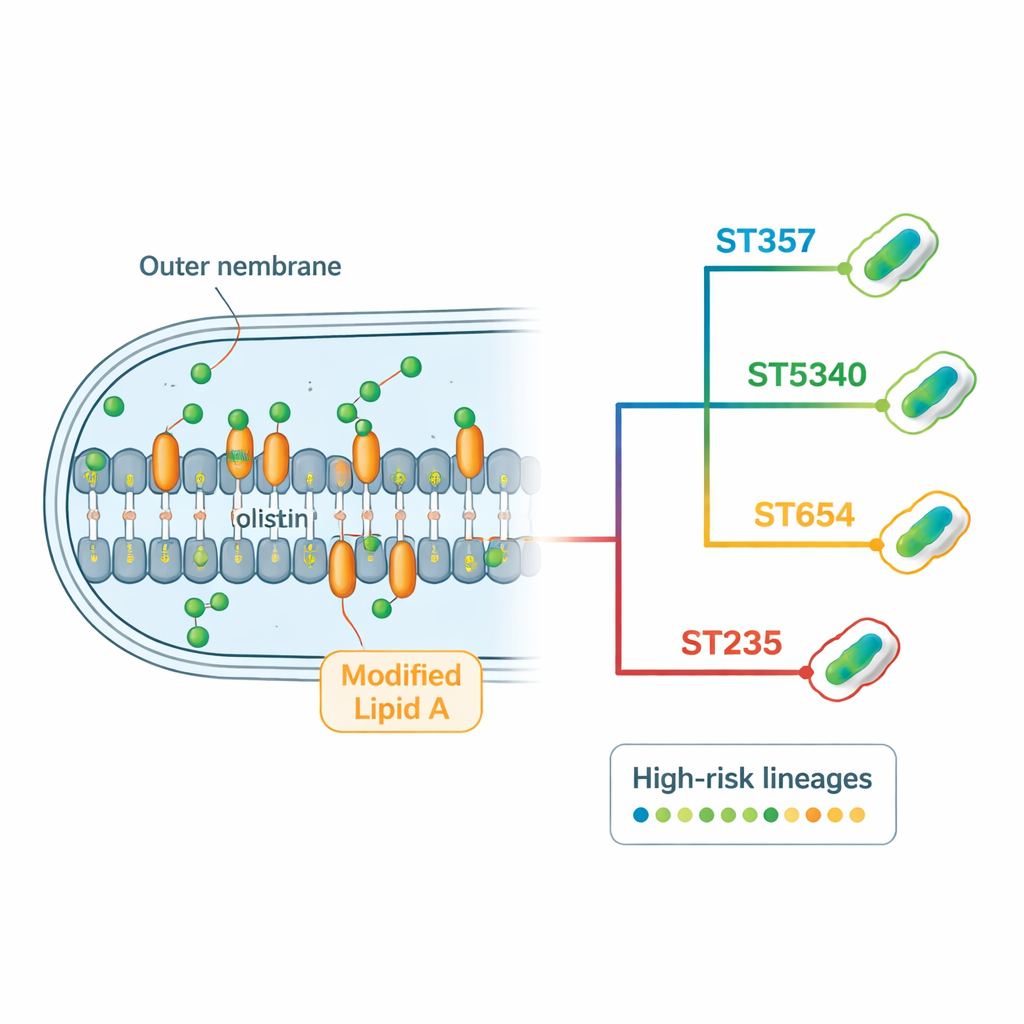
Как эти бактерии переигрывают антибиотики
Геномный анализ выявил насыщенный «резистом» — полный набор генов и мутаций, отвечающих за устойчивость, который несёт каждый штамм. Многие изоляты кодировали несколько типов бета‑лактамаз — ферментов, расщепляющих распространённые антибиотики, такие как пенициллины, цефалоспорины и карбапенемы. Ген карбапенемазы blaNDM‑1, связанный с устойчивостью к некоторым из самых мощных внутрибольничных препаратов, встречался почти во всех штаммах, иногда в нескольких копиях. Бактерии также несли гены, химически модифицирующие аминогликозидные антибиотики, а также мощные выбрасывающие насосы (efflux‑pump), которые действуют как молекулярные помпы, удаляющие препараты из клетки. Для колистина команда не обнаружила мобильных генов резистентности, но выявила повторяющиеся изменения в хромосомных генах, вовлечённых в строение наружной мембраны и её регуляцию. Отдельные мутации в регуляторных белках и в ферментах, формирующих липид A, были тесно связаны с устойчивостью к колистину, особенно в доминирующих линиях ST357 и ST5340.
Что это означает для пациентов и больниц
Сочетая национальный надзор с современным геномным секвенированием, это исследование демонстрирует, что больницы Таиланда сталкиваются с растущей угрозой со стороны недавно выявленного клона высокого риска ST5340 наряду с уже известными глобальными проблемными штаммами. Эти бактерии устойчивы не только к колистину, но и ко многим другим ключевым препаратам, резко сужая варианты лечения при развитии тяжёлых инфекций. Для непрофессиональной аудитории посыл ясен: устойчивость к антибиотикам — это не абстрактный риск будущего, а реальность настоящего, которая может напрямую повлиять на исход операций, реанимационных вмешательств и онкологического лечения. Авторы аргументируют, что необходимы непрерывный геномный надзор, более строгий контроль инфекций и бережное использование антибиотиков, чтобы предотвратить дальнейшее распространение этих высокоустойчивых линий и сделать их ещё труднее контролируемыми.
Цитирование: Wankaew, N., Arigul, T., Kruasuwan, W. et al. Comparative genomics of colistin-nonsusceptible multidrug-resistant Pseudomonas aeruginosa reveals emerging lineages in Thailand. Sci Rep 16, 5968 (2026). https://doi.org/10.1038/s41598-026-35520-7
Ключевые слова: Pseudomonas aeruginosa, устойчивость к антибиотикам, колистин, геномный надзор, внутрибольничные инфекции