Clear Sky Science · ru
Плазменный экзосомальный hsa-miR-339-5p ассоциирован с NOD-подобным рецептором с CARD-доменом 5 при сердечной недостаточности с сохранённой фракцией выброса
Почему крошечные молекулы в крови могут выдавать проблемы сердца
Сердечная недостаточность с пониженной фракцией выброса (HFrEF) — распространённое состояние, при котором сердце уже не способно перекачивать достаточно крови для потребностей организма. Врачам часто удаётся диагностировать его лишь после того, как повреждения стали значительными. В этом исследовании изучают, могут ли микроскопические сигналы, циркулирующие в крови — небольшие РНК-молекулы, упакованные в крошечные пузырьки, называемые экзосомами — заранее указывать на проблему и прояснять, как со временем сердце уплотняется и рубцуется.
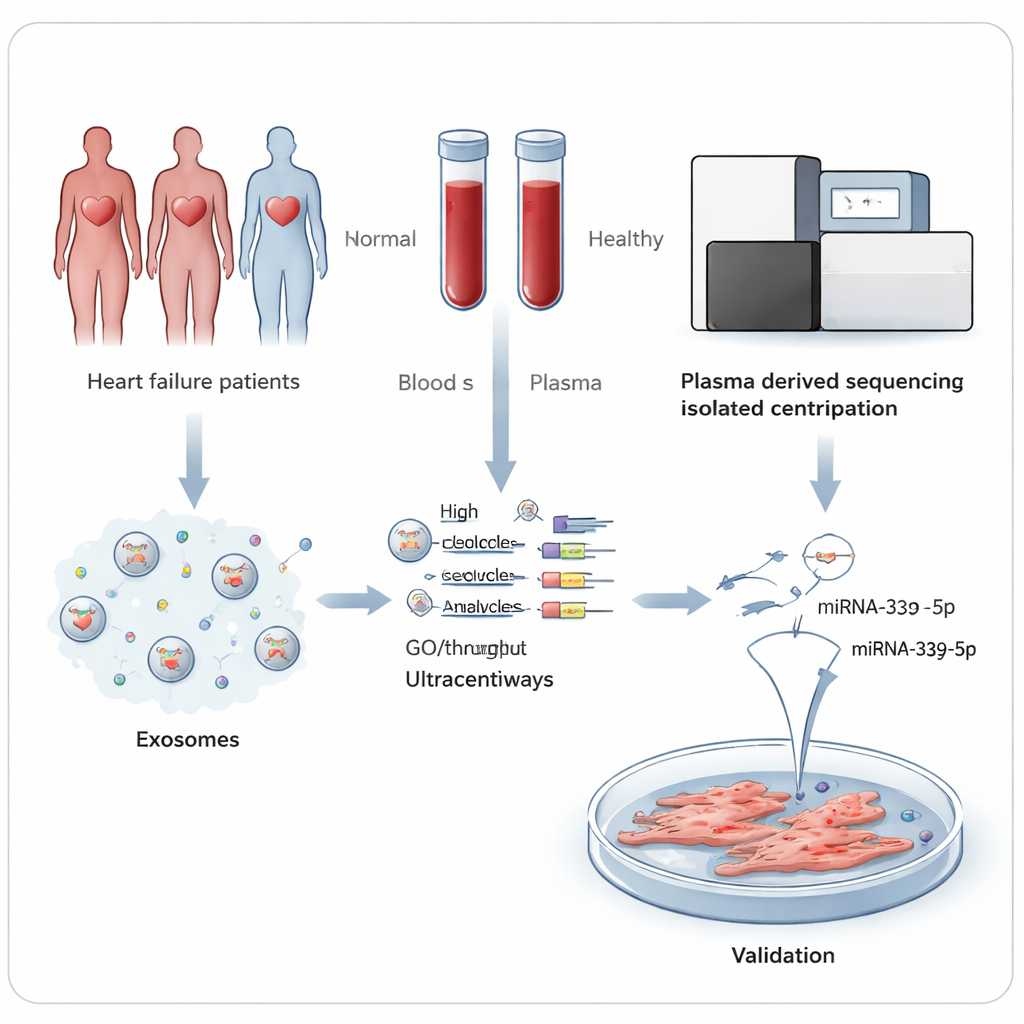
Скрытые послания в кровотоке
В нашей крови присутствуют бесчисленные экзосомы — нанометровые везикулы, выпущенные клетками и переносящие белки и генетический материал от одной клетки к другой. Среди их груза находятся микроРНК — короткие цепочки, которые точно регулируют, какие гены включаются или выключаются. Поскольку экзосомы защищают эти микроРНК от разрушения, их можно надёжно измерить в простом образце крови. Исследователи предположили, что если у больного сердца или связанных с ним тканей состав микроРНК в экзосомах отличается от такового у здорового сердца, эти шаблоны могут служить сигнальными маркерами и одновременно раскрывать процессы, движущие болезнь.
Сравнение пациентов с ослабленным сердцем и здоровых добровольцев
Группа собрала кровь у 45 человек с HFrEF и у 45 сопоставимых, но здоровых добровольцев в больнице в Хэфэе, Китай. Из плазмы крови они аккуратно выделили экзосомы и подтвердили их размер и форму с помощью электронной микроскопии и приборов для отслеживания частиц. На первом этапе они секвенировали малые РНК внутри экзосом у подгруппы из пяти пациентов и пяти контролей. Этот высокопроизводительный подход обнаружил сотни известных микроРНК и выделил 27, чьи уровни явно различались между двумя группами — 10 были повышены и 17 понижены у людей с сердечной недостаточностью.
Уточнение одного заметного сигнала
Чтобы проверить, какие из этих изменений наиболее надежны, учёные затем использовали высокочувствительный PCR для измерения шести перспективных микроРНК у всех оставшихся 40 пациентов и 40 контролей. Несколько сигналов подтвердились, но особенно выделялась одна — hsa-miR-339-5p. Она последовательно была выше у пациентов с HFrEF и, при анализе в качестве диагностического маркера, лучше всего отличала их от здоровых участников. Компьютерный анализ путей предположил, что эта микроРНК может влиять на ген под названием NLRC5, который, в свою очередь, действует на ключевой путь роста и выживания в клетке — PI3K/Akt, ранее связанный с утолщением сердечной мышцы и образованием рубцов.
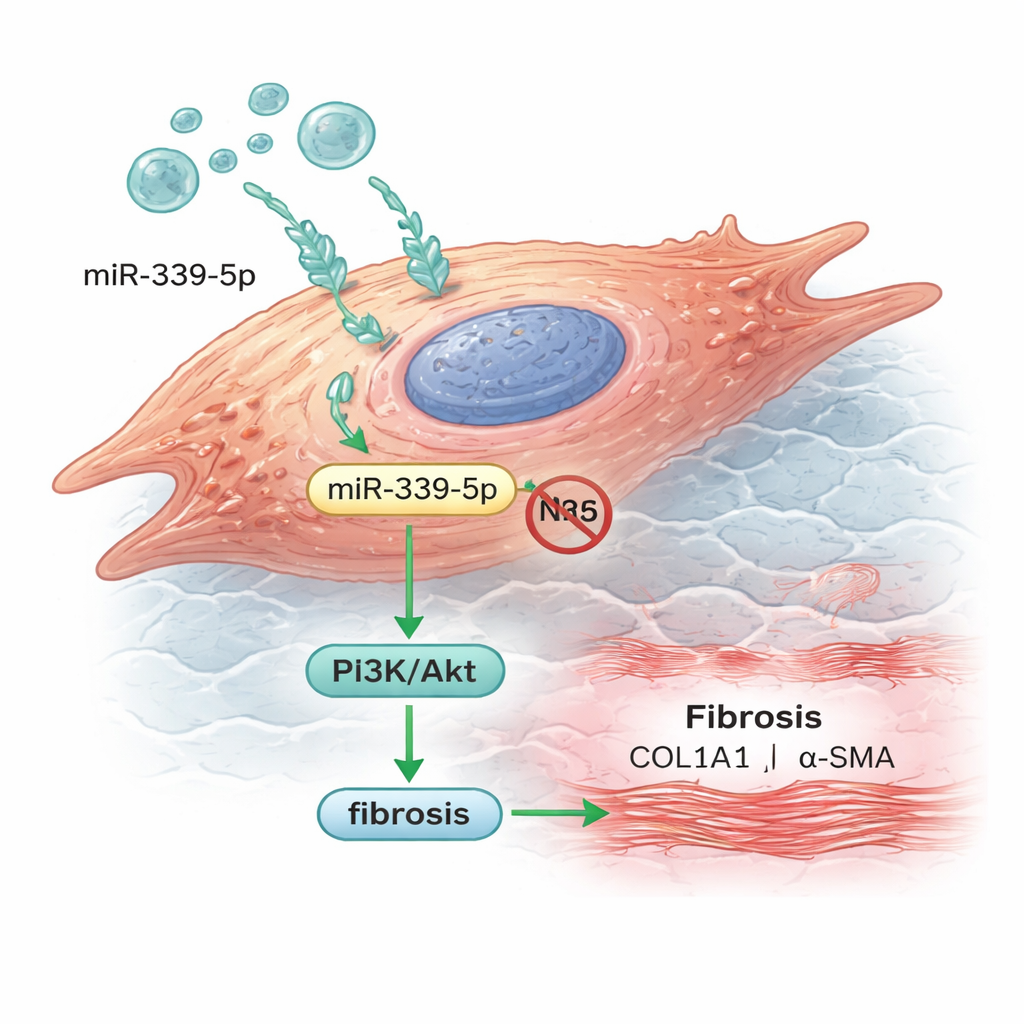
От маркера в крови к фактору фиброзирования
Исследователи затем перешли к клеткам, похожим на сердечные, выращенным в лаборатории, чтобы посмотреть, как эта микроРНК ведёт себя в ткани. Они показали, что экзосомы от пациентов легко захватываются человеческими кардиомиоцитами, доставляя miR-339-5p в клетки. При искусственном повышении miR-339-5p уровни NLRC5 снижались, а путь PI3K/Akt становился более активным. Одновременно клетки вырабатывали больше коллагена и белка альфа-гладкомышечного актина — оба признака фиброзной, жёсткой ткани, а не гибкой здоровой мышцы. Блокирование miR-339-5p обращало эти изменения, что говорит о том, что эта единичная микроРНК способствует смещению сердечных клеток в состояние, приводящее к образованию рубцов.
Что это значит для пациентов и будущей терапии
Прослеживая эту цепочку событий — от повышенного уровня miR-339-5p в плазменных экзосомах до снижения NLRC5, активации сигнального пути PI3K/Akt и увеличения белков рубцевания — исследование связывает измеримый маркер крови с правдоподобным механизмом повреждения внутри сердца. Для пациентов это открывает возможность, что рутинный анализ крови однажды поможет выявлять вредные ремоделирования раньше, чем позволяют нынешние сканирования и лабораторные маркеры. Также это указывает на перспективу, что лекарственные средства, направленные на снижение miR-339-5p или восстановление активности NLRC5, могут замедлить уплотнение и образование рубцов, усугубляющие сердечную недостаточность. Хотя требуются более крупные и длительные исследования, эти крошечные РНК-послания могут стать и индикатором тревоги, и новой мишенью для лечения.
Цитирование: Cheng, D., Hu, J., Zhao, M. et al. Plasma exosomal hsa-miR-339-5p is associated with NOD-like receptor family CARD domain-containing 5 in heart failure with reduced ejection fraction. Sci Rep 16, 5690 (2026). https://doi.org/10.1038/s41598-026-35519-0
Ключевые слова: сердечная недостаточность, экзосомы, микроРНК, фиброз, биомаркеры