Clear Sky Science · ru
Структурно- и вычислительно обоснованная разработка аналогов 2,5-дисубституированных-1,3,4-оксадиазолов как активных ингибиторов LOX, уреазы и α-глюкозидазы
Новые химические инструменты против распространённых заболеваний
Многие повседневные проблемы со здоровьем — от язв и камней в почках до диабета и хронического воспаления — вызваны чрезмерной активностью определённых ферментов в организме. В этом исследовании рассматривается семейство недавно спроектированных малых молекул, которые выполняют роль «тормозов» для трёх таких ферментов. Путём настройки их структуры и проверки в лаборатории и с помощью вычислительных методов исследователи стремятся заложить основу для более эффективных и безопасных лекарств в будущем. 
Почему эти ферменты важны
Команда сосредоточилась на трёх ферментных мишенях, которые выполняют очень разные, но одинаково важные функции для здоровья. Уреаза помогает расщеплять мочевину; когда она чрезмерно активна в некоторых бактериях или тканях, это может способствовать язвам желудка и мочевыводящих путей, образованию камней в почках и даже повышению артериального давления. Альфа‑глюкозидаза располагается на поверхности клеток кишечника и расщепляет сложные углеводы до глюкозы; её блокирование — хорошо известный способ контроля уровня сахара при диабете 2 типа. Липооксигеназа (LOX) превращает липиды в сигнальные молекулы, которые запускают воспаление, астму и некоторые процессы, связанные с раком. Поэтому весьма востребованы препараты, которые ослабляют активность этих ферментов, не причиняя вреда другим системам организма.
Создание библиотеки кандидатных молекул
Для поиска таких препаратов исследователи создали серию из 15 родственных соединений на основе гетероциклической системы 1,3,4‑оксадиазола, связанного с пиперидиновым фрагментом. Эта химическая «основа» уже присутствует в нескольких современных лекарствах и известна хорошей взаимодействующей способностью с биологическими мишенями. Команда варьировала «украшения», прикреплённые к этому ядру — небольшие группы, такие как метил, этил, метокси, бензил и циклогексил — в разных положениях, создав библиотеку кандидатов, обозначенных как 7a–7o. Структуры каждого соединения были подтверждены стандартными аналитическими методами, такими как инфракрасная и ядерно‑магнитно‑резонансная спектроскопия, что гарантировало соответствие полученных веществ проектным структурам.
Оценка способности молекул блокировать ферменты
Каждое соединение затем тестировали против очищенных ферментов LOX, уреазы и α‑глюкозидазы, чтобы оценить, насколько сильно оно способно замедлять ферментную активность. Несколько молекул выделялись. В отношении α‑глюкозидазы соединения 7a и 7n оказались особенно эффективными, превзойдя эталонный препарат для диабета акарабоз в лабораторных тестах, достигая высокого процента ингибирования при низких микромолярных концентрациях. Для LOX соединения 7a, 7h и 7n показали очень сильную активность, в некоторых случаях лучше, чем природный референтный ингибитор кверцетин. В испытаниях уреазы соединения 7a и особенно 7l соперничали с эталонным ингибитором тиоуреей или слегка его превосходили, что указывает на их перспективу в качестве лидов для разработки противоязвенных или противокаменных средств. 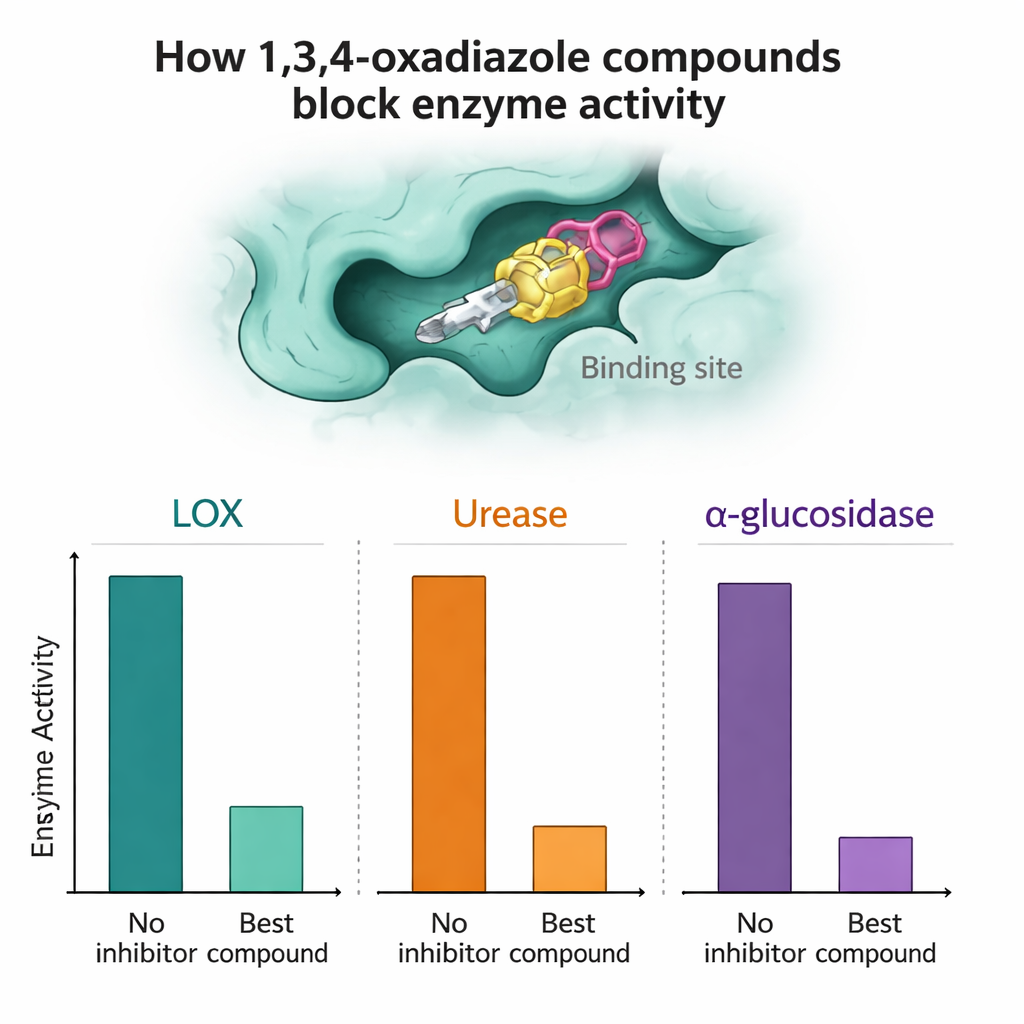
Связь структуры с активностью
Поскольку единственные различия между соединениями 7a–7o — это небольшие изменения вокруг основного кольцевого фрагмента, исследователи смогли начать картирование простых зависимостей «структура–активность». Например, добавление небольших углеродистых групп в определённых «орто»-положениях присоединённого фенильного кольца часто усиливало способность блокировать α‑глюкозидазу или LOX. Другие заместители, такие как некоторые метокси‑ или эфирные группы, размещённые менее удачно, как правило, ослабляли активность. Чтобы понять причины, команда использовала компьютерные симуляции. Квантово‑химические расчёты показали, что все молекулы термодинамически стабильны и достаточно гибки, чтобы адаптироваться к ферментным карманам. Докинг‑исследования — виртуальная подгонка каждой молекулы в трёхмерные модели ферментов — выявили, что наиболее активные соединения устанавливали более плотные контакты за счёт комбинации водородных связей и гидрофобных взаимодействий в ключевых точках активных центров, тогда как менее активные кандидаты располагались менее плотно или упускали критические точки контакта.
Что это значит для будущих лекарств
Проще говоря, исследование выявляет несколько перспективных «ключей», которые хорошо подходят к трём связанным с заболеваниями «замкам», и начинает объяснять на атомном уровне, почему одни ключи поворачиваются лучше других. Ни одно из этих соединений пока не готово стать лекарством — им предстоит проверка безопасности, оптимизация фармакокинетики и испытания на животных и людях. Но работа показывает, что каркас 1,3,4‑оксадиазол–пиперидин является плодородной отправной точкой для будущих терапий, направленных на диабет, воспалительные состояния и заболевания, связанные с уреазой. Сочетание тщательных лабораторных измерений и подробного компьютерного моделирования даёт дорожную карту по доработке этих кандидатов в более точные и эффективные лекарства.
Цитирование: Javid, J., Aziz-ur-Rehman, Iqbal, J. et al. Structural and computational supported development of 2,5-disubstituted-1,3,4-oxadiazole analogues as active LOX, urease, and α-glucosidase inhibitors. Sci Rep 16, 5866 (2026). https://doi.org/10.1038/s41598-026-35499-1
Ключевые слова: ингибиторы ферментов, поиск лекарств, оксадиазольные соединения, диабет и воспаление, уреаза и липооксигеназа