Clear Sky Science · ru
SHP2 способствует остеосаркоме через регуляцию сигнальной оси STAT3/TET3/HOXB2
Почему это исследование костного рака важно
Остеосаркома — наиболее частая первичная опухоль кости у детей и подростков, и несмотря на современные химиотерапию и хирургическое лечение, выживаемость пациентов с распространённой или рецидивирующей формой заболевания за последние десятилетия почти не изменилась. В этом исследовании авторы изучают внутреннюю «проводку» клеток остеосаркомы, чтобы выяснить, какие молекулы выполняют роль «главных выключателей», помогая опухолям расти, распространяться и сопротивляться лечению. Выявив ключевой контролирующий путь, в центре которого — белок SHP2, работа указывает на новые лекарственные мишени, которые потенциально могут сделать терапию остеосаркомы более эффективной и точечной.
Идя по следам активности генов опухоли
Исследователи начали с того, что подошли к остеосаркоме как к задаче анализа данных. Они проанализировали публичные наборы данных экспрессии генов, сравнивая образцы опухоли с нормальной костной тканью, и применили статистические методы для выявления генов, которые стабильно включены или выключены при раке. Отличия обнаружились у сотен генов, многие из которых сгруппировались в известные онкологические пути, управляющие ростом клеток, их выживанием и подвижностью. Среди них выделялся один белок — SHP2, выступавший узлом, тесно связанным с несколькими другими: сигнальным фактором STAT3, ДНК‑модифицирующим ферментом TET3 и регулятором развития HOXB2. Это навело на мысль, что эти молекулы могут образовать связанную цепь, помогающую клеткам остеосаркомы вести себя агрессивно. 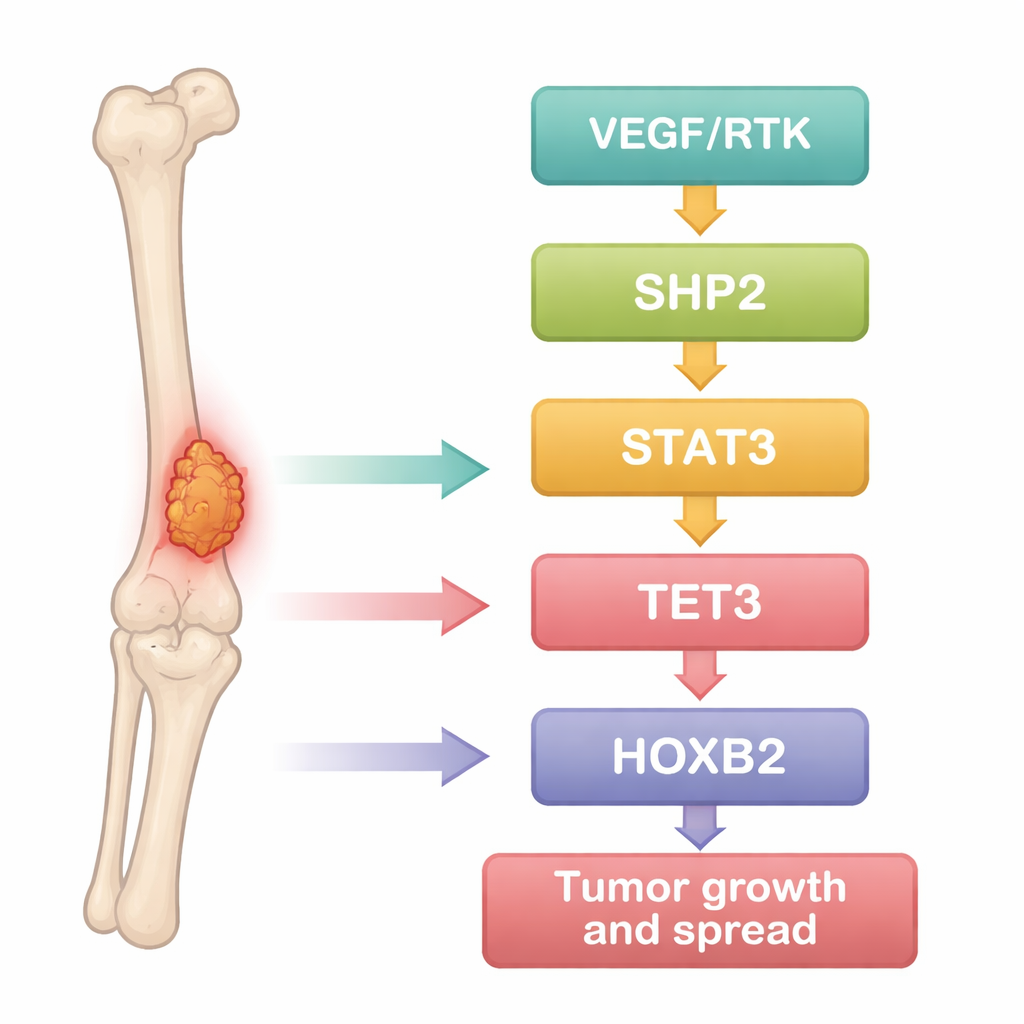
Проверка роли SHP2 в раковых клетках
Чтобы перейти от корреляций к причинно‑следственным связям, команда создала линии человеческих клеток остеосаркомы (143B и MG63) с пониженной или повышенной активностью SHP2. При подавлении SHP2 способность клеток к размножению, миграции по поверхности и инвазии через мембрану заметно снижалась. Также падали уровни белков STAT3, TET3 и HOXB2, а также онкологических маркеров, таких как c‑Myc, NANOG и NUSAP1. При реактивации STAT3 или сверхэкспрессии HOXB2 многие из этих эффектов обращались, что указывает на то, что SHP2 находится выше по цепочке и в конечном счёте влияет на гены, контролирующие деление клеток, стволоподобные свойства и механизмы митоза.
Построение пошаговой онкопути
Собрав результаты экспериментов воедино, авторы предлагают пошаговую модель. В микроокружении опухоли высокие уровни сосудистого эндотелиального фактора роста (VEGF) стимулируют рецепторные тирозинкиназы (RTK) на поверхности клеток. Те, в свою очередь, активируют SHP2 внутри клетки. Активный SHP2 включает STAT3 — транскрипционный фактор, который перемещается в ядро и способствует увеличению продукции TET3. TET3 затем редактирует химические метки на ДНК, в частности удаляет метильные группы в области гена HOXB2. Эта деметилизация действует как снятие тормоза, позволяя HOXB2 сильнее экспрессироваться. HOXB2, ген, обычно участвующий в регулировании развития, теперь усиливает активность c‑Myc, NANOG и NUSAP1, которые совместно подпитывают неукротимый рост опухолевых клеток, повышают инвазивность и поддерживают черты, связанные с метастазированием.
От чашки Петри до живых животных
Чтобы проверить, имеет ли значение этот путь в целых опухолях, учёные имплантировали модифицированные клетки остеосаркомы подкожно мышам. Опухоли, развившиеся из клеток с повышенной экспрессией SHP2, были крупнее и тяжелее, чем контрольные. При подавлении TET3 в этих клетках, богатых SHP2, рост опухолей замедлялся, а уровни HOXB2 падали, хотя SHP2 и STAT3 оставались активными. Повторное введение HOXB2 восстанавливало агрессивность опухоли. По ходу исследований измерения уровней белков в тканях опухолей подтверждали выводы клеточных культур, что укрепляет идею о том, что SHP2, STAT3, TET3 и HOXB2 действуют как связанная ось, продвигающая остеосаркому к более злокачественному поведению. 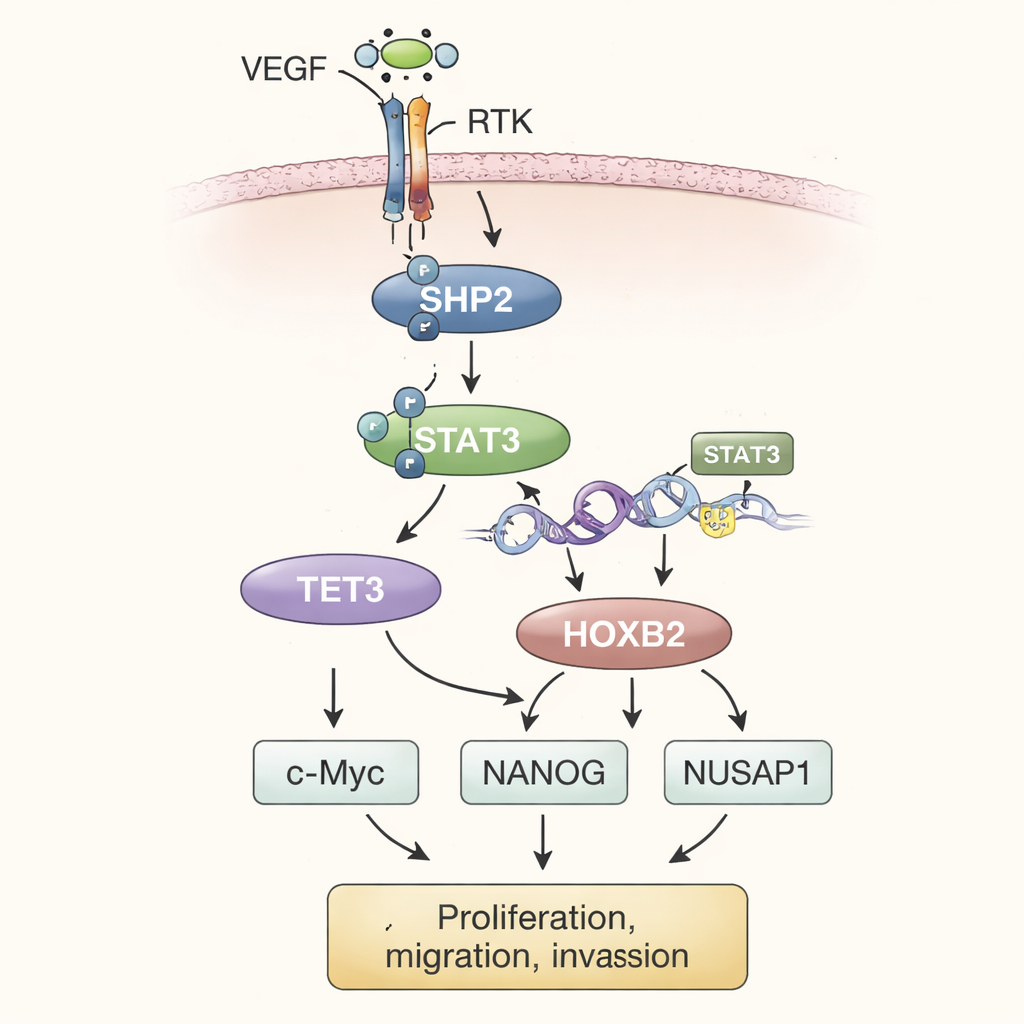
Что это значит для будущих методов лечения
Для неспециалиста главное в том, что исследователи проследили ясную сигнальную цепь — от VEGF и его поверхностных рецепторов через SHP2 и STAT3 к TET3, HOXB2 и нескольким мощным генам роста — которая помогает объяснить, почему остеосаркома может быстро расти и рано давать метастазы. Поскольку SHP2 и STAT3 — ферменты, которые теоретически можно блокировать малыми молекулами, а TET3 и HOXB2 представляют более поздние звенья того же пути, эта ось предоставляет несколько точек для потенциального терапевтического вмешательства. Хотя исследование выполнено на клеточных линиях и на мышах, оно даёт детальную карту, которую разработчики лекарств могут использовать при создании комбинированных подходов, направленных на отключение центральных управляющих переключателей опухоли, а не только на борьбу с её конечными проявлениями.
Цитирование: Yang, H., Ji, J. SHP2 promotes osteosarcoma via regulating STAT3/TET3/HOXB2 signaling. Sci Rep 16, 6158 (2026). https://doi.org/10.1038/s41598-026-35493-7
Ключевые слова: остеосаркома, SHP2, путь STAT3, опухолевые сигналы, таргетная терапия