Clear Sky Science · ru
Глобальный анализ экспрессии РНК в образцах пациентов выявил потенциальные диагностические биомаркеры, специфичные для перитонеального, яичникового и глубокого эндометриоза
Почему это состояние важно в повседневной жизни
Эндометриоз поражает примерно 190 миллионов женщин во всем мире, часто вызывая сильную тазовую боль, утомляемость и проблемы с фертильностью. Тем не менее многие люди ждут почти десятилетие, прежде чем получить четкий диагноз, который обычно подтверждается только при помощи операции. Это исследование задает простой, но важный вопрос: можно ли вместо этого «прочитать» молекулярные «отпечатки» организма, чтобы обнаруживать эндометриоз раньше и даже различать его формы с помощью простого теста в будущем?
Разные лица одного заболевания
Эндометриоз возникает, когда ткани, похожие на слизистую оболочку матки, растут в местах, где им не место — например на яичнике, на тонкой оболочке живота (перитонеуме) или глубоко в органах таза. Эти локализации определяют три основные подтипа: яичниковый, перитонеальный и глубокий эндометриоз. Каждый из них может вызывать разные модели боли, проблемы с фертильностью и повреждение органов. Сегодня врачи опираются на симптомы, визуализацию и часто лапароскопию — операцию под анестезией — чтобы подтвердить диагноз и определить подтип. Невмешательский способ различать эти формы избавил бы многих женщин от лет неопределенности и операций.
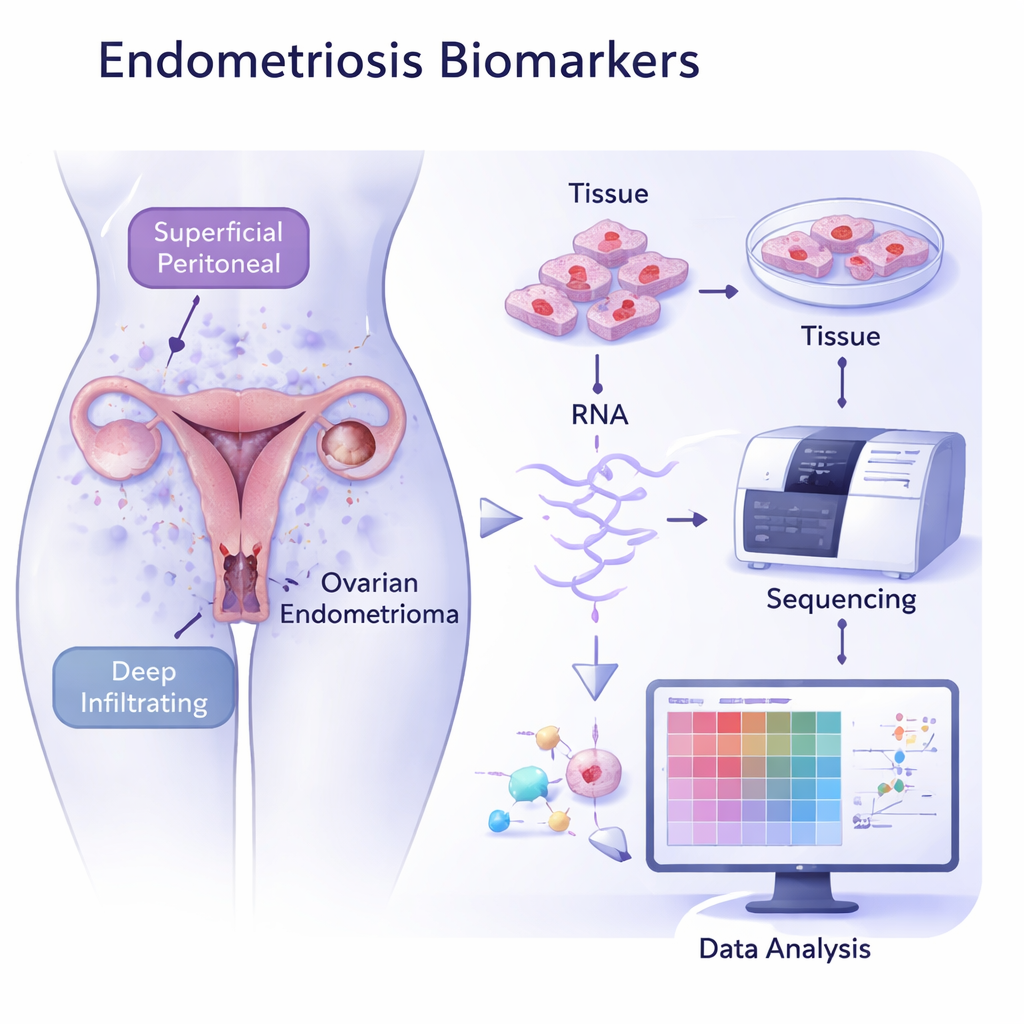
Чтение «штрихкода» РНК в пораженной ткани
Исследователи собрали образцы тканей у 26 женщин с эндометриозом — по всем трем подтипам — и у 15 женщин без заболевания. Затем они использовали секвенирование РНК, метод, измеряющий, какие гены включены или выключены, чтобы получить глобальную картину активности в этих тканях. При сравнении пораженной ткани с здоровой слизистой матки образцы разделились на отчетливые кластеры, выявив ясно различные паттерны генетической активности. Яичниковые очаги сформировали одну плотную группу, тогда как перитонеальные и глубокие очаги сгруппировались вместе, что поддерживает идею о том, что эти подтипы следуют разным биологическим путям, хотя и имеют общие черты.
Общие пути рубцевания и воспаления
Во всех трех подтипах команда обнаружила повышенную активность генов, связанных со строительством и ремоделированием внеклеточного матрикса, повышенную сократимость клеток, типичную для рубцевания, и сильную воспалительную сигнализацию. Эти изменения соответствуют тому, что врачи наблюдают клинически: жесткие, фиброзные поражения, вызывающие боль и спайки. Исследование также выявило измененный иммунный ландшафт в очагах. Так называемые M2-макрофаги, тип иммунных клеток, ассоциированных с заживлением ран и фиброзом, были особенно многочисленны, в то время как естественные киллеры (NK-клетки), важные для удаления аномальных клеток, были значительно снижены. Этот дисбаланс может помогать эндометриоидной ткани выживать и распространяться, несмотря на свое неправильное расположение.
Молекулярные подсказки, специфичные для подтипов
Помимо общих паттернов, каждый подтип имел свою молекулярную подпись. При глубоком и перитонеальном эндометриозе гены, вовлеченные в фосфодиэстеразную сигнализацию — пути, уже связанные с другими фибротическими заболеваниями — были значительно повышены. При яичниковом эндометриозе выделялись гены, связанные с презентацией антигенов и синтезом гормонов, что указывает на то, что в яичнике формируется особая биохимическая среда. Исследователи также изучали некодирующие РНК — молекулы, которые не кодируют белки, но могут регулировать генную активность. Они выявили несколько таких молекул, значительно увеличенных в целом или специфически в отдельных подтипах, что указывает на новые регуляторные участники и возможные биомаркеры, которые могут быть обнаружены в крови или других биологических жидкостях.
Многообещающие белковые маркеры для будущих тестов
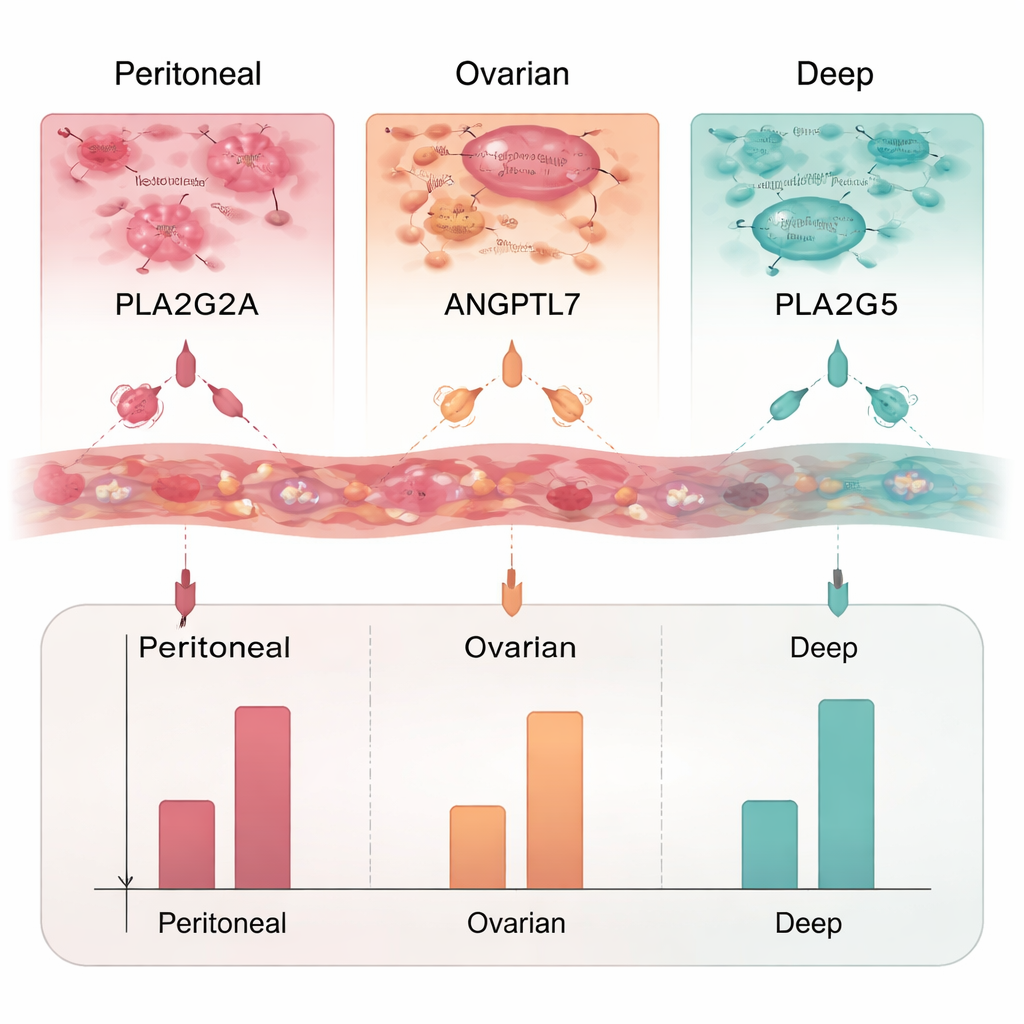
Из длинного списка измененных генов команда сосредоточилась на тех, которые кодируют секретируемые белки — идеальные кандидаты для будущего анализа крови. Они выбрали три белка для более детального изучения: PLA2G2A, ANGPTL7 и PLA2G5. С использованием ELISA, лабораторного метода измерения уровня белков, они обнаружили, что PLA2G2A повышен во всех трех типах эндометриоза, особенно при яичниковых очагах. ANGPTL7 был увеличен преимущественно при глубоком и перитонеальном эндометриозе, тогда как PLA2G5 повышался только при глубоком эндометриозе. В совокупности эти белки образуют потенциальную панель, которая может не только указывать на присутствие эндометриоза, но и подсказывать, где локализованы очаги.
Что это значит для пациентов
Это исследование пока не дает готового анализа крови, но закладывает важную основу. Картируя поведение тысяч генов и иммунных клеток в различных подтипах эндометриоза, исследование выделяет конкретные белки — PLA2G2A, ANGPTL7 и PLA2G5 — которые в будущем можно будет измерять неинвазивно. Если эти маркеры подтвердятся в больших независимых выборках пациентов, комбинации таких показателей могли бы сократить долгий путь к диагнозу, уменьшить необходимость в хирургии только для подтверждения заболевания и позволить более персонализированное лечение в зависимости от точного подтипа у женщины.
Цитирование: Lisá, Z., Fanta, M., Kokavec, J. et al. Global RNA expression analysis of patient samples identified potential diagnostic biomarkers specific for peritoneal, ovarian and deep endometriosis. Sci Rep 16, 5070 (2026). https://doi.org/10.1038/s41598-026-35467-9
Ключевые слова: эндометриоз, биомаркеры, секвенирование РНК, иммунные клетки, женское здоровье