Clear Sky Science · ru
Разработка глобальной системы скрининга для обнаружения белок–белковых взаимодействий с помощью люминесцентной комплементации в Schizosaccharomyces pombe
Освещая скрытую жизнь белков
Каждое биение сердца, мысль и вдох в наших телах зависят от того, как белки объединяются внутри клеток. Эти крошечные партнерства, называемые белок–белковыми взаимодействиями, контролируют всё — от того, как читаются гены, до того, как клетки реагируют на стресс. Многие из таких взаимодействий кратковременны или хрупки, поэтому их трудно обнаружить существующими инструментами. В этой работе описана новая, высокочувствительная «световая» система скрининга, созданная в простом модельном организме — дрожжах пондерм, — которая позволяет одновременно выявлять тысячи таких скрытых белковых связей.
Почему увидеть белковые партнерства так сложно
Белки редко действуют в одиночку. Они присоединяются к разным партнёрам в разное время, иногда лишь на мгновения, и их поведение может меняться из‑за химических модификаций или положения в клетке. Традиционные методы изучения таких взаимодействий либо выводят белки из их естественной среды, либо опираются на генетические хитрости, которые не улавливают все возможные пары. В результате существующие карты взаимодействий в клетке неполны. Авторы поставили задачу улучшить эту картину, создав более гибкую и чувствительную систему, способную обследовать почти все белки в дрожжах пондерм в живых клетках.
Преобразование прикосновения в свет
В основе нового подхода — расщеплённый фермент, который излучает свет. Одна часть, называемая LgBiT, прикреплена к «насадке» (bait) — белку, который исследователи хотят изучить. Другая часть, SmBiT, присоединена к множеству потенциальных «добыч» (prey), по одной на каждый штамм дрожжей. По отдельности эти части фермента почти не взаимодействуют. Но когда насадка и добыча связываются внутри клетки, две части соединяются, восстанавливая активный фермент, который светится в присутствии химического субстрата. Измеряя интенсивность света у каждого штамма дрожжей, команда может сказать, какие белки действительно встречаются в клетке и насколько сильно они взаимодействуют. Чтобы избежать пропуска партнёров из‑за того, что метка мешает нормальной функции белка, насадка производится в двух версиях — с LgBiT, прикреплённым к одному или другому концу — что значительно повышает шансы того, что хотя бы одна ориентация будет работать. 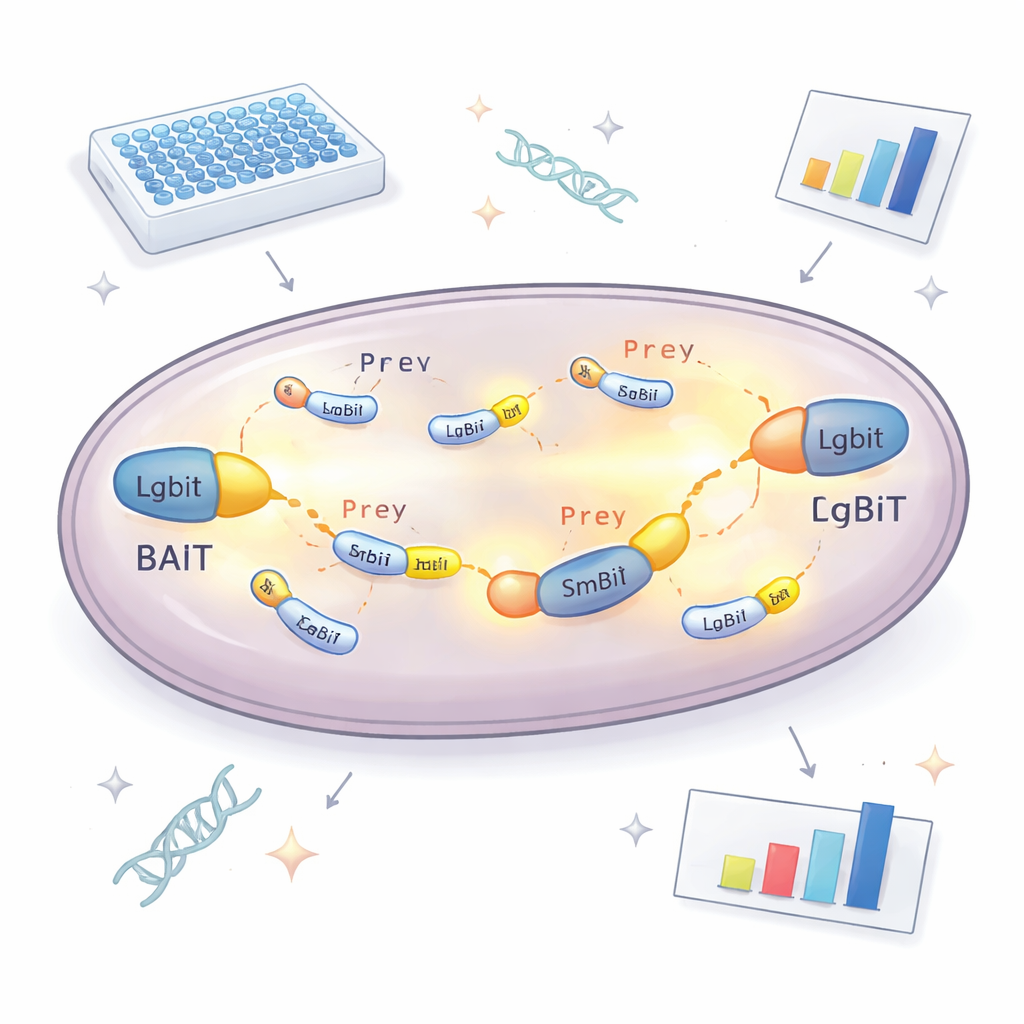
Создание библиотеки дрожжей и системы штаммов
Построение этой платформы требовало не только изобретательного фермента. Исследователям также пришлось вводить тысячи белков‑добычей в дрожжи контролируемым образом, по одному копию. Они разработали специальный ДНК‑вектор для белков‑добычей, который встраивается в определённое место в геноме дрожжей и содержит красный флуоресцентный маркер. Яркость этого красного сигнала отражает число вставленных копий, позволяя команде легко выбирать колонии с ровно одной копией — что важно для надёжных сравнений. Они также создали специализированные векторы для насадок, размещающие LgBiT в начале или конце белка‑насадки, разделённые гибкими линкерами, чтобы белок мог нормально сворачиваться и перемещаться. Были тщательно сконструированы штаммы дрожжей, способные одновременно содержать два конструкта насадки и один конструкт добычи, с использованием питательных маркеров, гарантирующих выживание только правильно собранных клеток.
Испытание системы
Чтобы проверить, действительно ли их конструкция улучшает обнаружение, учёные сначала изучили белки с хорошо известными партнёрами. Они подтвердили, что сила сигнала сильно зависит от того, к какому концу прикреплена светящаяся метка: некоторые взаимодействия проявлялись только при расположении LgBiT на одном конце насадки, а не на другом. Совместное экспрессирование обеих версий увеличивало световой сигнал, доказывая, что стратегия с двумя насадками облегчает улавливание слабых или чувствительных к ориентации взаимодействий. Система также фиксировала контакты с мембранными белками — класс, который традиционным методом двухгибридной системы дрожжей трудно анализировать. Имея это подтверждение, команда перешла к геномному скринингу, используя в качестве насадки белок, связанный с транскрипцией, Tfs1. Просканировав более 4600 белков‑добычей, они обнаружили 31 сильного кандидата, включая несколько уже известных партнёров и множество новых, некоторые из которых локализованы вне ядра, например в митохондриях и на поверхности клетки. 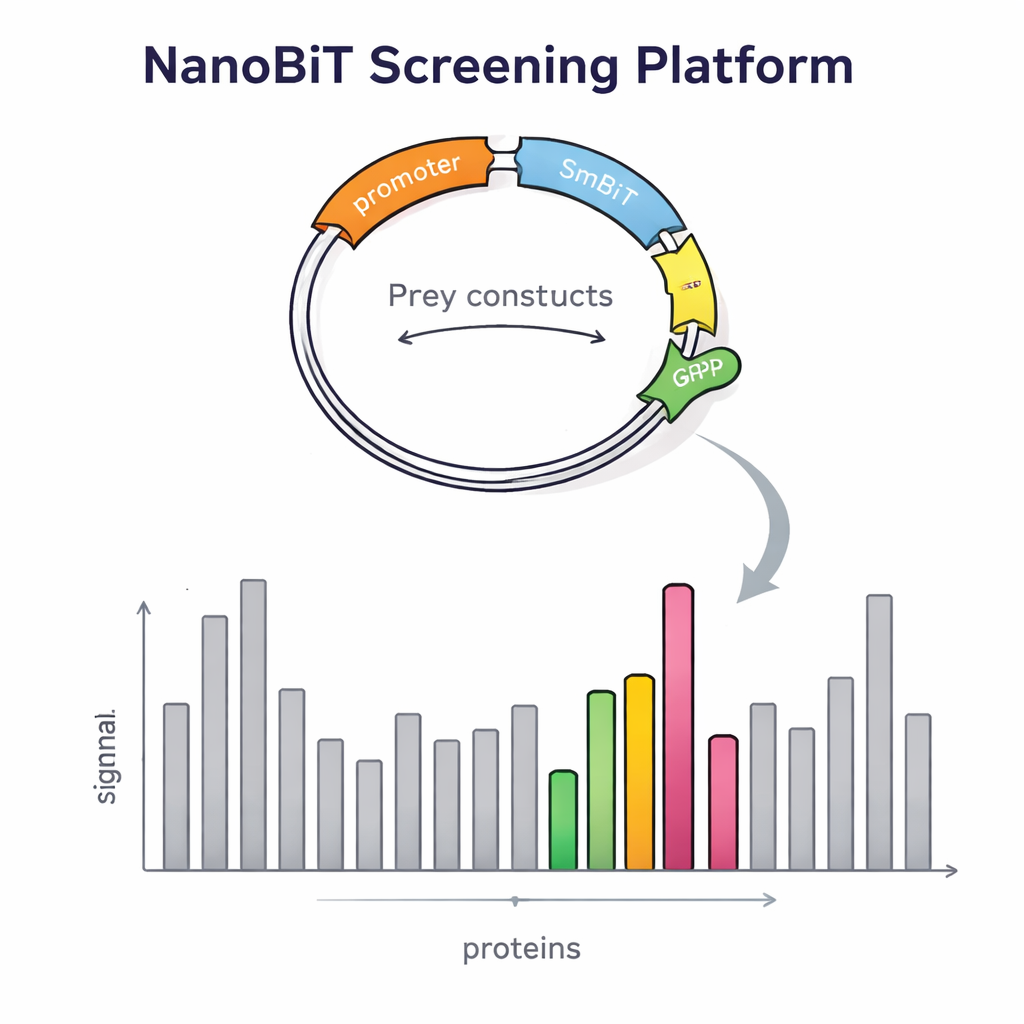
Что это значит для биологии и поиска лекарств
Для неспециалиста ключевая мысль такова: авторы создали более чувствительный «радар взаимодействий» внутри клеток дрожжей. Преобразуя короткие рукопожатия белков в измеримые вспышки света и грамотно организовав генетику так, чтобы три меченых белка могли экспрессироваться вместе, их система выявляет как известные, так и ранее невидимые белковые партнёрства. Хотя для подтверждения каждой новой пары по‑прежнему потребуются дополнительные методы, эта платформа заполняет важные пробелы в наших картах клеточных сетей. Поскольку штаммы также были сделаны более чувствительными к малым молекулам, ту же систему можно адаптировать для поиска препаратов, которые либо разрушают вредные белковые союзы, либо стабилизируют полезные, что даёт мощный новый инструмент как для фундаментальной биологии, так и для ранних этапов разработки лекарств.
Цитирование: Azadeh, F., Hashimoto, A., Nishimura, S. et al. Development of a global screening system for detecting protein–protein interactions by luminescence complementation in fission yeast. Sci Rep 16, 5034 (2026). https://doi.org/10.1038/s41598-026-35430-8
Ключевые слова: взаимодействия белков, Schizosaccharomyces pombe, люминесцентный тест, высокоэффективный скрининг, инструменты для поиска лекарств