Clear Sky Science · ru
Секретом, зависящий от частиц распознавания сигнала, у человека
Как клетки решают, какие белки покидают клетку
Наши клетки постоянно отправляют наружу белки, которые формируют гормоны, антитела и каркас между тканями. Но не каждый белок предназначен для транспортировки. В этом исследовании поднят фундаментальный, доселе не полностью решённый вопрос: как человеческие клетки определяют, какие белки полагаются на ключевого помощника — частицу распознавания сигнала (SRP), чтобы попасть в внутриклеточный «пункт отправки», а какие могут добраться туда без неё? Сопоставляя это решение сразу для тысяч белков, авторы показывают, кто зависит от SRP, кто обходится без него, и что происходит, когда эта система даёт сбой — тема, актуальная для многих заболеваний, связанных с неправильным направлением или отсутствием секретируемых белков.
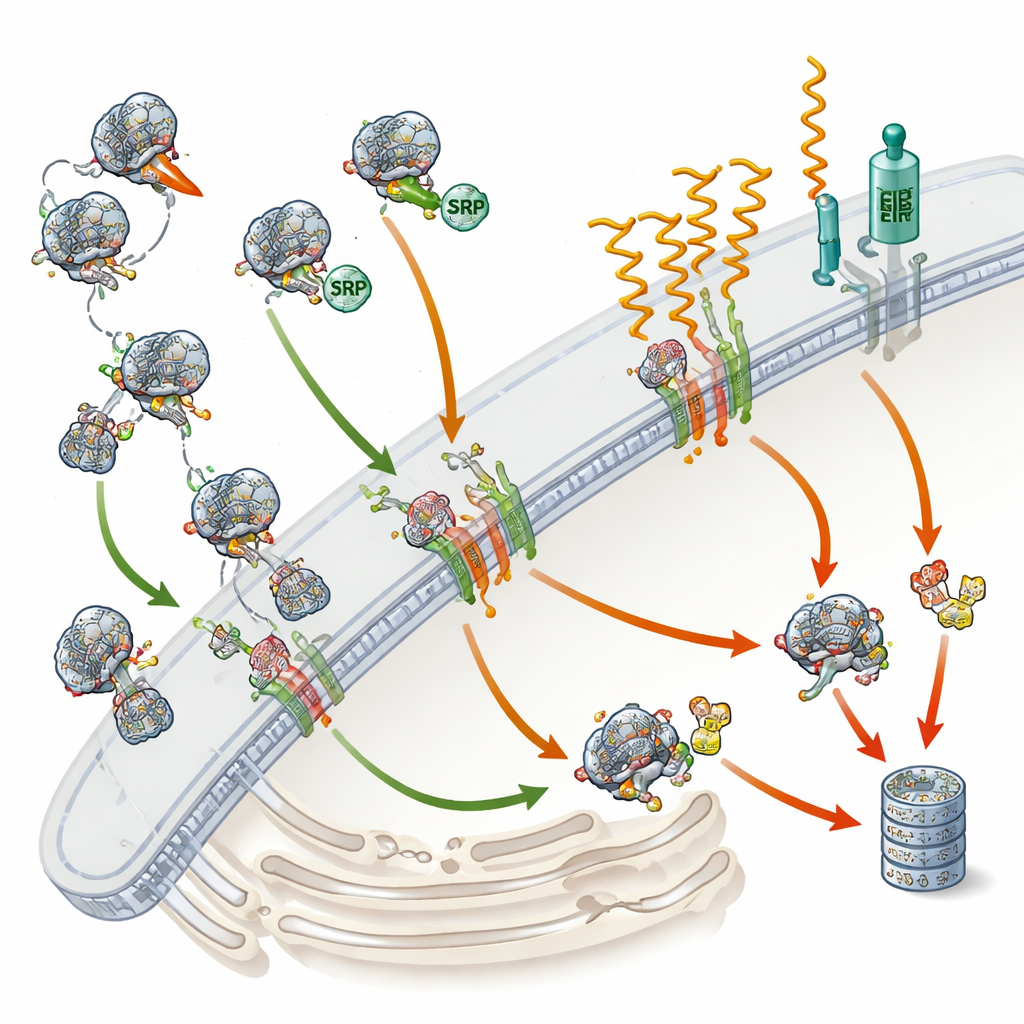
Порт отправки клетки и её главный проводник
Примерно один из трёх человеческих белков предназначен либо для поверхности клетки, клеточных мембран, либо для выделения за пределы клетки. Чтобы попасть в нужное место, большинству из этих белков сначала нужно войти в сеть внутренних мембран, называемую эндоплазматическим ретикулумом — «портом отправки» клетки. SRP выполняет роль проводника: она распознаёт небольшую «адресную метку» в начале вновь синтезируемых белков и временно приостанавливает их сборку. Эта пауза даёт рибосоме — машинке по производству белков — время пришвартоваться к эндоплазматическому ретикулуму, где сборка возобновляется, а растущий полипептид внедряется в мембрану или проходит через неё. Некоторые белки, однако, используют альтернативные пути, не требующие SRP, особенно очень маленькие белки или те, которые закреплены хвостом. До настоящего момента учёным не было известно в глобальном масштабе, какие именно человеческие белки действительно нуждаются в SRP, а какие могут её обходить.
Ослабляя SRP, чтобы увидеть, что ломается
Чтобы ответить на это, исследователи выборочно уменьшили уровень одного важного компонента SRP, SRP54, в человеческих клетках HeLa. Затем они использовали чувствительную методику масс-спектрометрии, чтобы измерить более 6000 белков внутри клеток и почти 2000 белков, присутствующих в окружающей жидкости, называемой кондиционированной средой. Сравнение клеток с нормальным уровнем SRP54 и с пониженным SRP54 позволило увидеть, какие белки стали менее выражены, какие увеличились и какие остались неизменными. Резкое падение уровня белка — особенно как внутри клетки, так и в среде — рассматривали как признак того, что этот белок зависит от SRP для правильного синтеза и маршрутизации.
Кто зависит от SRP, а кто справляется без него
Анализ показал, что большинство белков, обычно секретируемых в среду, явно зависят от SRP. При снижении SRP54 подавляющее большинство этих секретируемых белков, особенно несущих классическую сигнальную «адресную метку», резко снижались. Многие мембранные белки внутри клетки также уменьшались, что выявило их как клиентов SRP. Небольшая группа белков с похожими метками осталась в основном незатронутой, отмечая их как независимые от SRP; вероятно, они используют альтернативные пути попадания в эндоплазматический ретикулум. Исследователи также обнаружили, что конкретные особенности адресной метки — например, положительно заряженный участок в её начале — чаще встречались среди SRP-зависимых белков, что указывает на тонкие правила отбора груза SRP. В то же время некоторые белки, участвующие в пометке повреждённых белков для уничтожения, и белки, связанные с митохондриальной функцией, увеличивались, что говорит о том, что клетки активируют резервные системы и энергетическое производство, когда их главный проводник по доставке даёт сбой.
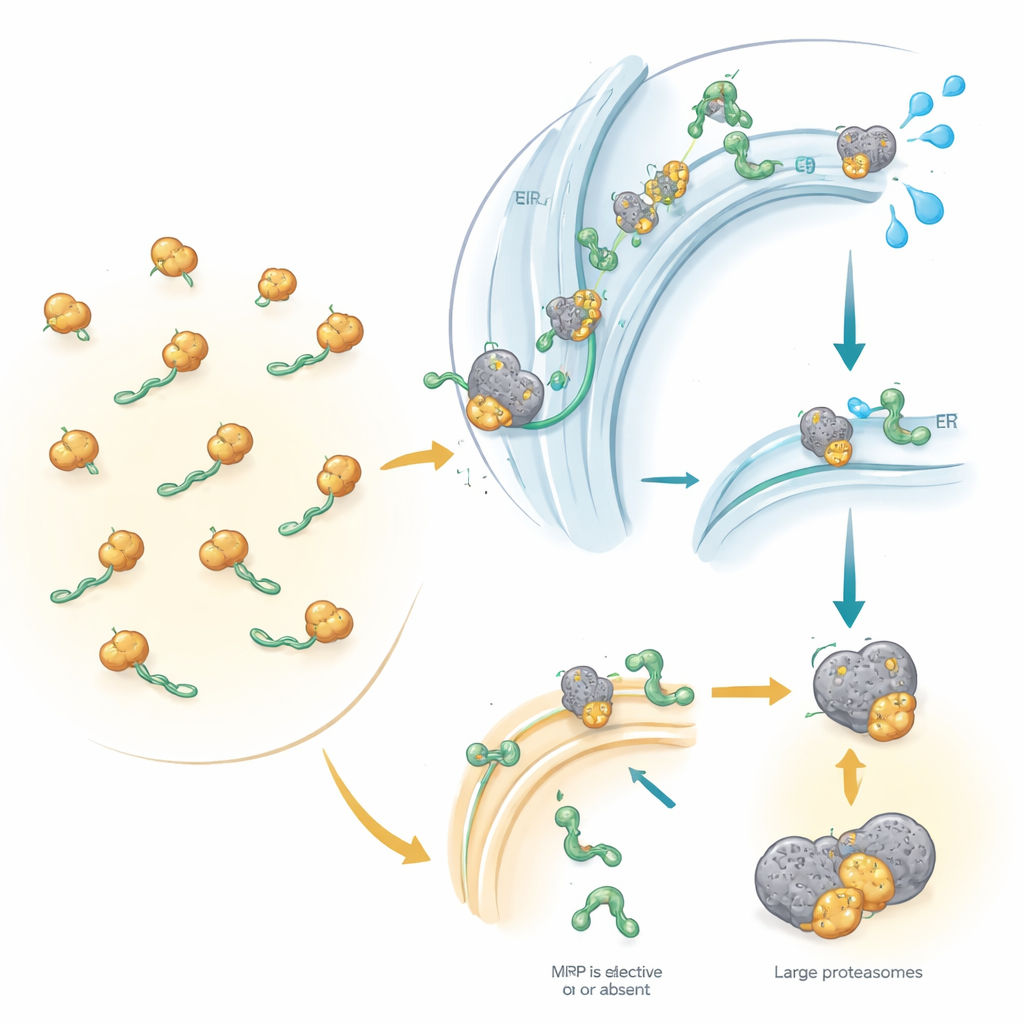
Контроль качества, когда нацеливание идёт не так
Исследование пошло дальше простого подсчёта белков: авторы сопоставили эти изменения со сдвигами в матричной РНК (мРНК), чертежах, используемых для синтеза белков. Многие SRP-зависимые белки теряли не только сам белок, но и соответствующие ему РНК-чертежи, что вовлекает путь контроля качества, известный как RAPP. Когда SRP не может надёжно взаимодействовать с формирующимся секреторным или мембранным белком, этот путь, по-видимому, запускает разрушение соответствующей мРНК, предотвращая дальнейшее производство неправильного белка. Одновременно незавершённые белки, не достигшие эндоплазматического ретикулума, вероятно, помечаются малыми молекулярными флажками и направляются к клеточным «измельчителям» — протеасомам. Интересно, что классические пути стресса эндоплазматического ретикулума не были сильно активированы, что намекает на то, что дефект SRP вызывает особый тип клеточной стресс-реакции.
Что это значит для здоровья и болезней
Проследив впервые в человеческих клетках, какие секретируемые и мембранные белки зависят от SRP, а какие нет, эта работа даёт справочную карту «правил доставки» в клетке. Результаты показывают, что большинство экспортируемых белков действительно полагаются на SRP и что при сбое SRP клетки реагируют деградацией и белков, и их чертежей, одновременно включая альтернативные механизмы выживания. Поскольку многие болезнетворные мутации затрагивают сигнальные «адресные метки» секретируемых белков, понимание того, как именно SRP распознаёт своих клиентов и как RAPP устраняет дефектные, может помочь объяснить, почему определённые мутации приводят к дефициту гормонов, проблемам иммунитета или нейродегенерации — и в конечном счёте указать пути для тонкой настройки маршрутизации белков в медицине.
Цитирование: Miller, S.C., Tikhonova, E.B., Rodríguez-Almonacid, C.C. et al. Signal recognition particle-dependent secretome in humans. Sci Rep 16, 8760 (2026). https://doi.org/10.1038/s41598-026-35427-3
Ключевые слова: секреция белков, частица распознавания сигнала, секретом, контроль качества белков, эндоплазматический ретикулум